FDA批准FIC药物Xphozah(tenapanor)用于降低成人CKD透析患者的血清磷水平
2023-10-20 MedSci原创 MedSci原创 发表于上海
10月18日,Ardelyx宣布,美国FDA批准“first-in-class”药物Xphozah(tenapanor)作为附加治疗用于降低接受成人慢性肾病(CKD)患者透析治
10月18日,Ardelyx宣布,美国FDA批准“first-in-class”药物Xphozah(tenapanor)作为附加治疗用于降低接受成人慢性肾病(CKD)患者透析治疗的血清磷水平。

图源:Ardelyx官网
Ardelyx, Inc.(纳斯达克股票代码:ARDX)是一家生物制药公司,其成立的使命是发现、开发和商业化创新的一流药物,以满足重大的未满足的医疗需求,今天宣布美国食品和药物管理局 (FDA) 已批准 XPHOZAH®(tenapanor),第一个也是唯一一个磷酸盐吸收抑制剂,用于降低患有慢性肾病(CKD)的成人透析患者的血清磷,作为对磷酸盐结合剂反应不足或患有慢性肾病的患者的附加治疗不能耐受任何剂量的磷酸盐结合剂疗法。 XPHOZAH 是一种单片剂,每日服用两次,具有一流的作用机制,可通过其主要途径阻止磷酸盐吸收。
“XPHOZAH 的批准对于透析患者、其家人和肾脏病护理界来说是一个重要的里程碑,因为它为尽管接受磷酸盐结合剂治疗但磷水平仍然升高的患者提供了一种新机制和新选择。 这对 Ardelyx 的每个人来说也是一项重大成就。”Ardelyx 总裁兼首席执行官 Mike Raab 说道。 “自 2007 年公司成立以来,我们一直坚定地致力于对肾脏界的承诺,今天的批准强化了 XPHOZAH 可能为众多患者提供的令人信服的临床特征和潜在益处。 这种疗法于 2008 年在我们的实验室诞生,现在看到它可供患者使用,确实证明了 Ardelyx 团队的奉献精神、出色的执行力和使命感。 此次获批也是对参与XPHOZAH研发的患者、家属、医生和临床试验人员的致敬。 肾脏界对 XPHOZAH 的推出抱有很高的期待和热情,我们的世界一流团队将以一流的产品进入市场。”
在美国约 55 万名 CDK 透析患者中,大多数人都患有高磷酸盐血症,目前高磷酸血症的治疗药物都是磷酸结合物,因此Xphozah作为一种口服磷酸盐吸收抑制剂,对于接受磷酸盐结合剂治疗但磷水平仍然升高的患者来说,它代表了一种新的机制和新选择,是一个重要的里程碑。
斯坦福大学医学教授 Glenn Chertow 博士补充道:“高磷血症管理一直是一个持续的临床挑战,因为尽管使用磷酸盐结合剂进行治疗,大多数接受维持性透析的患者仍无法持续达到目标血清磷酸盐浓度。 XPHOZAH 不是磷酸盐结合剂。 XPHOZAH 是一种磷酸盐吸收抑制剂。 对于对磷酸盐结合剂治疗没有充分反应的患者,XPHOZAH 已被证明有助于增加达到目标血清磷酸盐浓度的患者比例。 我相信 XPHOZAH 可以促进高磷血症患者的护理,提供具有补充作用机制的新治疗选择。”
支持 XPHOZAH 的临床数据
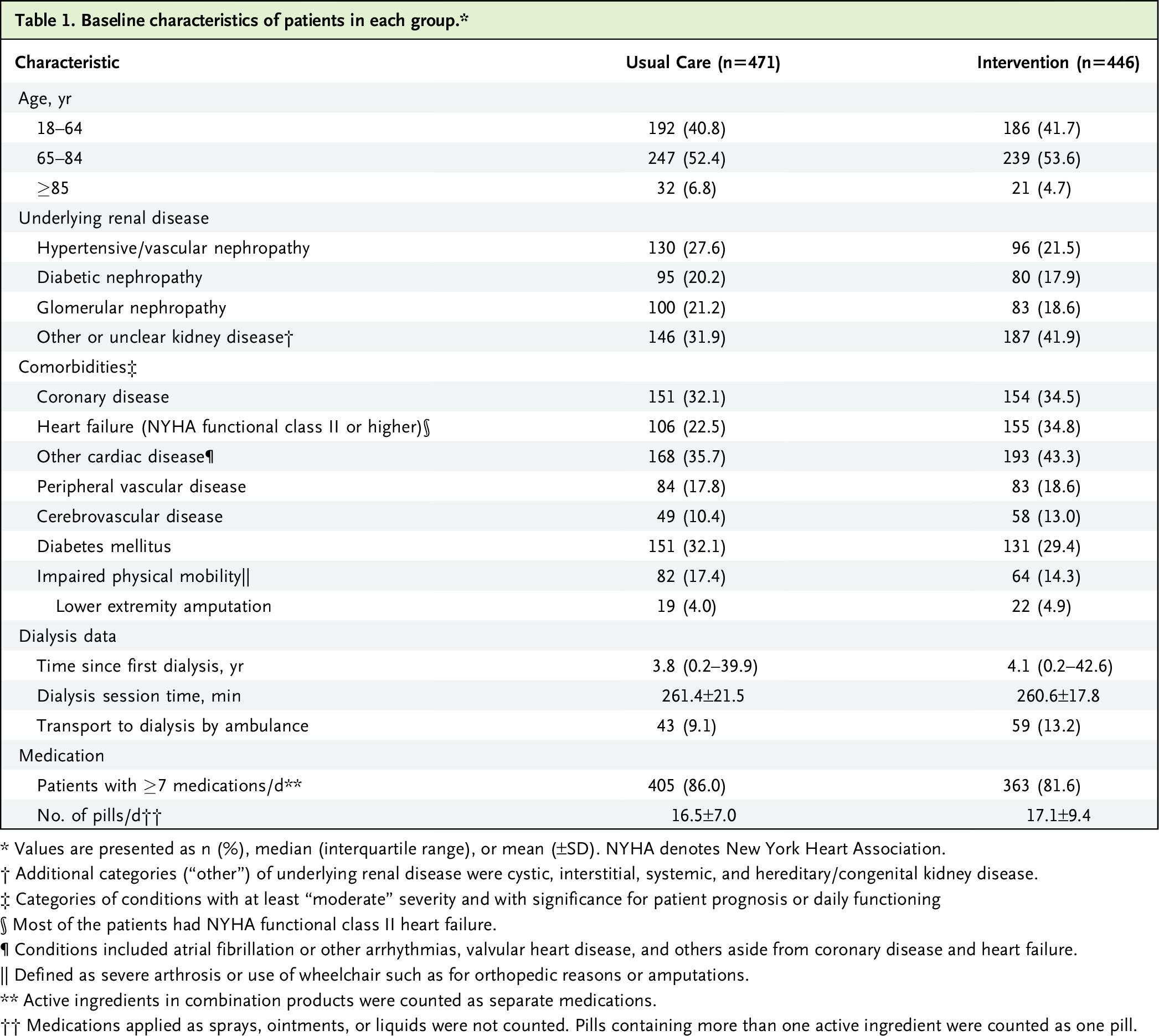
FDA 对 XPHOZAH 的批准基于一项全面的开发计划,包括在三项 3 期临床试验中对超过 1,000 名患者进行的不同人群进行评估,评估 XPHOZAH 作为单一疗法和与磷酸盐结合剂疗法联合治疗的有效性和安全性,所有这些都满足了主要和关键次要终点(PHREEDOM、BLOCK 和 AMPLIFY)。 三项临床试验的数据表明,XPHOZAH 显着降低接受维持性血液透析患者升高的血清磷水平。
腹泻是 43% 至 53% 的患者出现的唯一不良反应,在整个试验中,至少有 5% 接受 XPHOZAH 治疗的 CKD 透析患者报告了唯一的不良反应。 据报道,接受 XPHOZAH 治疗的患者中大多数腹泻事件的严重程度为轻度至中度,并随着时间的推移或剂量减少而得到缓解。 腹泻通常在开始后不久报告,但也可能在 XPHOZAH 治疗期间的任何时间发生。 在这些试验中,5% 的 XPHOZAH 治疗患者报告出现严重腹泻。
Ardelyx 还完成了两项开放标签临床试验(OPTIMIZE 和 NORMALIZE),以评估将 XPHOZAH 融入临床实践的不同选择。
XPHOZAH历经坎坷
Xphozah在FDA的批准之路上可谓也是经过了起起落落,也可以说是命途多舛。
但在2012年,阿斯利康与Ardelyx协议以 2.73 亿美元获得Xphozah的全球权益。就在阿斯利康接手Xphozah的第三年,Xphozah在一项3 期肾病糖尿病患者的 2a 期试验中,主要目标蛋白尿未达到终点。这也使阿斯利康准备放弃Xphozah。
正是由于Xphozah的3期研究失败,Ardelyx得以归还阿斯利康2500 万美元后重新收回Xphozah。而在Ardelyx的不屑努力下,Xphozah得以在2019年被批准用于治疗便秘型肠易激综合征。Ardelyx正以为看到了二起的希望,但没想到二落也随之而来。
就当Ardelyx以为Xphozah用于治疗降低接受肾透析治疗的慢性肾病(CKD)成人患者的血清磷水平也会顺利获得批准的时候,被FDA回复以“降幅小且临床意义不明确”为由打了回来。
什么叫做临床意义明确的结果呢?Ardelyx公司首席商务官Susan Rodriguez在10月18日早些时候的电话会议上说高磷酸盐血症的治疗指南,要求将磷酸盐水平降至 2.5 mg/dL 至 4.5 mg/dL 的正常范围。
但在 Xphozah 获批之前,只有磷酸盐结合剂这一类药物可用于降低磷酸盐水平。"Rodriguez说:尽管磷酸盐结合剂被广泛使用,但大多数患者仍无法持续维持或达到指导水平。
在Xphozah的三项Ⅲ期研究,PHREEDOM研究中,Xphozah(30mg)组患者的血清磷水平平均降低1.4mg/dL;在AMPLIFY研究中,Xphozah(30mg)组患者的血清磷水平平均降低0.84mg/dL;在BLOCK研究中,Xphozah组3mg、10mg和30mg剂量组患者的血清磷水平分别平均降低1.00mg/dL、1.02mg/dL和1.19mg/dL。
但FDA表示对以上研究结果均不满意,要求Ardelyx进行额外的临床试验以证明Xphozah对降低血清磷水平或CKD导致的高磷血症有效。
Ardelyx的第二次希望也破灭了。这一次打击使Ardelyx股价直接跌了74%,而当时Ardelyx账上只有1.718亿美元。因此Ardelyx不得不通过裁员65%以节省开支从而维持研究进展。
Ardelyx这时也处于三起的开端。在FDA表示对Xphozah的研究结果不满,并要求Ardelyx进行额外的临床试验进一步证明,Ardelyx表示不服,并给予上诉处理。
这一举动也为Xphozah带来了转机,2022年11月在召开的CRDAC会议上,对于成人透析患者高磷血症使用Xphozah单药治疗获专家组9:4投票支持,而Xphozah联合磷酸盐治疗则获得专家组10:2投票支持。专家组的支持也让投资者对Xphozah增加了大幅信心。
Ardelyx则带着这份信心在今年4月重新向FDA提交了Xphozah的上市申请,最终Xphozah获批!
早在2017年就获得Xphozah中国权益的复星医药也在今年7月向NMPA提交了其用于治疗CKD高磷血症的上市申请。Ardelyx公司的日本合作伙伴Kyowa Kirin公司于2023年9月也获得了MLHW的批准,从而为Ardelyx公司带来了3000万美元的里程碑付款。
随着FDA的批准申请通过之后,Ardelyx在另一份声明中表示已修订了与SLR Capital Partners (SLR)管理的投资关联公司签订的2022年债务融资协议,以获得额外的5000万美元,并可能进一步增加5000万美元,从而向商业化进一步迈进。
FDA对于Xphozah的批准,行业媒体及许多业内人都用了“终于”一词,想必大家都对于Xphozah的上市能够为肾透析患者带来受益而开心,解决了目前肾透析高磷酸血症患者无药可用的现状。
Xphozah在中国也将上市
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








签到学习
73
血清磷有效降低
83