复宏汉霖曲妥珠单抗生物类似物获欧盟批准上市
2020-07-29 网络 网络
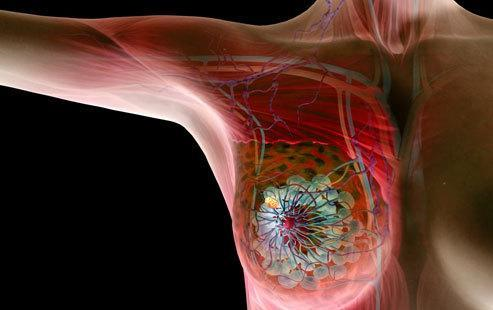
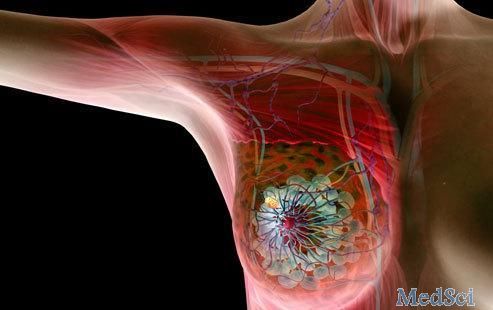
2020年7月29日,复宏汉霖公告称,其自主研发的生物类似药曲妥珠单抗HLX02在欧盟获批上市(商品名:Zercepac),用于治疗HER2阳性早期乳腺癌、HER2阳性转移性乳腺癌,以及未经治疗的HE
2020年7月29日,复宏汉霖公告称,其自主研发的生物类似药曲妥珠单抗HLX02在欧盟获批上市(商品名:Zercepac),用于治疗HER2阳性早期乳腺癌、HER2阳性转移性乳腺癌,以及未经治疗的HER2阳性转移性胃癌或胃/食管交界处腺癌。此次获批后,HLX02在所有欧盟成员国及冰岛、列支敦士登和挪威(各自为欧洲经济区(EEA)国家)获得集中上市许可。截止目前,HLX02是首个在欧盟获批上市的中国国产曲妥珠单抗。 Accord Healthcare S.L.U。(公司商务合作伙伴Accord Healthcare Limited的全资子公司)递交的 HLX02(注射用曲妥珠单抗,欧盟商品名:Zercepac)用于HER2阳性的早期乳腺癌、HER2阳性的转移性乳腺癌,以及未经治疗的HER2阳性的转移性胃癌或胃/食管交界处腺癌治疗的营销授权申请(Marketing Authorization Application, MAA)获欧盟委员会(European Commission, EC)批准。 此次获欧盟委员会(European Commission, EC)批准主要是基于对HLX02一系列研究数据的审查,包括质量对比研究、临床前研究及临床研究。这些数据都证明了HLX02与参照药(Herceptin,赫赛汀)在质量、安全性和有效性方面的高度相似。其中,比较HLX02与欧洲市售原研曲妥珠单抗的3期临床研究为一项国际多中心3期临床试验,设立了中国、菲律宾、波兰、乌克兰的89个研究中心,共入组了649例既往未接受治疗的HER2阳性复发性或转移性乳腺癌患者。研究结果进一步证实HLX02与欧洲市售原研曲妥珠单抗在疗效与安全性上无临床意义上的显著差异。 曲妥珠单抗是抗HER2单克隆抗体,原研药赫赛汀由罗氏公司(Roche)研发,自诞生以来,它已成为HER2阳性乳腺癌和胃癌一线治疗的基石。2019年4月,HLX02曲妥珠单抗在中国的上市申请已经被纳入优先审评程序,有望于近期在中国获批上市。 除了在中国的申报,复宏汉霖还对HLX02开展了前瞻性的国际化布局。公开信息显示,该公司陆续与Accord、Cipla、Mabxience和雅各臣药业等海外生物制药企业达成合作,促进HLX02在全球80多个国家和地区的商业化进程。 曲妥珠单抗原研是罗氏的赫赛汀,是一种重组 DNA 衍生的人源化单克隆抗体,可与人表皮生长因子受体 2 蛋白(HER-2)的细胞外结构域结合从而抑制肿瘤细胞生长,同时能够诱导抗体依赖型细胞毒作用(ADCC)杀伤肿瘤细胞。 目前,曲妥珠单抗已在国内获批多个适应症,包括 HER2 阳性的转移性乳腺癌,HER2 阳性的早期乳腺癌的辅助、新辅助治疗,HER2 阳性晚期胃癌以及超适应用药于 HER2 阳性非小细胞肺癌。
参考资料:
[1] HLX02(注射用曲妥珠单抗,欧盟商品名:Zercepac®)的营销授权申请(MAA)获欧盟委员会(EC)批准. 2020-07-29, from http://www.cninfo.com.cn/new/disclosure/detail?stockCode=02696&announcementId=1208098865&orgId=fzqy1031451&announcementTime=2020-07-29本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#曲妥珠#
85
#曲妥珠单抗生物类似物#
83
#复宏汉霖#
62
#欧盟批准#
78