Nature:减肥或许迎来新方法!王冬冬等人发现GDF15通过增加肌肉的能量消耗来促进体重减轻
2023-07-02 iMedicines iMedicines 发表于上海
该研究发现除了抑制食欲外,GDF15还抵消了能量消耗的代偿性降低。
限制热量摄入以促进体重减轻是治疗非酒精性脂肪肝和改善Ⅱ型糖尿病患者胰岛素敏感性的有效策略。尽管其有效性,但在大多数人中,体重减轻通常无法长期保持,部分原因是生理适应会抑制能量消耗,这一过程被称为适应性热能产生,然而其机制尚不清楚。
2023年6月28日,麦克马斯特大学Gregory R. Steinberg团队(王冬冬为第一作者)在Nature 在线发表题为“GDF15 promotes weight loss by enhancing energy expenditure in muscle”的研究论文,该研究发现除了抑制食欲外,GDF15还抵消了能量消耗的代偿性降低,导致与单纯热量限制相比更大的体重减轻和非酒精性脂肪肝 (NAFLD) 的减少。
GDF15通过GFRAL-β-肾上腺素能依赖的信号通路,在小鼠骨骼肌中增加脂肪酸氧化和钙离子无效循环,从而维持能量消耗。这些数据表明,治疗性地靶向GDF15-GFRAL通路可能有助于在热量限制期间维持骨骼肌中的能量消耗。

GDF15在肝脏和肾脏中高度表达,并在所有细胞类型中作为线粒体毒素和内质网应激的应答而诱导表达。最初GDF15被发现是由巨噬细胞和癌细胞分泌的可溶性因子,后来证明其能引起消瘦,并保护小鼠免受肥胖和胰岛素抵抗的影响。在接受高脂饮食的啮齿动物中,重组GDF15的治疗可导致体重减轻、减少肝脏脂肪变性,并改善血糖控制。这种减重效应已被证明需要脑干,更具体地说,需要GDF15受体GFRAL。
在短期实验(7-10天)中,通过对照组进行配对喂养的小鼠实验证明,GDF15引起的体重减轻是由于食物摄入的减少。重要的是,通过遗传方式缺乏Gdf15的小鼠、靶向肝脏的Gdf15缺失小鼠以及通过遗传方式缺乏Gfral的小鼠,在接受高脂饮食时,食物摄入和脂肪堆积均略有增加,这支持了这一通路在调节能量平衡中的生理作用。
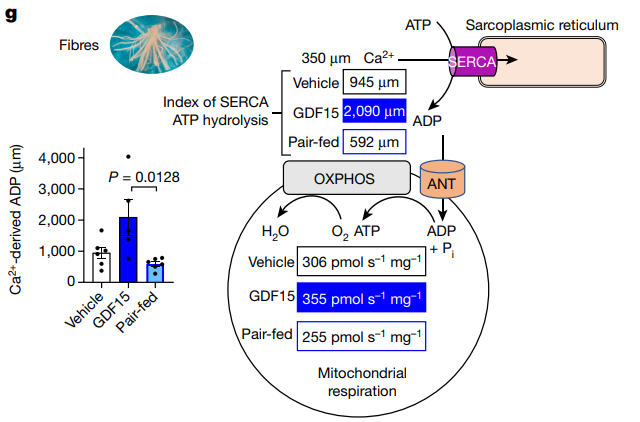
机理模式图(图源自Nature )
这些研究已经提出了GDF15通过GFRAL信号通路减轻体重和改善血糖控制的概念,主要是通过抑制食欲而对能量消耗几乎没有影响。然而,需要考虑以下三个重要区别,才能得出这是唯一导致减重的机制的结论:首先,能量摄入、能量消耗和体重是相互依赖的变量,它们之间动态相关,即能量摄入减少和体重减轻都可能导致能量消耗减少。其次,通过对Gfral缺失小鼠使用重组GDF15的研究,实验时间相对较短(7-10天),这可能不足以检测到与能量消耗减少(即适应性热能生成)相关的反向调节响应,而这种反应通常在较长时间的热量限制后在啮齿动物中发生。最后,现在已经认识到,在室温(21°C)下饲养的小鼠中进行能量平衡实验会刺激交感神经驱动,这可能抑制通过β肾上腺素能信号通路诱导的产生无效循环或刺激能量消耗的药物引起的体重减轻。
在这项研究中,通过对小鼠进行精心控制和延长的配对喂养实验,作者发现了GDF15和GFRAL与β肾上腺素能受体和骨骼肌钙循环之间的生物学回路。与热量限制的配对喂养对照组相比,GDF15处理的小鼠能够保持能量消耗,这与骨骼肌去甲肾上腺素、脂肪酸氧化、氧耗和钙循环的增加有关。总之,该研究表明,鉴于GDF15在针对肌肉热产生方面的独特作用,这些发现可能解释了与肠促胰岛素类治疗联合使用时观察到的增强减重效果。
原文链接:https://doi.org/10.1038/s41586-023-06249-4
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













