Toripalimab联合化学疗法一线治疗鼻咽癌,中国国家药品监督管理局已批准其补充性新药申请
2021-02-20 Allan MedSci原创
中国国家药品监督管理局(NMPA)已接受Toripalimab联合化疗一线治疗复发性或转移性鼻咽癌的补充性新药申请。
鼻咽癌是一种发生于鼻咽腔或上咽喉部的癌症。在世界的某些地区,例如东南亚和非洲,患此病的人比其他地方多,过去认为是主要是膳食的影响,目前倾向为遗传基因为主要的影响因素。
中国制药公司君实生物近日宣布,中国国家药品监督管理局(NMPA)已接受Toripalimab联合化疗一线治疗复发性或转移性鼻咽癌的补充性新药申请。
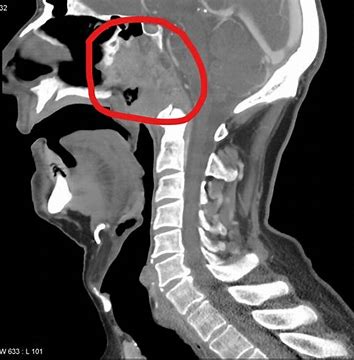
这项批准是基于JUPITER-02研究(NCT03581786)的最新结果,该研究是一项随机、双盲、安慰剂对照的III期研究。研究结果表明,与标准的吉西他滨/顺铂一线疗法相比,Toripalimab单抗联合吉西他滨/顺铂一线治疗复发或转移性鼻咽癌患者时,显著延长了患者的无进展生存期(PFS)。
先前,Toripalimab已从美国FDA获得了治疗鼻咽癌的“突破性疗法称号”和“孤儿药称号”,君实生物也将在美国提交生物制剂许可申请(BLA)。Toripalimab可能会成为首个在海外市场实现商业化的中国抗PD-1单克隆抗体。
原始出处:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#监督#
67
#新药申请#
86
#化学疗法#
72
学习了
79
Toripalimab #特瑞普利单抗#
137
#补充性新药申请#
64
#mAb#
65
学习了,谢谢分享
0
#国家药品监督管理局#
74
已读,受益匪浅
101