等待15年的突破!双特异性抗体革新眼科anti-VEGF疗法,每4个月注射1次
2021-02-18 医药魔方 医药魔方
年龄相关性黄斑变性(AMD)是一种会影响到人们需要清晰中央视力的日常活动(比如阅读)的眼部疾病,该疾病进展到晚期则称为新生血管性年龄相关性黄斑变性(nAMD),或者叫做湿性年龄相关性黄斑变性(wAMD
年龄相关性黄斑变性(AMD)是一种会影响到人们需要清晰中央视力的日常活动(比如阅读)的眼部疾病,该疾病进展到晚期则称为新生血管性年龄相关性黄斑变性(nAMD),或者叫做湿性年龄相关性黄斑变性(wAMD),病理表现为新生和异常的血管在黄斑下不受控制地生长,导致肿胀、出血和/或纤维化,造成快速和严重的视力丧失。
新生血管性年龄相关性黄斑变性(nAMD)
nAMD是60岁以上人群失明的主要原因,在美国大约有110万例nAMD患者。随着人口老龄化加速,预计在全球和美国都还会影响到更多的人群。当前临床上针对nAMD的标准疗法是眼球玻璃体内注射血管内皮生长因子(VEGF)抑制剂。
尽管anti-VEGF疗法已大大降低了nAMD引起的视力丧失风险,但是这种疗法的局限性也很明显,一方面,眼球注射给药需要在医院由医生操作,频繁注射会有较重的治疗负担,而且患者每次注射不仅要克服恐惧心理,同时面临感染风险,以上会导致现实世界治疗不足的问题,造成患者视力结局不理想;另一方面,anti-VEGF疗法可以有效抑制新生血管,但是对导致nAMD的炎症的减轻作用有限。因此nAMD患者迫切需要更为有效、作用更为持久的新疗法。
制药公司在nAMD新疗法的开发上首先考虑到的便是降低注射频率。比如从雷珠单抗到阿柏西普(VEGFR-Fc融合蛋白),由于后者可以结合VEGF-A的所有亚型,亲和力可以到达雷珠单抗的100倍,能够长期维持眼内的anti-VEGF活性,给药频率可以做到每2个月1次(前3个月每月1次),目前是nAMD的标准疗法,2020年销售额达到79.09亿美元。
诺华开发的Beovu(brolucizumab)在2019年10月8日迎来了FDA的批准,Brolucizumab移植了一个anti-VEGF-A抗体的互补决定区,是一个单链抗体片段(scFv)。由于scFv是最小的抗体功能单元,相比于大分子可以实现更高摩尔剂量给药,并且组织穿透力更强。而解剖学也证实了Brolucizumab的低分子量和高浓度梯度可以增加病变部位的药物分布,能够更有效地控制病变,成为首个治疗nAMD只需要每3个月注射1次的anti-VEGF疗法,2020年全球销售额为1.90亿美元。
毫无疑问,Beovu是nAMD临床治疗的重大突破,将注射频率从每年6次降低为每年4次可以极大减轻患者的治疗负担,但是从治疗策略和药物作用机制上看,anti-VEGF疗法作为nAMD的标准手段已经有15年没有更新了。这一局面将会被罗氏的双特异性抗体药物faricimab(RG7716)打破。
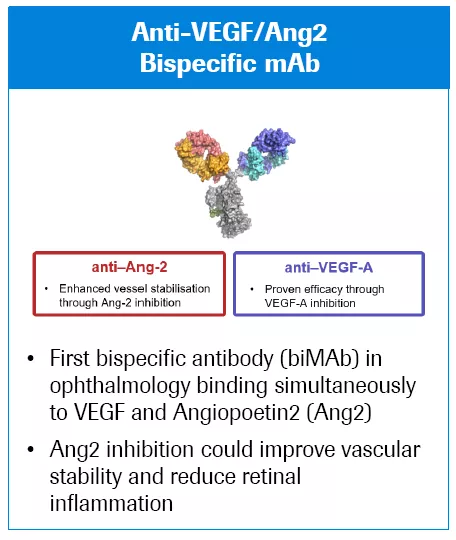
Faricimab是首个针对眼科疾病开发的双特异性抗体,目前进展至III期阶段,为全球最快。Faricimab同时靶向作用于血管内皮生长因子A(VEGF-A)和血管生成素2(Ang-2)这两条不同的信号通路。从生物学机制上看,VEGF-A和Ang-2信号会使血管不稳定,诱导形成新生血管和促进炎症。Faricimab在阻断VEGF/VEGFR信号有效控制新生血管形成的同时,也能抑制Ang-2信号来改善血管稳定性和减轻视网膜炎症,与单纯anti-VEGF疗法相比,用于治疗多种视网膜疾病就可以实现减少眼部注射给药频率,改善患者的远期视力结局。
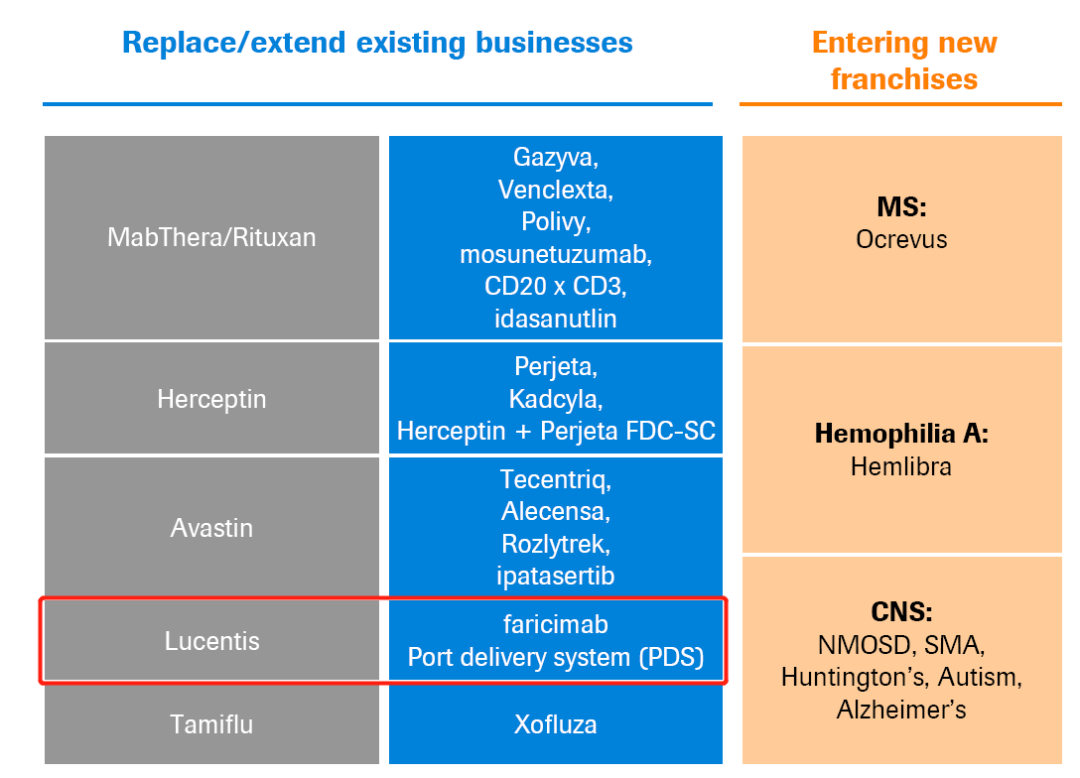
罗氏将faricimab视为未来取代Lucentis的项目,目前在同步开发faricimab治疗nAMD、糖尿病性黄斑水肿(DME)、视网膜静脉阻塞继发黄斑水肿的适应证,均已进展至III期阶段,对标的也是临床标准疗法阿柏西普。
针对nAMD适应证,罗氏开展了代号为TENAYA (NCT03823287) 和LUCERNE (NCT03823300)的两项III期研究。这两项全球多中心、随机、双盲III期研究采用相同的试验设计,分别在671例和658例nAMD患者中评估faricimab和阿柏西普的疗效和安全性差异。
研究均设置faricimab 6mg(每2个月、3个月或者4个月1次,根据第20周和第24周疾病活动程度评估确定)和阿柏西普2mg(每2个月1次)两个给药组。研究的主要终点是第48周最佳矫正视力(BCVA)评分较基线的平均变化,次要终点包括安全性,faricimab 组每2个月、3个月或4个月1次的受试者比例,BCVA评分较基线增高和避免降低15个字母以上受试者比例,黄斑中心区视网膜厚度较基线的变化。
2月12日,罗氏在血管生成、渗出和变性2021年研讨会召开前夕公布了上述两项III期研究的详细数据。结果显示,faricimab在治疗第48周的视觉敏锐度(BCVA评分)较基线的改善程度均不劣于阿柏西普,在TENAYA研究和LUCERNE研究中分别改善5.8和6.6个字母,而阿柏西普组为5.1和6.6个字母,到达了主要终点。
TENAYA研究中,faricimab治疗组nAMD患者在第1年时能够实现每4个月1次给药的比例为45.7%(144/315),每3个月1次给药的比例为34%(107/315);LUCERNE研究中,faricimab治疗组在第1年时能够实现每4个月1次给药的比例为44.9%(142/316),每3个月1次给药的比例为32.9%(104/316)。相当于接受faricimab治疗的患者近80%在1年时能够实现每3个月或更长时间间隔的注射给药。此外,每4个月1次faricimab在黄斑中心区视网膜厚度降低方面也不劣于每2个月注射1次阿柏西普。
糖尿病性黄斑水肿(DME)是另一种威胁视力的眼科疾病,faricimab同样在两项III期研究中取得了不劣于阿柏西普的结果。
糖尿病性黄斑水肿(DME)
DME是糖尿病性视网膜病变(DR)的一种并发症。糖尿病患者因为血糖过高,对眼部血管造成损伤,会导致血液和/或体液渗入视网膜,就会造成糖尿病性视网膜病变(DR)的发生,表现视网膜部分区域的肿胀和血液供给阻断。如果如果血管损伤和渗漏发生在视网膜的中央区域,就会引起黄斑水肿,即糖尿病性黄斑水肿。DME如果不加以干预治疗,会严重威胁到视力,影响生活质量。目前全球大约有2100万DME患者,美国大约有75万患者。随着糖尿病患者人数的增加,DME患者的数量预计还会增加,也需要anti-VEGF之外更加有效、更加长效的治疗方案。
针对DME适应证,罗氏开展了代号为YOSEMITE (NCT03622580) 和RHINE (NCT03622593)的两项III期研究。这两项全球多中心、随机、双盲III期研究采用相同的试验设计,分别在940例和951例DME患者中评估faricimab和阿柏西普的疗效和安全性差异。
研究均设置3个给药组,分别是faricimab 6mg(个体化给药间隔,最长4个月,根据疾病严重程度确定)、faricimab 6mg(每2个月1次)和阿柏西普2mg(每2个月1次)。研究的主要终点是第52周最佳矫正视力(BCVA)评分较基线的平均变化,次要终点包括安全性,faricimab 个体化给药间隔组组第52周时实现每1个月、2个月、3个月或4个月1次的受试者比例,第52周时糖尿病视网膜疾病严重程度较基线改善2个等级以上的受试者比例,BCVA评分较基线增高和避免降低15个字母以上受试者比例,黄斑中心区视网膜厚度较基线的变化。
结果显示,faricimab 6mg个体化给药间隔组、faricimab 6mg每2个月1次组DME患者的视觉敏锐度(BCVA评分)改善均不劣于阿柏西普每2个月1次。在YOSEMITE研究中,三组的视力敏锐度较基线分别平均增加11.6,10.7和10.9个字母,在RHINE研究中则分别平均增加10.8,11.8和10.3个字母。
YOSEMITE研究中,faricimab个体化给药间隔组DME患者在第1年时能够实现每4个月1次给药的比例为52.8%(151/286),每3个月1次给药的比例为21%(60/286);RHINE研究中,faricimab个体化给药间隔组DME患者在第1年时能够实现每4个月1次给药的比例为51%(157/308),每3个月1次给药的比例为20.1% (62/308);相当于接受faricimab个体化间隔给药的DME患者超过70%能够在治疗1年时实现每3个月或更长时间间隔的注射给药。
Faricimab是首个在治疗DME和nAMD的III期研究中达到4个月间隔给药的药物,而且具有良好的耐受性,没有任何新发或预期之外的安全性事件。罗氏计划2021年向全球药监机构同时提交faricimab针对这两项适应证的上市申请。如果获批, faricimab将是15年来nAMD患者的首个新疗法,也将是DME患者近10年来的首个新疗法,这绝对会是激动人心的一个时刻。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













双特异性抗体是热点,但是也不一定都有效!
79
目前进展如何
85
新的研究突破!
79
#特异性#
66
#VEGF#
104
#特异性抗体#
56