闪耀ESMO!礼来阿贝西利(abemaciclib)显著降低HR+,HER2-高危早期乳腺癌患者复发风险达25%
2020-09-22 医药魔方 医药魔方
9月20日,礼来制药宣布,阿贝西利(abemaciclib)联合标准辅助内分泌治疗(ET)用于激素受体阳性(HR+)、人表皮生长因子受体2阴性(HER2-)的高危早期乳腺癌患者,较单独使用标准辅助ET
9月20日,礼来制药宣布,阿贝西利(abemaciclib)联合标准辅助内分泌治疗(ET)用于激素受体阳性(HR+)、人表皮生长因子受体2阴性(HER2-)的高危早期乳腺癌患者,较单独使用标准辅助ET显着降低了乳腺癌复发风险25%(HR:0.747;95% CI:0.598,0.932;p = 0.0096)。在所有预设的亚组中,患者均一致显示出具有统计学意义的获益,治疗2年后组间差异为3.5%(阿贝西利组为92.2%,对照组为88.7%)。这些结果来自预设的期中分析,在两组的意向治疗人群中观察到323例IDFS事件,阿贝西利组为136例,对照组为187例。该研究结果已于9月20日(欧洲时间)在2020年欧洲肿瘤内科学会(ESMO)线上年会的主席研讨会上发布,并同期在《临床肿瘤学杂志》(JCO)刊发。
monarchE研究的安全性数据与阿贝西利既往研究的安全性特征一致,并未观察到新的安全性信号。在进行分析时,每组中约有70%的患者仍处于2年阿贝西利治疗期内。两组患者的中位随访时间约为15.5个月。阿贝西利的中位治疗时间为14个月。
英国皇家马斯登医院的乳腺肿瘤学教授及肿瘤内科顾问医生、monarchE研究的主要研究者Stephen Johnston博士表示:“对于高危HR+,HER2-早期乳腺癌患者来说,这是一个重要的里程碑。它可能是过去二十年来针对此类乳腺癌患者最显着的治疗进展之一。阿贝西利联合标准辅助内分泌治疗可以显着改善具有高复发风险的HR+,HER2-早期男性和女性乳腺癌患者的无浸润性疾病生存期。如果获得批准,它将成为此类患者的全新标准疗法。”
monarchE研究从38个国家的600多个中心随机入组了5,637例HR+, HER2-高危早期乳腺癌患者。高危的定义为:淋巴结转移、原发肿瘤瘤体大或细胞增殖程度高(由肿瘤分级或Ki-67指数确定)。患者接受2年阿贝西利治疗(治疗期),或者直到满足停药标准为止。治疗期过后,所有患者将根据临床指征继续接受共5-10年的内分泌治疗。
礼来制药肿瘤事业部副总裁、产品后期开发负责人Maura Dickler博士表示:“我们很高兴阿贝西利被证明能够具有临床意义地降低HR+, HER2-高危早期乳腺癌患者复发风险。礼来要感谢全球各地参与这项临床研究的患者和研究人员。阿贝西利显着改善无浸润性疾病生存期的这一研究结果非常重要,这为具有复发风险的高危早期乳腺癌患者带来了希望。礼来将尽快将这些结果提交到各国的药品监管机构。我们期待能够为这些患者提供阿贝西利这一新的治疗选择。monarchE研究结果进一步夯实了阿贝西利既往已获得的充分的临床证据,我们对此感到非常自豪。”
阿贝西利联合辅助内分泌治疗亦改善了患者的无远处复发生存期,即延缓了癌症扩散到身体其他部位的时间。阿贝西利联合内分泌治疗降低了28%的转移风险(HR:0.717;95%CI:0.559,0.920),其中肝转移和骨转移的发生率降幅最大。所有预设的亚组中,患者均显示出一致的治疗获益。阿贝西利组患者的2年无远处复发生存率为93.6%,而对照组为90.3%。
致力于关怀和支持乳腺癌患者群体的非盈利机构“Living Beyond Breast Cancer”的首席执行官Jean Sachs表示:“monarchE的研究结果对我们的乳腺癌患者群体而言,是激动人心的好消息。高达30%的HR+早期乳腺癌患者可能会出现复发。因此,对HR+, HER2-高危早期乳腺癌患者来讲,这是一个令人振奋的进展,尤其是因为这项研究的患者包括处于绝经前或绝经后的所有女性患者以及男性患者 。”
总生存期结果尚不成熟,monarchE研究将继续开展直至研究完成(预计为2027年6月)。期中分析中IDFS的显着获益是确证性的。所有参与monarchE研究的患者都将继续被随访至完成主要分析及完成评估总生存期和其它研究终点。礼来将于2020年底前向监管机构递交monarchE研究的研究结果。
关于monarchE 研究
monarchE是一项随机、开放标签的多中心III期临床研究,共入组5,637例淋巴结阳性的HR+、HER2-高危早期乳腺癌患者。受试者按1:1的比例被随机分配至阿贝西利(150 mg,每日两次)联合标准辅助内分泌治疗组,或单纯标准辅助内分泌治疗组。患者接受2年的治疗(即治疗期),或者直到满足停药标准为止。治疗期过后,所有患者将根据临床指征继续接受共5-10年的辅助内分泌治疗。研究的主要研究终点为基于“疗效终点标准定义“(STEEP)标准的无浸润性疾病生存期(IDFS)。在乳腺癌的辅助治疗研究中,该指标的定义为至癌症复发、新发癌症或死亡的时间。次要研究终点包括:无远处复发生存期、总生存期、安全性、药代动力学和健康结局。
高危被明确定义为:HR+, HER2-早期浸润性乳腺癌的女性(包括绝经前和绝经后)和男性患者,病理腋窝淋巴结(ALN)阳性≥4个,或阳性腋窝淋巴结数为1至3个且至少具有以下一种高风险特征:原发性浸润性肿瘤≥5cm;肿瘤组织学分级3级;或中心实验室检测的Ki-67指数≥20%。患者在入组前还需已完成辅助化疗和放疗(如适用),并已从治疗的所有急性副反应中恢复。
关于早期乳腺癌
乳腺癌是全球女性中最高发的癌症1。据估计,90%的乳腺癌确诊在早期2。其中最常见的亚型为HR+, HER2-型,约占乳腺癌患者总数的70%3。即使在这个亚型内,HR+, HER2-乳腺癌也呈现出其复杂性。许多因素,诸如癌症的淋巴结转移及其生物学特性,都可以影响该病的复发风险。在确诊HR+, HER2-早期乳腺癌的人群中,约30%的患者存在癌症复发乃至进展为不可治愈的转移癌的风险4。
关于阿贝西利(abemaciclib)
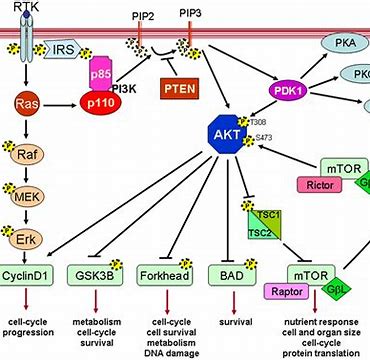
阿贝西利(abemaciclib)是一种细胞周期蛋白依赖性激酶(CDK)4和6的抑制剂。在雌激素受体阳性(ER+)的乳腺癌细胞系中,CDK4和6通过与细胞周期蛋白D1结合而活化,促进视网膜母细胞瘤蛋白(Rb)磷酸化,从而推动细胞周期进程和加速细胞增殖。
在体外,阿贝西利的连续暴露会抑制Rb磷酸化,并阻断细胞周期从G1期向S期的进展,从而导致细胞衰老和凋亡(细胞死亡)。临床前研究中,不间断地每天采用阿贝西利治疗使肿瘤显着缩小。在健康细胞中抑制CDK4和6可能会引起副作用,某些副作用甚至较严重。临床证据还表明,阿贝西利可穿越血脑屏障。以晚期癌症患者(包括乳腺癌)为对象的研究显示,脑脊液中阿贝西利及其活性代谢产物(M2和M20)的浓度与未结合的血浆浓度相当。
阿贝西利是礼来的首个固体口服药物,采用更快、更高效的“连续生产”模式进行生产。“连续生产”是制药行业中的一种先进的新型生产模式,而礼来是最早使用该技术的公司之一。
注:1. 相关产品或适应症尚未获批
2. 礼来不推荐任何未获批的药品/适应症使用
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#SMO#
62
#HER2-#
65
#MAC#
52
#复发风险#
66
#ESMO#
63
#EMA#
63
#乳腺癌患者#
53
不要太贵就更好了
122