【Haematologica】多发性骨髓瘤MRD评估的五个挑战
2024-02-17 聊聊血液 聊聊血液 发表于陕西省
《Haematologica》近日发表综述,阐述了MRD评估的不同方法及其在多发性骨髓瘤治疗中的作用,重点阐述了临床实践中五个已解决和未解决的挑战。
MM的MRD评估
多发性骨髓瘤(MM)是一种异质性疾病,具有多种分子亚型和不同的预后。随着包括单克隆抗体、双特异性T细胞衔接器和嵌合抗原受体T细胞(CAR-T细胞)在内的高效治疗方法的出现,大多数MM患者获得了长期生存,但该疾病仍无法治愈,部分高危患者会出现早期复发且生存期较短。新型和高灵敏度方法可以在治疗期间或治疗后检测微小残留病(MRD),且MRD阴性是强有力的独立预后因素。虽然目前MRD评估已在临床试验中得到验证,但其在临床实践中的应用尚未建立,对指导治疗的潜在影响也仍在深入评估。《Haematologica》近日发表综述,阐述了MRD评估的不同方法及其在多发性骨髓瘤治疗中的作用,重点阐述了临床实践中五个已解决和未解决的挑战。

不同MRD评估手段
MRD评估包括基于骨髓和基于外周血的手段,前者包括多色流式细胞术(MFC)、二代流式细胞术(NGF)和二代基因测序(NGS),NGF的灵敏度可达10-5-10-6且不需要诊断时样本, NGS需要诊断时骨髓样本,灵敏度可达10-6,MRD阴性与良好预后相关。骨髓MRD的评估需要重复的有创操作,并且受限于MM的斑片性质和MM固有的髓外病变的可能性,替代评估方法包括基于血液或影像学的MRD评估。
基于血液的MRD评估包括循环浆细胞(PCP,但灵敏度不如骨髓)、循环游离DNA(cfDNA,也称液体活检,与骨髓结果高度一致,但低水平的循环肿瘤DNA是重大挑战,且目前的大多数方法不够敏感)、单细胞RNA测序(可在单细胞水平进行转录组分析,并检测罕见的恶性肿瘤细胞。但可及性低、流程相对复杂、可重复性低、成本高,此外评估的数量细胞远远少于流式或NGS,可能出现假阴性)和质谱(MS,可检测浓度远低于标准血清免疫固定电泳的单克隆免疫球蛋白,还可区分治疗性单克隆抗体和骨髓瘤单克隆免疫球蛋白,及识别与有临床意义的单克隆免疫球蛋白病尤其是AL型淀粉样变性患者相关的翻译后修饰。是PFS的强预测因子,但需要更多的研究才能将其纳入临床实践。此外存在假阳性)。
全身影像学评估手段包括PET/CT和MRI,可识别骨病灶和髓外病变,对基于骨髓的MRD评估具有重要的补充作用。
MRD评估的重要挑战
随着MRD数据量的不断增加、检测方法的可获得性、可重复性和标准化,MRD的评估已成为临床试验中重要且经过验证的标准。目前MRD评估被用于患者选择、风险分层或试验人群富集,以及作为终点。此外MRD评估可能有助于加快药物开发。然而,使用MRD评估来指导治疗和将MRD纳入临床实践尚未经过验证。下面是五个已经解决或需要解决的重要挑战。
1.应该使用哪种MRD评估手段?
使用基于骨髓的方法进行MRD评估仍是金标准,而可用性、成本、预后功效和一致性是需要考虑的重要因素。关于基于骨髓的MRD评估,NFC和NGS都是MM的强预后标志物。表1总结了其特点。
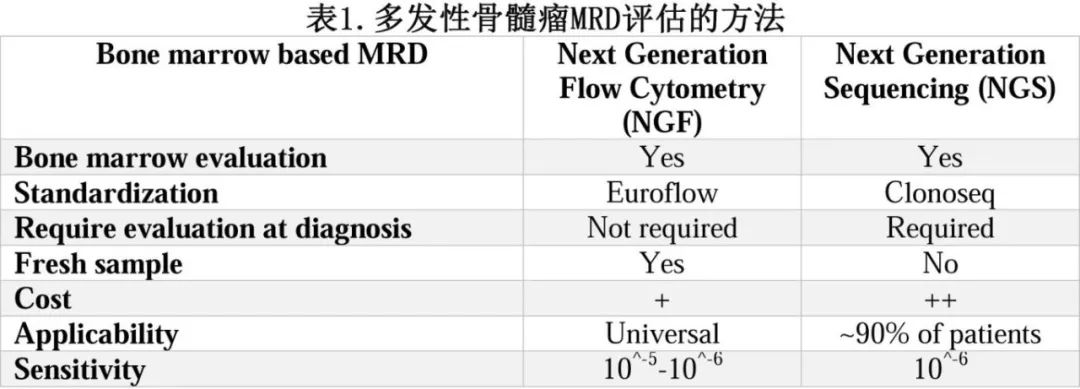
流式细胞术和NGS已在随机临床试验中进行比较。在2期多中心随机FORTE试验≥CR患者中,灵敏度为10-5时与MRD的相关性为86%。在3期CASSIOPEIA试验中,MFC和NGS的一致性为83.5%,灵敏度为10-5。一项106例患者的研究直接对比了NGF和NGS(但并非clonoseq平台),显示出高度的相关性(R2=0.905)。
由于NGS和NGF具有可比性,应根据当地的可用性来考虑。评估骨和髓外MRD的互补影像学方法包括全身MRI和PET/CT,可提供额外的信息。基于骨髓和的方法具有相对较好的一致性,尤其在髓外病变和高危MM方面可提供额外的信息,因此,对于高危或髓外病变患者,全身影像学应与基于骨髓的MRD联合使用。表2总结了全身影像学方法的特点有报告支持在患者治疗中联合使用两种MRD方法的获益。
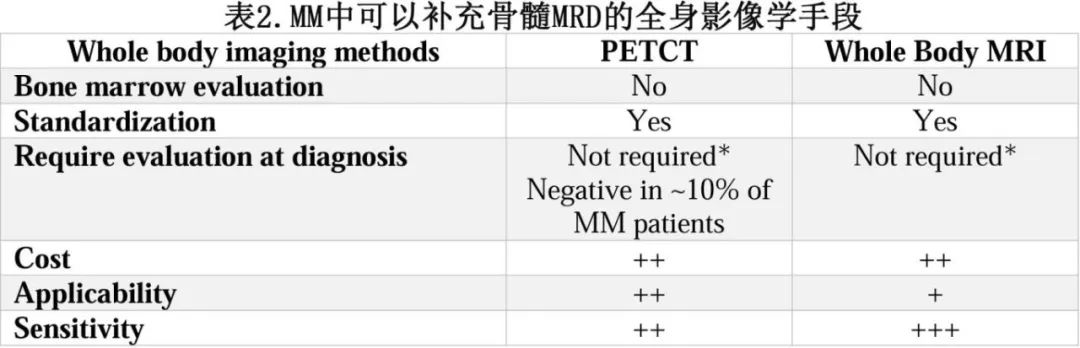
2.何时进行MRD评估?
MRD利用方面的另一个重要挑战在于其时间轴。第一个问题在于MRD评估应在一线治疗的早期(例如SCT之前)还是稍后、巩固治疗后或维持治疗期间进行。数项试验评估了这些时间点中的每一个,而且由于MRD的动态特性(意味着从MRD阳性转为阴性或阴性转为阳性),因此多次评估可提供更多信息。这些研究还定义了“持续”MRD阴性的概念,似乎是MM的关键预后因素,但又产生了新的重要问题,即两个时间点之间相隔多久。似乎较长的时间点可能与较好的结局相关,目前有研究正在探讨6个月、1年或2年的MRD阴性是否与可能更多的影响治疗决策,但还需要大型3期临床试验来解决这一问题。在未来的临床实践中,对于新诊断的骨髓瘤和复发/难治性骨髓瘤,巩固治疗前、后或维持治疗期间,MRD评估可能有助于评估特定治疗策略的疗效。然而包括双特异性抗体和CAR-T细胞疗法在内的细胞疗法的出现彻底改变了患者结局,并且与MRD和血清学残留病的动态模式(此外通常是分离模式)相关。因此,在这些新型疗法的背景下,MRD评估的作用仍有待充分验证。
3.高危MM中MRD评估的价值如何?
一线治疗后早期复发的MM患者预后最差,改善这一亚组患者治疗策略的重要研究正在进行中,其中关于MRD状态对高危患者临床影响,相关报道结果有差异。虽然MRD阴性与高危MM的临床改善相关,但并不能克服其不良预后,高危 MM仍可能出现早期进展。此外,大型3期试验(Myeloma XI)的数据表明,即使对于达到MRD阴性状态的患者,高危分子学特征仍可对PFS和OS产生不利影响。此外正如前文提到的斑片状病变和髓外病变,仅骨髓MRD评估可能不足以完全评估MRD。事实上,在一项比较骨髓和基于影像学的MRD评估的研究中,通过流式细胞术达到骨髓MRD阴性的患者中,有12%的PET/CT或全身扩散加权MRI (WB-DWI-MRI)阳性,并且与骨髓和影像学MRD均阴性的患者相比PFS更短。还需要更多的数据来更好地解读和使用MRD状态,尤其是在高危患者和EMD患者中。持续性MRD,以及骨髓联合影像学(PET/CT或全身MRI)的MRD评估都是需要考虑的重要参数,也是HR MM患者最有价值。随机试验的结果有望解答这一重要问题。
同样,在复发/难治性MM患者中,虽然MRD阴性与较好的预后相关,但大多数患者会出现复发。评估Idecabtagene vicleucel (ide-cel)治疗复发性和难治性骨髓瘤患者疗效和安全性的KarMMa试验充分说明了这一点,例如,在该试验中,26%的患者达到MRD阴性,包括79%达到CR的患者。但在20个月随访时,≥CR患者中只有40%仍处于缓解状态。在这种情况下,MRD持续阴性联合全身影像学似乎更有意义。
4.是否仅完全血液学缓解患者进行MRD评估?
哪些患者应评估MRD?在临床试验中,MRD研究在达到CR或严格CR的MM患者中进行,或者在特定治疗方案的特定时间点(如干细胞移植前,维持治疗前或期间)进行。MRD阳性CR的患者预后明显差于MRD阴性且CR的患者。然而也有多项研究报告了达到非常好的部分缓解(VGPR)的MM患者的MRD阴性率,事实上,在通过流式细胞术或NGS评估达到MRD阴性的患者中,高达25%的患者为免疫固定电泳持续阳性,因此归类为VGPR。重要的是,免疫固定电泳阳性和MRD阴性患者的预后与免疫固定电泳阴性和MRD阴性患者相似。免疫固定电泳阳性与MRD阴性之间的差异可能与髓外病变、骨髓标本无法代表全骨髓或单克隆免疫球蛋白半衰期长等原因有关,且在使用质谱的研究中更加突出。在一项研究中,在ASCT后100天后达到常规定义的CR且骨髓NGF-MRD阴性的患者中,69%的患者仍可通过MALDI-TOF质谱检测到单克隆免疫球蛋白。最后,CAR - T细胞治疗后经常观察到不一致的MRD和免疫固定电泳结果,在达到MRD阴性的患者中CR率低,特别是在治疗后的前6个月,表明MRD评估(反映骨髓中骨髓瘤细胞清除)可能是这种情况下的独立预后标志物。因此,在获得≥VGPR的患者中评估MRD具有重要意义。
5.MRD评估是否应影响治疗决策?
MRD阴性是非常强的预后标志物,但其对治疗决策的影响仍有待确定,为解决这一问题,目前有几项随机临床试验正在进行中(表3)。
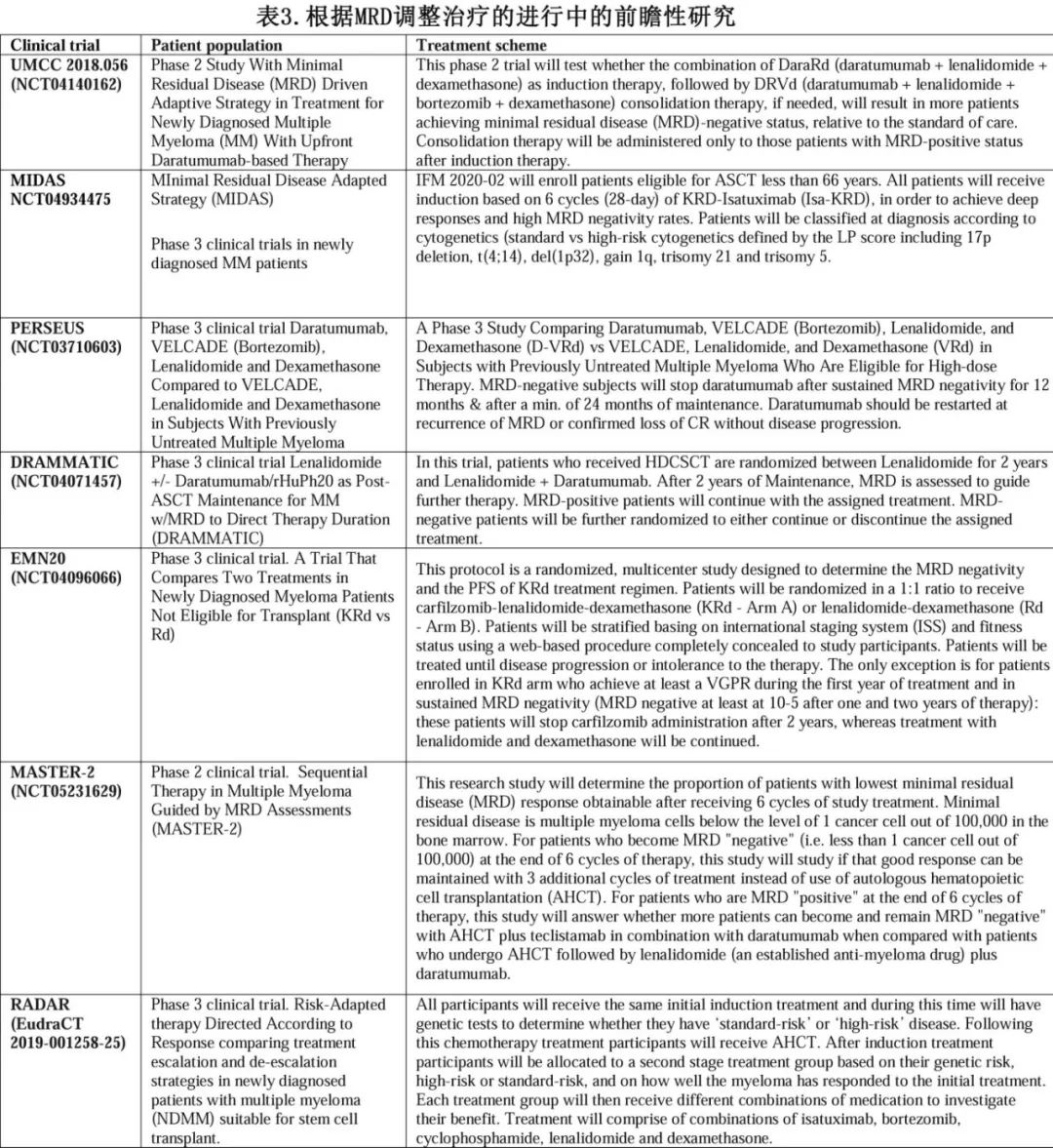
这些研究的目标是确定是否应根据MRD状态调整治疗:在MRD阳性时加强治疗,在MRD持续阴性时停止维持治疗,在MRD状态从阴性转为阳性时改变治疗。MASTER试验开创了这一策略,并评估了基于骨髓的MRD在巩固治疗期间的作用。患者接受Dara-KRd方案诱导治疗,并在不同时间点(诱导结束后、大剂量化疗序贯自体干细胞移植[HDCSCT]后、每4个周期巩固治疗后)进行骨髓MRD检测,以指导Dara-KRd方案的使用和持续时间,连续两次MRD阴性评估的患者停止治疗。在纳入的123例患者中,43%无高危细胞遗传学特征,37%有1个高危细胞遗传学特征,20%有2个高危细胞遗传学特征,96%有NGS可追踪的骨髓MRD。中位随访25.1个月,80%的患者达到MRD阴性(0、1和2+个高危细胞遗传学患者钟分别为78%、82%和79%),包括66%达到MRD<10-6;71%在治疗期间达到连续两次MRD阴性,并进入无治疗监测。2年无进展生存率为87%(有0、1和2+个高危细胞遗传学的患者分别为91%、97%和58%)。在有0个、1个或2+个HRCA的患者中,停止治疗后12个月的MRD反弹或进展的累积发生率分别为4%、0%和27%。
一项3期临床试验(GEM2012MENOS65)在新诊断骨髓瘤患者中评估了来那度胺和地塞米松联合或不联合伊沙佐米维持治疗,如果骨髓MRD阴性则在24个周期后停止治疗。结果维持治疗24个月后达到MRD阴性的患者在4年时的进展率较低(17.2%),强烈提示维持治疗的持续时间可以根据MRD阴性进行调整。
关于高危MM患者中实现MRD阴性和早期复发的数据已经报道,但尚未发表,包括Dara-VTd的CASSIOPEIA研究。虽然仍需更长时间的随访,但这些试验已经提示,对于标危细胞遗传学异常的患者,停止治疗可能是可行的,但对于高危细胞遗传学异常的患者则不可行。
结合骨髓和影像学评估可能对一线高危细胞遗传学患者的MRD评估更有意义。
评估来那度胺维持治疗期间MRD动态的2期研究报告了另一个重要观察结果:失去MRD阴性的患者比MRD持续阴性的患者更有可能发生进展(HR=无穷尽;P<0.0001),这是可以预料的,但也比MRD持续阳性的患者更差(HR=5.88,P=0.015)。这些数据表明,当考虑使用MRD作为治疗指导时,其动态是另一个非常重要的参数。
正在进行中的MIDAS试验(NCT04934475)旨在根据初治MM患者诱导治疗后的MRD状态评估HDCSCT的作用。患者接受6个周期的isatuximab/卡非佐米/来那度胺/地塞米松(isa-KRd)四联方案诱导治疗,并在诱导后评估骨髓MRD(阈值为10-5个细胞)。患者接下来分层为标危(MRD阴性<10-5)或高危(MRD阳性>10-5);诱导后达到MRD阴性的患者随机分组,一组接受另外6个周期的Isa-KRd治疗序贯维持治疗,另一组为HDCSCT序贯两个周期的Isa-KRd治疗,并使用来那度胺维持治疗3年。将诱导后MRD阳性患者随机分组,一组接受HDCSCT序贯两个周期isa-KRd和isatuximab-iberdomide维持治疗3年;另一组接受串联HDCSCT序贯isatuximab-iberdomide维持治疗3年。这项雄心勃勃的试验将阐明MRD状态是否可用于指导治疗,以及对于诱导后达到早期MRD阴性的患者,HDCSCT是否仍然是金标准。
其他多项随机临床试验也在评估基于MRD的治疗决策。PERSEUS试验(NCT03710603)将评估在的持续MRD阴性12个月且维持治疗24个月以上的情况下停用达雷妥尤单抗的可能性,以及在MRD转换(从阴性转为阳性)或在CR单位未达到IMWG疾病进展标准的情况下重启达雷妥尤单抗治疗的获益。AURIGA试验(NCT03901963)将达到VGPR但MRD阳性的患者随机分组,分别接受达雷妥尤单抗联合来那度胺治疗和来那度胺维持治疗,主要终点是维持治疗开始后12个月时的MRD转换率。SWOG (S1803)开展的DRAMMATIC试验(NCT04071457)将患者随机分组,分别在HDCSCT后接受达雷妥尤单抗联合来那度胺治疗和来那度胺维持治疗,维持治疗2年后评估MRD以指导进一步治疗。MRD阳性患者继续接受所分配的治疗,而MRD阴性患者将进一步随机分组,继续或停止所分配的治疗。ECOG (EAA171)开展的OPTIMUM试验(NCT03941860)将HDCSCT后接受来那度胺维持治疗的MRD阳性患者随机分组,分别在继续接受来那度胺的基础上接受伊沙佐米或安慰剂治疗。
参考文献
Szalat R, Anderson K, Munshi N. Role of minimal residual disease assessment in multiple myeloma. Haematologica; https://doi.org/10.3324/haematol.2023.284662
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言

















#多发性骨髓瘤# #MM# #MRD#
77