心血管治疗类医疗器械非劣效性试验特点及界值设置的系统评价
2024-03-17 冯堃, 郭琼, 钟文涛, 等 中国循证医学杂志 发表于威斯康星
中国心血管疾病现患人数高达3.3亿并持续上升,疾病负担较大[1]。在迫切的临床需求下,心血管疾病领域的创新医疗器械发展迅速,在疾病的诊断、治疗以及康复随访等各个阶段均发挥了重要作用[2]。其中,经皮冠
中国心血管疾病现患人数高达3.3亿并持续上升,疾病负担较大[1]。在迫切的临床需求下,心血管疾病领域的创新医疗器械发展迅速,在疾病的诊断、治疗以及康复随访等各个阶段均发挥了重要作用[2]。其中,经皮冠状动脉介入术所使用的冠状动脉支架、球囊等医疗器械发展最为突出[3]。2021年9月至2022年8月,我国有130项国产心血管三类器械获批,其中有115项为介入类器械[1]。此领域的同品种器械众多,同时更新换代快、迭代周期短[4],研究者在开展临床试验时总是希望可以最大程度缩短研发周期,因此对其临床评价多采用非劣效性试验设计。
非劣效性试验设计目的是拟证明新干预的效果不比对照组的效果差,或者效果略差但没有超过临床上可以接受的程度[5]。即使新干预在疗效上相比对照组不一定更优,但可能具有其他方面的优势,如治疗过程创伤产生更小、使用剂量更少、患者花费更少、患者接受度和可及性更高等。此外,出于伦理风险考虑,心血管领域的器械在开展临床试验的过程中使用安慰剂对照或空白对照不恰当,因此多选择阳性对照(如金标准治疗)[6]。然而在已有标准治疗手段的基础上进一步证明某种新干预显著更优是非常困难的[7],不同品牌与代次的同品种器械虽然在功能上不断进步,但其疗效差异有限。因此非劣效性试验设计的优势逐渐显现,已成为评价创新医疗干预的重要工具之一[8],如SYNTAX试验[9]、PRECOMBAT试验[10]、SORT OUT试验[11]等非劣效性试验,均为心血管领域创新器械上市提供了关键性证据。
开展非劣效性试验的关键在于确定两种干预效果相差多少是临床可接受的范围,即确定非劣效性界值。一般非劣效性界值应小于等于临床可接受的最大差值范围,且小于阳性对照干预与安慰剂的疗效差异[12]。然而,对于非劣效性界值的设置方法尚未统一规范[13],既往研究表明非劣效性试验设计多存在界值设置依据报告不清[14]、不同研究间同一指标的界值设置差异过大[15,16]等问题。Donken等[17]的研究就发现评价疫苗的非劣效性试验的界值设置从小于5%到30%不等,跨度较大。非劣效性界值的设置将直接影响研究样本量大小及结果解释,不恰当的界值设置将导致错误或难以解释的研究结论,进而影响新干预措施的市场准入[18]。
目前心血管领域非劣效性试验的研究质量尚不清楚,尤其是其非劣效性界值设置情况仍不了解,故本研究全面检索心血管领域医疗器械干预的非劣效性试验,调查其方法学质量,尤其是非劣效性界值设置情况,为未来提高心血管领域非劣效性试验的设计质量提供参考。
1 资料与方法
1.1 纳入与排除标准
1.1.1 研究类型
非劣效性设计试验。
1.1.2 研究对象
接受治疗的心血管疾病患者,其年龄、性别、国籍等不限。
1.1.3 干预措施
试验与对照措施均为心血管领域治疗类医疗器械,包括手术作用器械(如冠状动脉介入治疗器械、结构性心脏病介入器械、起搏及电生理器械)、手术辅助器械(如导管、介入机器人)等。
1.1.4 结局指标
不限。
1.1.5 排除标准
① 药物与医疗器械联合治疗;② 未报告非劣效性设计相关信息;③ 文章类型为壁报、评论、信件类的研究;④ 重复发表的研究;⑤ 无法获取全文;⑥ 非英文文献。
1.2 文献检索策略
计算机检索PubMed、Embase、CENTRAL数据库,搜集心血管领域医疗器械类的非劣效性试验,检索时限均为建库至2023年7月26日。检索采用主题词与自由词相结合的方式进行,并根据各数据库特点进行调整。同时检索纳入研究的参考文献,以补充获取相关资料。检索词包括:non-inferiority、non-inferior、cardiovascular diseases、coronary disease、stroke、cerebrovascular disorders、atrial fibrillation、myocardial infarction等。以PubMed数据库为例,其具体检索策略见附件框1。
1.3 文献筛选
由2名经过培训的研究者独立进行文献筛选。根据文献标题和摘要进行初筛,排除明显不相关文献,随后获取并阅读其全文以进行复筛,最终确认研究所纳入的文献。当2名研究者意见不一致时,由第三位研究者协助判断并讨论其是否纳入。
1.4 资料提取
资料提取的主要内容包括:① 纳入研究的基本信息,包括研究作者、发表年份、发表期刊、发表国家、资金资助等;② 非劣效性试验设计特征:包括样本量、试验臂数量、干预/对照组类型、非劣效性终点效应值变量类型(分类变量/连续变量);③ 非劣效性界值:包括设置依据、界值指标、界值大小、界值类型等;④ 研究结果信息:包括试验开展前预估的和试验开展后实际的干预组与对照组的效应值。
1.5 统计分析
采用Excel 2020和R 4.2.1软件进行统计分析与图表绘制。采用描述性统计报告结果,定性资料采用频数(n)和百分比(%),定量资料采用中位数、四分位数间距(interquartile range,IQR)和界值范围描述结果。纳入研究的非劣效性绝对界值与相对界值使用以下公式转换:
 |
非劣效性界值受不同干预影响差异较大,因此在非劣效性界值设置现状的研究中,针对同种干预的同种指标开展亚组分析,且只分析纳入同一亚组内研究数量大于等于5篇的终点指标类型。
2 结果
2.1 文献筛选流程及结果
初检出相关文献18 930篇,包括:PubMed(n=6 718),Embase(n=8 468),CENTRAL(n=3 744)。经过逐层筛选后,最终纳入214篇非劣效性研究。文献筛选流程和结果见附件图1。
2.2 纳入研究的基本特征
纳入研究的基线特征见表1。
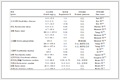 表1 纳入研究的基本特征
表1 纳入研究的基本特征2.3 纳入的非劣效性试验特征
纳入的非劣效性试验特征见表2。纳入的非劣效性试验多为双臂试验(199,92.9%),有极少数研究(15,7.1%)为单臂、三臂和四臂试验。119篇(55.6%)研究纳入样本量小于500例,另有11篇(5.1%)样本量超过3 000例。纳入研究干预措施主要为冠状动脉支架(167,78.0%),其次为冠状动脉球囊(21,9.8%),其他医疗器械干预包括导管射频消融、左心室辅助装置、心脏起搏器等。研究的冠状动脉支架类型多样,包括普通药物涂层支架(drug-eluting stents,DES)、可生物降解涂层支架(biodegradable polymer drug-eluting stents,BP-DES)、无聚合物涂层支架(polymer-free drug-eluting stents,PF-DES)、生物可吸收支架(bioresorbable vascular scaffolds,BVS)和金属裸支架(bare-metal stents,BMS)等,其中比较不同DES的试验最多(68,31.8%),其次为比较BP-DES与DES(51,23.8%)。
 表2 纳入的非劣效性试验特征
表2 纳入的非劣效性试验特征不同非劣效性试验的非劣效性终点指标选择各不相同,其中最常见的非劣效性定性终点指标为靶病变失败率(target-lesion failure,TLF)(35,16.4%)、主要心血管不良事件(major adverse cardiovascular events,MACE)发生率(20,9.3%)和靶血管失败率(target-vessel failure,TVF)(12,5.6%)。而最常见的非劣效性定量终点指标为晚期管腔丢失(late lumen loss,LLL),其包括支架内LLL(32,15.0%)和节段内LLL(27,12.6%)。
所有纳入的非劣效性试验均报告了具体的非劣效性界值,其中绝大多数(207,96.7%)采用绝对非劣效性界值。部分研究(46,21.5%)并未报告非劣效性界值的设置依据,150篇(70.1%)研究在确定非劣效性界值过程中考虑了对照组的效应值,其中117篇(54.7%)研究说明了预估对照组效应值的来源。189篇(88.3%)研究最终得到试验组非劣于对照组的结果。
2.4 非劣效性界值设置现状
纳入研究中常见的终点指标所设置的非劣效性界值见表3。不同试验所设置的非劣效性界值差异较大,其中TVF的非劣效性绝对界值设置范围为2.5%至19.6%,设置差异最大。球囊与支架研究均采用节段内LLL作为非劣效性终点,球囊研究的非劣效性绝对界值高于支架研究。将纳入研究中的非劣效性绝对界值换算为所对应的相对界值,其范围为1.20~3.67。
 表3 纳入研究最常见非劣效性终点指标的非劣效性界值
表3 纳入研究最常见非劣效性终点指标的非劣效性界值在以心血管支架和球囊为干预措施的研究中,研究者估计的对照组效应值与非劣效性绝对界值关系如图1所示。根据美国食品药品监督管理局(Food and Drug Administration,FDA)颁布的《非劣效性试验指导原则》,建议将非劣效性界值设置为对照组效应值的50%[19],因此部分研究采用相对非劣效性界值=1.5的所对应的非劣效性绝对界值作为非劣效性判定依据。然而对于干预、对照及终点指标选择均相同的试验,不同研究间所设置的非劣效性界值差异较大。冠脉支架干预研究中,以MACE为终点结局的共纳入13篇,其中非劣效性相对界值大于1.5的有7篇,小于等于1.5的有6篇;以靶病变失败率为结局的共纳入30篇,其中非劣效性相对界值大于1.5的有13篇,小于等于1.5的有17篇;以靶血管失败率为结局的共纳入9篇,其中非劣效性相对界值大于1.5的有5篇,小于等于1.5的有4篇。在以二分类变量为终点指标的研究中(n=52),共有5篇研究未做出非劣效性统计推断,其非劣效性相对界值均小于等于1.5;在以连续变量为终点的研究中(n=37),共有6篇研究未做出非劣效性统计推断,其中3篇非劣效性相对界值小于1.5,另3篇大于1.5。
 图1 预估的对照组效应值与非劣效性绝对界值的分布
图1 预估的对照组效应值与非劣效性绝对界值的分布3 讨论
本研究发现,心血管领域医疗器械干预非劣效性试验中研究干预多以冠状动脉支架(78.0%)、球囊(9.8%)为主,研究多采用双臂设计(92.9%),大多使用非劣效性绝对界值(96.7%)作为非劣效性结论的判定依据。70.1%的研究基于预估的对照组效应值确定非劣效性界值,其中15.4%的研究未报告预估的对照组效应值来源。非劣效性试验终点结局指标多样,TLF、TVF、MACE是研究数量最多的三项定性指标,LLL是研究数量最多的定量指标。将所有指标的非劣效性绝对界值转化为相对界值后,范围为1.20~3.67,同一干预、同一指标下的非劣效性界值设置差异较大。
本文纳入研究大多采用双臂试验设计,试验组与对照组样本量比例设置为1∶1,然而标准非劣效性试验应当采用三臂设计,即同时纳入试验组、对照组和安慰剂组,在证明试验组不劣于对照组的同时保证对照组优于安慰剂组[19]。但由于在心血管领域疾病治疗中采用安慰剂对照存在医学伦理问题,故既往非劣效性试验多采用双臂设计。采取双臂需保证试验中对照干预与既往历史研究中的对照干预是同质的,即保证对照干预优于安慰剂,此时证明试验组干预的非劣效性才具有临床意义。
在纳入的研究中,大多数研究采用了非劣效性绝对界值作为统计推断的依据,一项非劣效性试验的Meta分析所纳入的研究中有94.8%的原始研究采用非劣效性绝对界值作为统计推断的依据[20],与我们的结果一致。使用非劣效性绝对界值进行统计推断的优势在于临床意义明确,结果也更容易解释,但其无法直接体现试验干预相比阳性对照组的相对差距。此外,也有研究表明在非劣效性统计推断过程中,使用绝对或相对界值会对检验效能与检验水准产生一定影响[21]。在确定非劣效性界值时,应综合考虑绝对界值与相对界值所带来的影响。
我们发现在纳入研究中,不论干预为何种支架,其非劣效性对照干预均以DES为最多。心血管支架问世初期主要采用BMS设计,紧接着出现了DES,随着技术发展逐渐出现了BP-DES、PF-DES和BVS[22]。我们分析造成此现象的原因在于DES上市时间较早,相关数据较为全面,其安全性、有效性已经得到充分验证,而新产品很难在安全性、有效性上获得更大优势,因此多选择开展非劣效性试验。
非劣效性界值的设定与研究背景密切相关,需要考虑临床意义与统计学意义并综合确定。有学者认为如果新的干预能够更大地减少患者负担,则设置相对较大的非劣效性界值是合理的[23]。研究者对于对照干预的看法在很大程度上能够影响非劣效性界值的设置,因此报告非劣效性界值设置依据对于判定研究是否科学合理至关重要。纳入的研究中,21.5%未报告非劣效性界值的设置依据,另有15.4%未报告设置非劣效性界值所使用的数据来源,非劣效性界值的设置依据的报告质量有待提升。
非劣效性界值的设置情况会直接影响统计推断结果,FDA颁布的《非劣效性试验指导原则》中建议,一般情况下可以将非劣效性界值设置为对照组效应值的50%[19]。在定性资料的研究中,TLF和MACE的非劣界值设置围绕在对照组效应值的50%左右,而TVF与定量变量的界值设置与50%存在较大偏离。我们所分析的研究均为低优指标,在定性资料的研究中未做出非劣效性推断的研究其非劣效性相对界值均小于等于1.5(偏向于更难做出非劣效性统计推断的设置),且其预估的对照组效应值均处于同类研究的极端值水平,可见非劣效性试验中绝对界值与相对界值会共同对统计推断产生影响。
既往有研究报告了以死亡为结局的非劣效性界值设置与研究设计情况[15]、不同研究非劣效性界值设置依据的分析调查[16],但均未涉及某个具体的疾病领域,没有对非劣效性界值的分布情况进行分析。本研究首次全面检索心血管治疗领域医疗器械的非劣效性研究,主要关注纳入研究的非劣效性界值的指标选择、设置依据与分布情况。
本研究亦存在局限性:① 心血管领域医疗器械种类众多,本研究只分析了占比最高的冠脉支架和球囊干预研究的界值具体设置情况,且分析样本较少,可能对结果的稳定性造成潜在影响;② 本研究为二次研究,研究质量受原始研究质量影响,部分原始研究存在数据报告不全的情况。
综上所述,心血管疾病治疗类医疗器械的非劣效性研究干预多为冠状动脉支架与球囊,研究设计以双臂试验为主,非劣效性试验终点结局指标多样,多采用非劣效性绝对界值;相同干预、相同指标下非劣效性界值设置的差异较大,存在较多极端值;部分研究非劣效性界值置依据未报告或报告不清晰。希望在未来的研究中,研究者在设置非劣效性界值的过程中能够同时考虑绝对与相对界值,同时在方法部分简洁明了地报告非劣效性界值设置过程,以方便读者评判其设置的合理性。
原始出处:
冯堃, 郭琼, 钟文涛, 刘悦, 刘宇琪, 冷柔菲, 许译涵, 顾先林, 龙囿霖, 杜亮, 李正赤, 黄进. 心血管治疗类医疗器械非劣效性试验特点及界值设置的系统评价. 中国循证医学杂志, 2024, 24(3): 288-294. doi: 10.7507/1672-2531.202312134
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#心血管# #非劣效性试验# #界值标准#
76