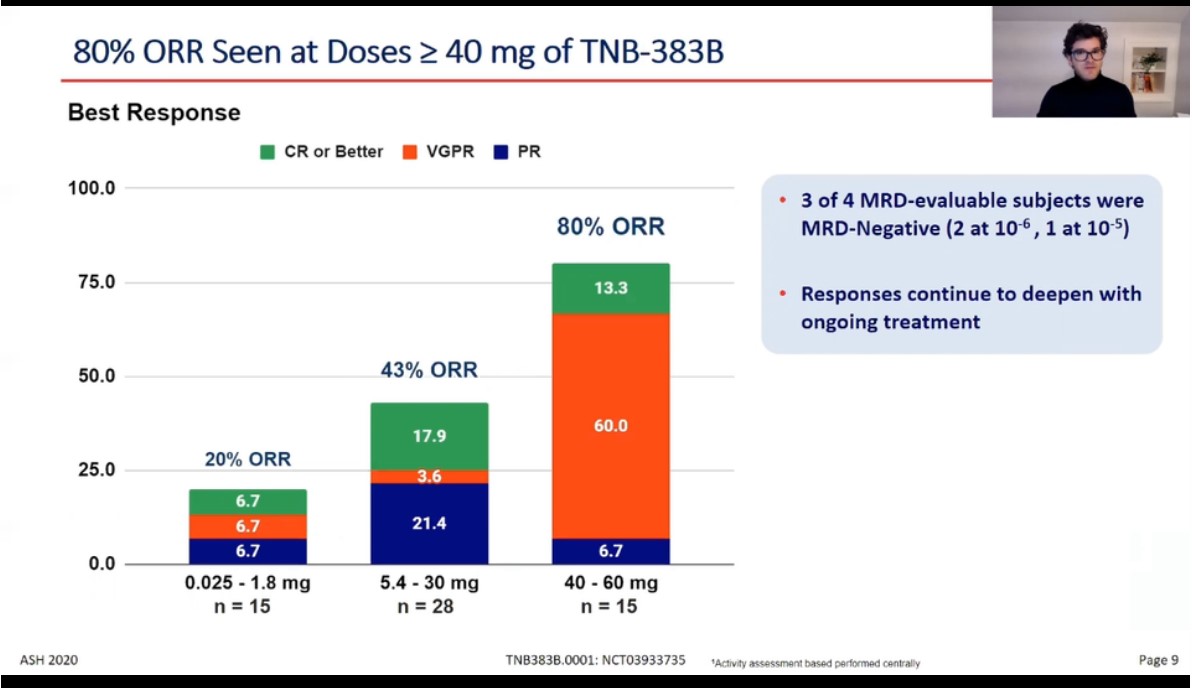
Robert Galbraith—Reuters 新闻概要 安进(Amgen)将支付 9 亿美元预付款收购 Teneobio,Teneobio 是一家拥有发现和开发抗体药物技术的生物技术公司。 尽管安进已经拥有自己的抗体平台,但该公司表示,Teneobio 的技术和药物资产将与其自身形成互补。 7月27日,安进(Amgen)和Teneobio宣布一项协议,根据该协议,安进同意收购Teneobio。后者是一家临床阶段的生物技术公司,正在开发一类重链抗体的新型生物制品。根据协议条款,安进将以9亿美元的预付款在收盘时收购Teneobio的所有已发行股票,以及未来向Teneobio股权持有人支付可能高达16亿美元的里程碑付款。 据了解安进已拥有抗体平台技术,该平台已研发出获得 FDA 批准的药物,以及更多仍在研发中的治疗候选药物。 但在Teneobio,安进看到了一种有吸引力的抗体药物发现和开发替代技术。据安进称,Teneobio的能力将帮助其开发具有治疗多种疾病潜力的新分子。此次收购包括Teneobio公司专有的双特异性和多特异性抗体技术,这将使发现和开发新分子(new molecules)的速度和效率得到显著的加速,这些新分子有可能用于治疗安进核心治疗领域的各种重要疾病。这些平台补充了安进现有的抗体能力,增加了一个重链抗体平台,该平台允许对靶标结合物进行精简的、基于序列的发现方法。 安进的抗体技术 BiTE(双特异性 T 细胞接合器的缩写)生产由两种抗体组成的药物,一种与肿瘤上的抗原结合,另一种与 CD3(T 细胞上的一种蛋白质)结合。 Teneobio 还开发了双特异性 T 细胞接合器,Amgen 表示这项技术将补充 BiTE。但 Teneobio 拥有一项额外的技术TeneoSeek,用于开发多特异性抗体,该公司将其称为“UniAbs”。这家生物技术公司表示,TeneoSeek 可以快速识别出大量针对特定治疗目标的独特结合分子。根据Teneobio 的说法,这项技术可以生产多特异性治疗蛋白,可以针对多个目标,比目前可用的抗体药物更进一步。 Teneobio的新型T细胞接合器(T cell engager)平台,通过为安进目前的BiTE平台提供一种差异化但互补的方法,扩展了安进在双特异性T细胞接合器中现有的领导地位。 “Teneobio 的抗体平台补充了我们现有的能力,并有可能为我们提供更多样化的构建模块,可以开发成新的多特异性疗法,”安进研发执行副总裁 David Reese 在一份准备好的声明中说. “此外,Teneobio 的 CD3 接合器技术的可用性将使我们能够扩大产生双特异性的能力,并利用我们自己的技术,根据疾病和目标定制分子的 T 细胞接合域。” Teneobio产品管线包括双特异性和多特异性抗体药物,其中一些正在与其他公司合作开发。葛兰素史克(GSK)和强生子公司杨森是 Teneobio 的合作伙伴,开发针对癌症的多特异性抗体。通过名为 TeneoOne 的子公司,Teneobio 还与艾伯维 (AbbVie) 结盟,专注于开发针对多发性骨髓瘤的双特异性抗体TNB-383B。 今年6月24日,艾伯维 (AbbVie) 达成协议,收购了该子公司 TeneoOne 及其第 2 阶段准备好的治疗候选药物。协议规定,TeneoOne可获得9000万美元预付款,并负责TNB-383B的I期临床研究。而艾伯维则可获得收购TeneoOne的独家选择全和领导TNB-383B后续开发和推广的权益。TNB-383B是一款全人源BCMA/CD3双抗,采用KIH技术将固定轻链(FLC)与重链(HCO)配对结合,FLC可以弱激活CD3,HCO有两个高亲和力的抗BCMA基团。TNB-383B还具有一个沉默的人IgG4 Fc段,可以限制非特异性激活并有着较长的半衰期。 TNB-383B 第一期临床试验中期分析结果表现亮眼,使得艾伯维决定收购TeneoOne。该临床试验主要评估在先前已接受过至少 3 线治疗的复发/难治性多发性骨髓瘤患者(n=24)接受 TNB-383B 后的安全性、临床药理学和临床活性。结果显示,在剂量递增组中,剂量 ≥ 40 mg 时 TNB-383B 的客观反应率(ORR)为79%,非常好的部分反应率(VGPR)为 63%,完全反应率(CR)为 29%。追踪中位数时间为 6.1 个月时,其反应持续时间(DOR)中位数尚未达到。 多发性骨髓瘤(multiple myeloma)被认为是第二大最常见的血癌,仅次于急性淋巴性白血病。全球每年约有 16 万多例新确诊病例,占所有血癌的 10% 以上。 2020 年这项疾病的全球药物市场规模为 83 亿美元,预计到 2027 年,将达到 175 亿美元,复合年增长率约 11.2%。 此次收购还将为安进的研发管线增加TNB-585,一种用于治疗转移性去势抵抗性前列腺癌(mCRPC)的双特异性T细胞接合器,目前处于1期临床试验阶段;以及数个具有近期新药临床试验(IND)申报潜力的临床前肿瘤管线资产。TNB-585是安进现有前列腺癌产品组合的补充,包括处于1期临床试验阶段的acapatamab(前称AMG 160)和AMG 509。 安进研发执行副总裁David M. Reese医学博士说:“收购Teneobio将加强我们开发治疗严重疾病患者的创新药物的能力,并将潜在'best-in-class'产品推向市场,特别是针对我们核心治疗领域广泛疾病靶点的多特异性和双特异性药物。Teneobio的抗体平台补充了我们现有的能力,并可能给我们提供一套更多样化的可开发成新的多特异性治疗药物构件模块。此外,Teneobio的CD3结合器技术将拓宽我们生成双特异性抗体方面的的能力,通过我们自己的技术,能够根据疾病和靶标定制分子的T细胞结合域。” “Teneobio团队非常高兴与生物治疗药物先驱安进联手,安进的研发资源及其在免疫肿瘤学方面的广泛临床经验非常适合应用和推进Teneobio的差异化技术和多特异性抗体,”Teneobio首席执行官Roland Buelow博士说,“在过去5年中,Teneobio在针对众多适应症有效设计差异化的多特异性和双特异性疗法方面发展了领先的专业知识,与第一代T细胞接合器相比,具有潜在更好的安全性、有效性和药代动力学特征。总之,我们共同致力于快速发现、开发和向有需要的患者提供新型且有意义的疾病修饰性多特异性抗体。” 
 medcitynews
medcitynews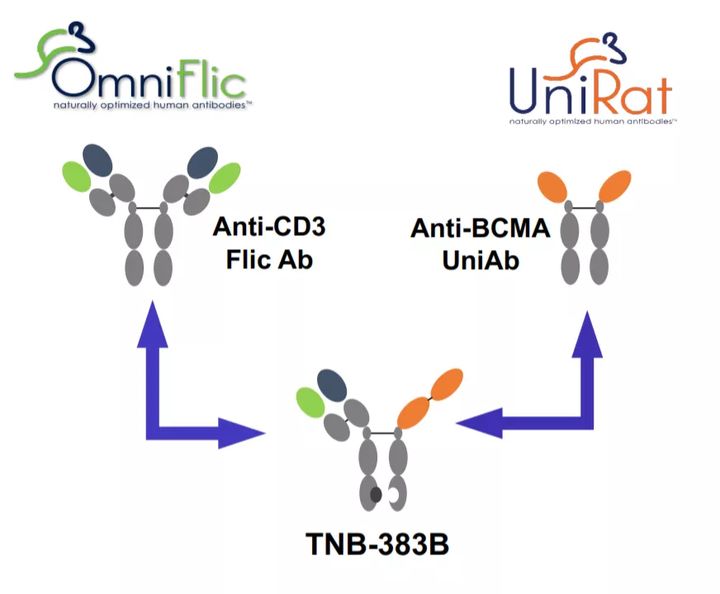
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#Bio#
68
#抗体药物#
86
#抗体药#
92