Nat Commun:科学家发现肿瘤免疫治疗潜在靶点!
2022-04-23 生物谷 生物谷
该研究发现了一种RBP DENR可以调节PD-L1表达以逃避肿瘤免疫,并突出了DENR作为免疫治疗靶点的潜力。
程序性死亡配体1(PD-L1)通常在肿瘤细胞和免疫细胞如巨噬细胞和树突状细胞上表达,PD-L1与其在T细胞上的受体程序性细胞死亡-1(PD-1)之间的相互作用抑制了这些细胞的肿瘤杀伤活性。近年来,PD1 / PD-L1阻断剂的发展的癌症研究最令人兴奋的进展之一,然而,只有一小部分患者可以从抗PD-1 / PD-L1治疗中受益。RNA结合蛋白(RMP)可以识别数千种有助于维持细胞稳态的RNA,并且在各种癌症中经常观察到RBP功能障碍。然而,特异性RBPs是否通过调节程序性死亡配体-1(PD-L1)参与肿瘤免疫逃逸尚不清楚。近日,发表在Nat Commun上的一篇题为“DENR controls JAK2 translation to induce PD-L1 expression for tumor immune evasion”的研究性论文对这一问题进行了具体分析。

在本研究中,为了公正和系统地筛选PD-L1的转录后调节因子,研究人员构建了一个新的定制RBP CRISPR迷你文库,该RBP文库每个基因包含1467个已知RBPs的10个单向导(sg)RNA,以及阳性和阴性对照sgRNA,使用荧光激活的单细胞分选(FACS)来量化PD-L1表达水平,通过合并CRISPR筛选,确定DENR是PD-L1的调节剂。为了验证DENR(一种RBP,可直接结合以在体外转移RNA)是否间接调控PD-L1,他们敲除了小鼠结肠腺癌MC38细胞中的DENR基因,并分别通过免疫印迹、FACS和RT-qPCR测定PD-L1的蛋白质和mRNA水平,发现DENR可降低不同细胞系中PD-L1表达。通过进一步潜在信号通路分析,发现DENR通过JAK-STAT信号通路调节PD-L1表达。研究人员又进一步探索了DENR功能在PD-L1调控中的分子机制,通过蛋白质印迹法确定了STAT1/3所有上游因子的蛋白质和磷酸化水平,包括IFNGR1,IFNGR2,JAK1和JAK2,发现DENR直接调节JAK2表达,反过来又驱动PD-L1表达响应IFNγ。通过敲除人类癌细胞系中的DENR,如人结肠HT29癌细胞和人黑色素瘤A375细胞,也导致JAK2蛋白水平降低,表明DENR调节JAK2表达的机制在小鼠和人类中都是保守的。他们测试了Jak2基因上游uORFs的功能,发现uORFs上游Jak2 mRNA确实负责抑制JAK2翻译效率,uORFs的抑制作用直接被DENR拮抗。此外,研究人员发现,DENR与核糖体组成性地结合,沿着所有mRNA不加选择地传播,仅在遇到属于某些mRNA的uORFs时才促进翻译重新启动。肿瘤中的DENR表达通过调节PD-L1表达来支持肿瘤逃避,而DENR KO有助于更快的肿瘤免疫射出,这表明DENR是一种有前途的免疫治疗靶点。最后,他们在临床研究中发现,DENR 与免疫治疗患者生存率相关。肿瘤中较低的DENR表达与给予抗PD-1疗法的患者更好的生存结局相关,但与抗CTLA-4疗法无关,这表明使用DENR作为免疫治疗靶点或标志物的潜在益处。
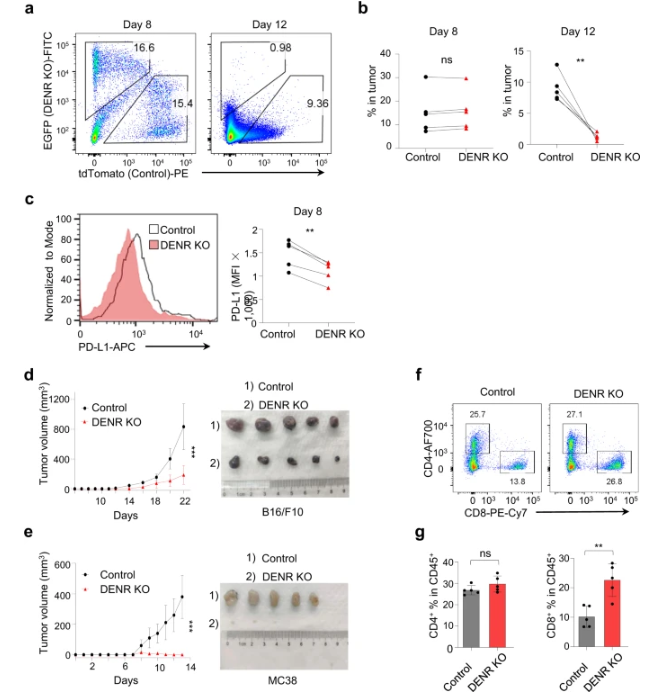
图 DENR耗竭降低肿瘤生长和体内PD-L1表达
总之,该研究发现了一种RBP DENR可以调节PD-L1表达以逃避肿瘤免疫,并突出了DENR作为免疫治疗靶点的潜力。
参考文献:
Chen, B., Hu, J., Hu, X. et al. DENR controls JAK2 translation to induce PD-L1 expression for tumor immune evasion. Nat Commun 13, 2059 (2022). https://doi.org/10.1038/s41467-022-29754-y
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#Nat#
85
#科学家发现#
98
#COMMUN#
84