中国食管癌新辅助治疗中免疫检查点抑制剂的安全性和疗效
2023-07-02 柳叶堂胸外 柳叶堂胸外 发表于上海
今日分享一篇发表在Diseases of the Esophagus杂志2022年的文献,通讯作者是上海交通大学附属胸科医院胸外科的李志刚教授。

前言
目前,可手术切除的局部晚期食管癌的标准治疗是术前放化疗(CRT)或化疗(CT),然后进行根治性切除术。然而,尽管5年生存率已达50%左右,但复发率仍然较高,尤其是术后1年内发生远处转移和早期失败的患者。事实上,自2012年放化疗联合手术治疗食管癌研究(CROSS)以来,局部晚期食管癌的治疗进展有限。此外,在CROSS研究的10年随访中,新辅助放化疗+手术患者的非肿瘤原因死亡率高于单纯手术患者(15% vs. 11%),提示局部放疗可能存在远期损伤。
在过去10年中,免疫检查点抑制剂(ICIs)与CT、放疗和手术一起迅速成为包括食管癌在内的几种癌症的治疗支柱。迄今为止,ICI治疗食管癌的证据主要局限于晚期疾病患者。Keynote590 (pembrolizumab, NCT03189719)、CheckMate648 (nivolumab, NCT 03143153)和ESCORT-1st (camrelizumab, NCT 03691090)的研究结果表明,ICI在晚期食管癌的一线治疗中具有较好的疗效。CheckMate577(纳武利尤单抗,NCT02743494)研究表明,对于新辅助CRT和手术后有残留病变的患者,纳武利尤单抗辅助治疗与延长无病生存期、减少远处转移以及可接受的毒性相关。此外,ICI在新辅助治疗中的应用也在过去2年中受到关注,并有多项临床试验报道。
由于术前ICI的潜在优势,包括暴露整个肿瘤抗原和导致更多样化的免疫应答,在一些实体肿瘤的新辅助治疗中显示出比辅助治疗更好的效果。然而,术前免疫系统的激活也有一些考虑因素,包括延迟手术、增加手术复杂性和围手术期发病率的可能性。因此,ICI作为食管癌新辅助治疗是否有益尚不明确,需要进一步研究。
以中国抗癌协会食管癌专业委员会成员单位为单位,通过多中心资源收集内部数据。主要目的是评估在不同医疗机构中,ICIs作为食管癌新辅助治疗的安全性和疗效。
据我们所知,这是第一项针对真实世界患者的食管癌新辅助免疫治疗安全性和有效性的专门研究。免疫治疗新辅助治疗的TRAEs率为53.8%,pCR率为25.8%,与nCRT相当,提示免疫治疗可安全有效地用于局部晚期食管癌的新辅助治疗。
摘要
目的
免疫检查点抑制剂(ICI)在食管癌新辅助治疗中显示出强大的获益,但其安全性和疗效的证据有限,可能无法反映真实世界的实践。
方法
回顾性分析2019年5月至2020年12月国内15家食管癌中心接受ICI新辅助治疗的局部晚期食管癌初治患者的临床资料。主要终点为治疗相关不良事件(TRAEs)和免疫相关不良事件(irAEs)的发生率和严重程度。次要观察指标包括病理完全缓解(pCR)率、R0切除率、病死率和并发症率。
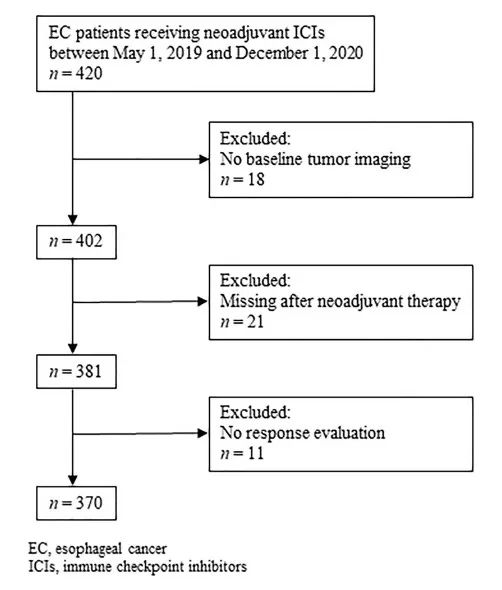
结果
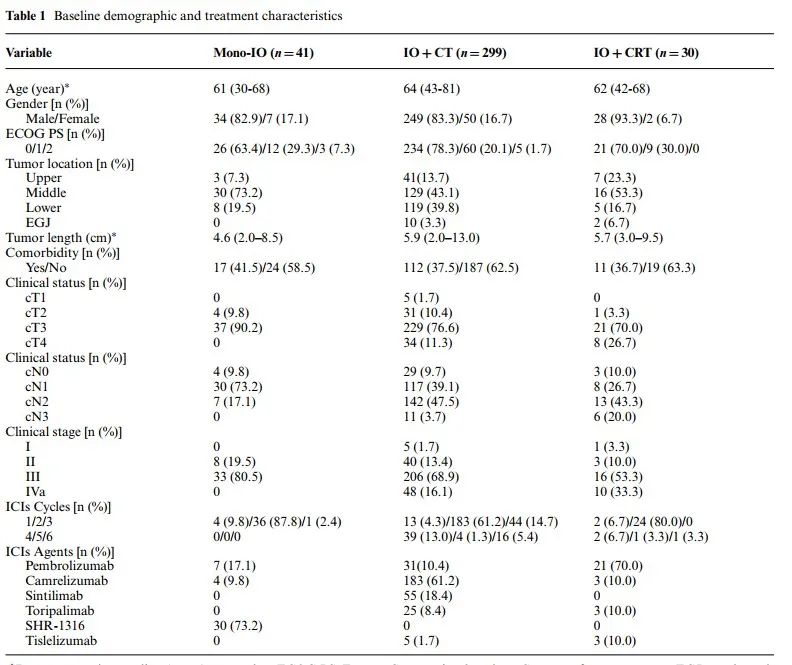
370例患者中,男性311例(84.1%),中位年龄63(30-81)岁,III或IVa期患者占84.1%。299例(80.8%)患者接受了ICI联合化疗。199例(53.8%)患者发生TRAEs,其中1-2级占39.2%;3-4级13.2%;5级 1.4%);24.3%的患者发生irAE,且多为1-2级(21.1%)。341例(92.2%)患者接受手术治疗,其中333例(97.7%)达到R0切除。原发灶局部pCR率为34.6%,其中ypT0N0为25.8%,ypT0N+为8.8%。术后并发症发生率为41.4%,其中3级及以上并发症35例(10.3%)。术后30 d内无死亡,术后90 d内死亡3例(0.9%)。
结论
真实世界数据显示局部晚期食管癌新辅助免疫治疗的不良反应可接受。长期生存结果有待进一步研究。
讨论
据我们所了解,这是第一项专门研究食管癌真实世界患者中新辅助免疫治疗的安全性和有效性的研究。该研究显示,新辅助免疫治疗与传统放化疗方案的治疗结果相当,不良事件发生率为53.8%,pCR率为25.8%,这表明免疫检查点抑制剂可以安全有效地用于局部晚期食管癌的新辅助治疗。
术前新辅助治疗已成为食管癌的标准治疗方式。随着CROSS和NEOCRTEC5010研究的进展,已确认应用新辅助放化疗可以降低局部和区域复发率。然而,新辅助放化疗尚未解决手术后远处转移率高的问题,并且CROSS研究的10年随访结果表明可能存在辐射的长期损害。此外,单独应用术前化疗已有报道显示肿瘤反应差且远处转移率高。因此,在新辅助治疗中,我们需要更有效的全身治疗方法。免疫治疗是一种有前景的选择,特别是对于食管鳞癌患者,在晚期食管癌的一线治疗中显示出优越的疗效,从而为免疫治疗在新辅助治疗中确立了重要的角色。
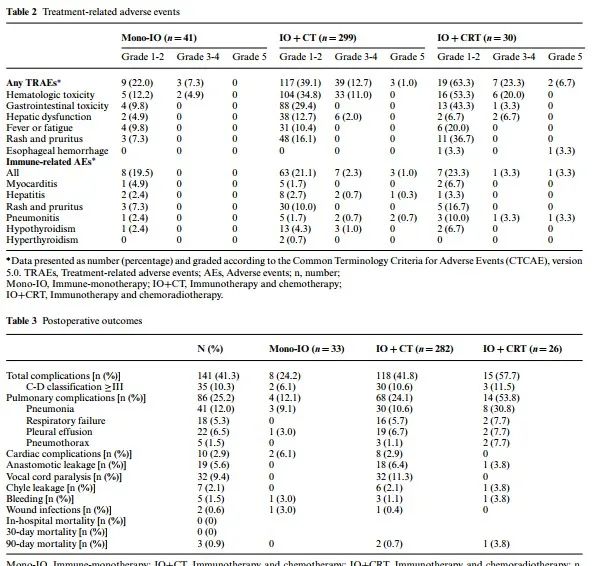
在本研究中,TRAE的发生率为53.8%,5级不良事件发生在5名患者(1.4%),与新辅助放化疗的结果相似。IRAE的发生率为24.3%,主要包括心肌炎、肝炎、肺炎、甲状腺功能减退、皮疹和瘙痒,其中肺炎是最令人担忧的并发症。此外,免疫治疗与放化疗的联合治疗导致了更高的TRAE发生率,但IRAE发生率与其他组相当。Kim等首次报告了一项关于新辅助pembrolizumab加放化疗治疗局部晚期食管癌的II期临床试验。然而,12.9%的死亡率引发了对该方案安全性的关注。随后,PALACE-1研究中,新辅助pembrolizumab加放化疗导致5%的死亡率,主要是由于食管出血。这两项研究揭示了在标准放化疗基础上加用免疫治疗时的安全问题。但是,Memorial学者报告称,新辅助免疫治疗与增加并发症无关。在我们的数据中,有8.1%的患者接受术前放疗,其中两例患者(6.7%)出现了5级出血和肺炎的不良事件。此外,多项研究表明,免疫治疗与化疗的联合应用具有可控的安全性和有希望的抗肿瘤效果,与本研究结果一致。考虑到免疫治疗和放疗可能引起的不良事件,特别是食管穿孔和肺炎的风险增加,免疫治疗与化疗可能是大多数临床试验中的首选组合。然而,新辅助免疫治疗的安全性需要进一步评估。
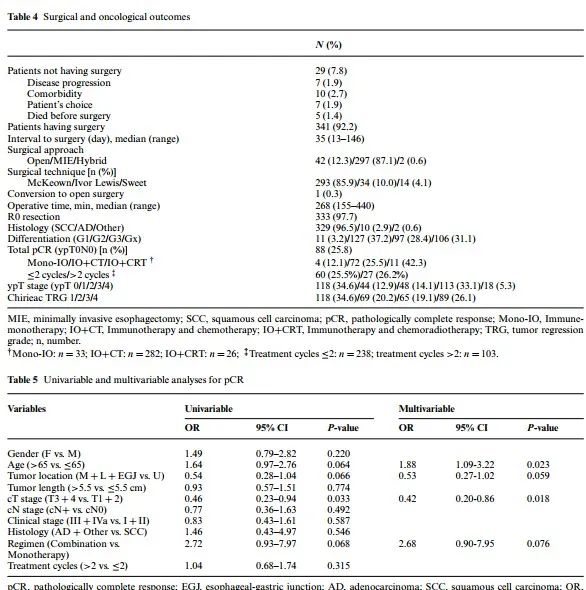
在我们的数据中,IO+CRT组患者的pCR率为42.3%,与CROSS和NEOCRETC5010的结果相当。在PALACE-1研究中,新辅助免疫治疗加放化疗可达到超过50%的pCR率。因此,我们建议免疫治疗的应用至少应与放化疗的结果相当。本研究中IO+CT组患者的pCR率为25.5%。从ESCORT-1st研究的结果来看,紫杉醇联合顺铂的效果优于Keynote590研究中的5-FU联合顺铂。紫杉醇联合顺铂也是本研究中首选的化疗方案。因此,我们推测化疗药物的组合是肿瘤反应的一个非常关键的因素。NICE研究中,每周使用紫杉醇脂质体(nab-紫杉醇)导致了39.2%的pCR率。在本研究中,包含nab-紫杉醇的新辅助方案也具有更高的pCR率(31.8%对比22.5%)。综合以上信息,我们相信在合理的化疗和免疫治疗的组合下可以实现令人鼓舞的pCR结果。
我们还发现早期T分期或年龄超过65岁的患者可能在实现更好的pCR结果方面有一定趋势。因此,在早期阶段患者中,新辅助免疫治疗的应用可能会使积极观察策略成为未来的现实,而对于晚期疾病来说,放射治疗可能非常重要。此外,年轻患者的免疫系统更加强健,这可能导致肿瘤对免疫治疗的敏感性较低。加利福尼亚大学的研究人员报道了年轻女性患者对某些癌症免疫治疗的反应特别低的发现,这可能归因于年轻患者对基于MHC的驱动突变选择表现出最强烈的效果。
我们的数据显示,免疫治疗并没有增加食管切除术及术后并发症的风险。此外,手术的难度也没有增加,就像在肺癌中报道的情况一样。然而,我们观察到ICIs与放化疗联合治疗会伴随着更高的术后肺部并发症发生率。因此,ICIs与放化疗联合治疗的安全性仍需要进一步关注。
这项研究的主要优势在于首次对真实世界的数据进行回顾,并具有较大的样本量。然而,我们也需要讨论一些限制,主要包括回顾性设计、数据报告的非标准化、缺乏生物标志物以及抗癌药物的异质性。此外,该研究未记录肿瘤复发或长期生存的数据。另外,该研究缺乏以CRT或CT(不包括ICIs)作为对照组,以比较新辅助免疫治疗的安全性和疗效结果。
编者
本研究证实了新辅助免疫联合化疗在中国食管癌中的疗效与CRT相近,且安全性较好。可行长期随访,证实其生存获益。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言