广州医科大学附属第二医院胡胜锋团队《自然·通讯》:揭示蛋白质翻译后修饰调控Treg细胞分化新机制
2024-07-18 BioMed科技 BioMed科技 发表于上海
该研究揭示了E3泛素连接酶RNF213介导转录因子FOXO1泛素化修饰对Treg细胞分化的调控具有重要作用。为寻找新的药物靶点治疗MS等自身免疫疾病提供了新的思路。
在全球范围内,多发性硬化症(MS)是最常见的中枢神经系统(CNS)多方面自身免疫性疾病之一,其症状可能会出现大脑损害、视神经损害、脑干损害等,会影响患者的工作能力、生活的状态,甚至危及生命。自身反应性CD4+ T辅助细胞在MS和其他神经炎症性自身免疫性疾病中发挥了关键作用。CD4+ T细胞分化调控机制极其复杂,其中蛋白质的泛素化修饰调控发挥了重要作用。蛋白质的泛素化修饰中的大部分E3泛素连接酶在CD4+ T细胞分化中的作用和机制并不清楚。因此,加强E3泛素连接酶对CD4+ T细胞分化调控机制的研究,对加深理解MS等自身免疫疾病的发病机制,寻找新的药物靶点,具有重要意义。

广州医科大学附属第二医院胡胜锋/广州妇女儿童医院李晓敏/广州市第一人民医院张惠丽团队合作近日以“RNF213 promotes Treg cell differentiation by facilitating K63-linked ubiquitination and nuclear translocation of FOXO1”为题在国际权威期刊Nat Commun上在线发表了相关研究结果。该研究揭示了E3泛素连接酶RNF213介导转录因子FOXO1泛素化修饰对Treg细胞分化的调控具有重要作用。为寻找新的药物靶点治疗MS等自身免疫疾病提供了新的思路。
为了探索RNF213在CD4+ T细胞分化中的作用,研究团队首先构建了RNF213全身敲除小鼠和RNF213在CD4+ T细胞特异性敲除小鼠,检测了正常小鼠和实验性变态反应性脑脊髓炎(EAE)模型小鼠CD4+ T细胞的分化情况(图1);随后分离小鼠naive CD4+ T细胞,探讨体外标准分化条件下RNF213对CD4+ T分化的影响; 最后开展T细胞混合转输过继实验和体外实验等,进一步阐明RNF213对Treg免疫抑制能力的影响(图2);最终证明了RNF213在CD4+ T细胞中可特异性促进Treg细胞分化,抑制机体自身免疫疾病发病的严重程度。
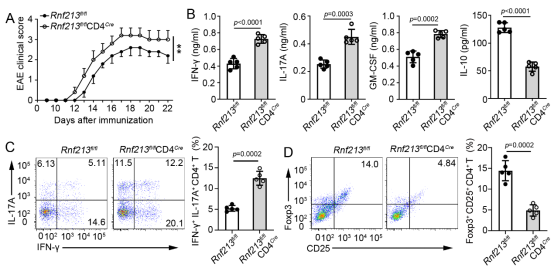
图1. RNF213在CD4+ T细胞中的缺陷促进了EAE发病
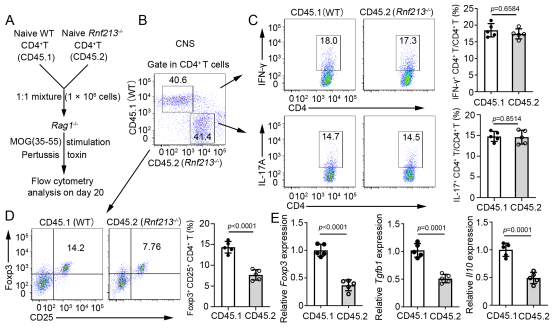
图2. RNF213在CD4+ T细胞中特异性抑制了Treg细胞分化
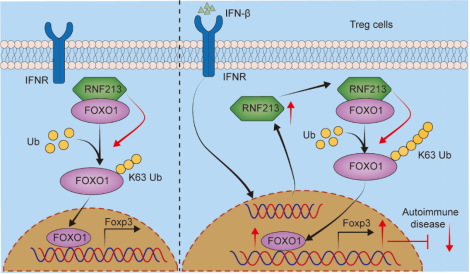
进一步为了探索RNF213调控Treg细胞分化的机制,研究团队通过质谱分析并通过免疫共沉淀证明,RNF213可与叉头盒蛋白O1 (FOXO1)结合;随后在转入相关质粒的HEK 293T细胞和CD4+ T细胞中开展IP实验,并检测FOXO1的表达和泛素化水平,证实了RNF213可调控FOXO1的K63位泛素化和核转位(图3)。并且随后在人细胞中验证了上述结果,值得注意的是,研究团队发现RNF213在CD4+ T细胞中可由IFN-β诱导产生,并在IFN-β治疗MS的疗效中发挥关键作用(图4)。
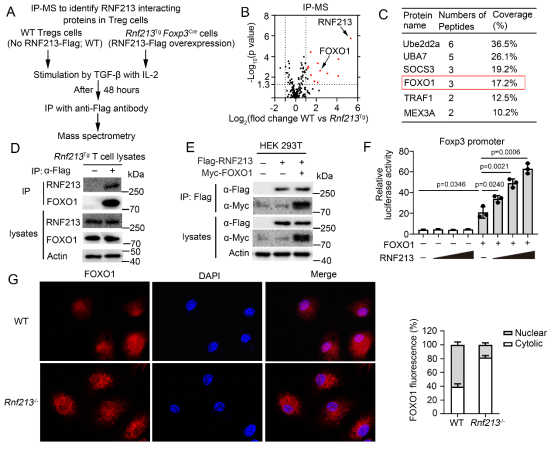
图3. RNF213与FOXO1结合并调控了FOXO1的入核
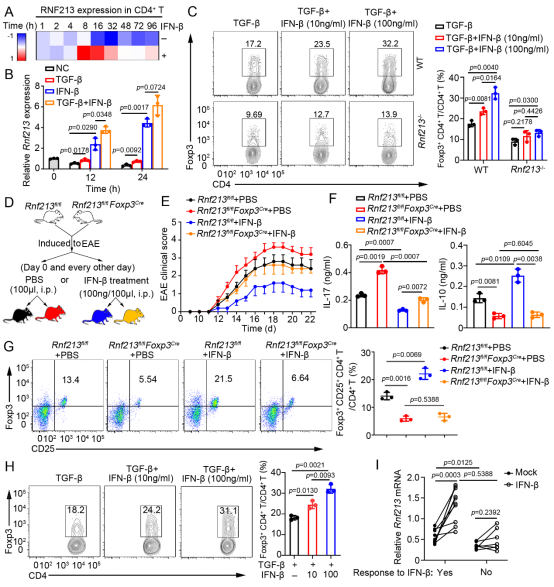
图4. IFN-β通过诱导RNF213表达促进Treg细胞分化
上述结果证明了RNF213在调节适应性免疫反应中的关键作用,有助于加深对蛋白质翻译后修饰调控CD4+ T免疫功能的理解,并提示RNF213有望成为治疗Treg细胞相关疾病的治疗靶点(图5)。
该研究由广州医科大学附属第二医院胡胜锋/广州妇女儿童医院李晓敏/广州市第一人民医院张惠丽团队合作共同完成。胡胜锋教授/李晓敏医师/张惠丽副主任医师为共同通讯作者。该研究得到了国家自然科学基金,广东省基础与应用基础研究基金,广州市基础与应用基础研究基金和中国博士后基金的支持。
原文链接:
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言
















#多发性硬化症# #E3泛素连接酶# #CD4+ T# #RNF213#
77