临床研究|PEG-IFNα-2b治疗慢性乙型肝炎患者血清HBsAg清除率的效果分析
2023-09-06 临床肝胆病杂志 临床肝胆病杂志 发表于上海
本研究旨在评价真实世界应用聚乙二醇干扰素α-2b(PEG-IFNα-2b)治疗CHB患者清除血清HBsAg的效果。
慢性乙型肝炎(CHB)是由HBV感染引起的慢性传染性疾病,是引起肝炎肝硬化、肝衰竭和肝癌的主要原因之一。规范有效的抗病毒治疗是控制疾病进展、降低HBV感染相关终末期肝病发生风险的重要手段。
近年来,多项研究证实CHB患者获得血清HBsAg清除后可使肝癌发生风险降到最低。相对于核苷(酸)类似物,由于具有直接抗病毒和免疫调节双重作用,IFNα治疗在清除血清HBsAg方面更具优势。
本研究旨在评价真实世界应用聚乙二醇干扰素α-2b(PEG-IFNα-2b)治疗CHB患者清除血清HBsAg的效果。
1 资料与方法
1.1 一般资料
纳入2017年6月—2021年1月本科诊治的CHB患者,所有患者符合《慢性乙型肝炎防治指南(2019年版) 》[1]诊断标准,且符合以下纳入标准:(1)血清HBsAg阳性,HBV DNA阳性;(2)患者临床检查结果及既往病史排除失代偿期肝硬化,包括有消化道出血、腹水、肝性脑病等并发症病史;(3)临床检查证据排除无IFNα禁忌证;(4)女性患者在治疗期间无生育要求,孕产妇不能入组;(5)签署IFN知情同意书。排除标准: 合并心肺肾等重要脏器疾病,妊娠或哺乳期妇女,合并HCV或HIV感染;临床明确诊断为肝硬化、肝癌或其他系统恶性肿瘤,合并自身免疫性、遗传性肝病或药物性肝损伤,酗酒或吸毒者。
1.2 治疗方法
给予所有患者PEG-IFNα-2b (厦门特宝生物工程股份有限公司,国药准字S20160001) 180 μg皮下注射,1次/周。
1.3 血清HBV标志物检测
使用雅培I-2000全自动免疫分析仪和Abbort公司配套Architect HBV标志物检测试剂盒检测。
2 结果
2.1 人口学资料及基线情况
共入组411例患者,男287例(69.8%),女124例(30.2%),年龄为(36.4±8.7)岁,平均病程(60.3±9.9) 个月,核苷(酸)类似物经治338例(82.2%),IFN单用106例(25.8%),IFN联合核苷(酸)类似物305例(74.2%),HBeAg阳性94例(22.9%),ALT异常108例(26.3%)。
2.2 基本疗效和血清HBsAg阴转情况
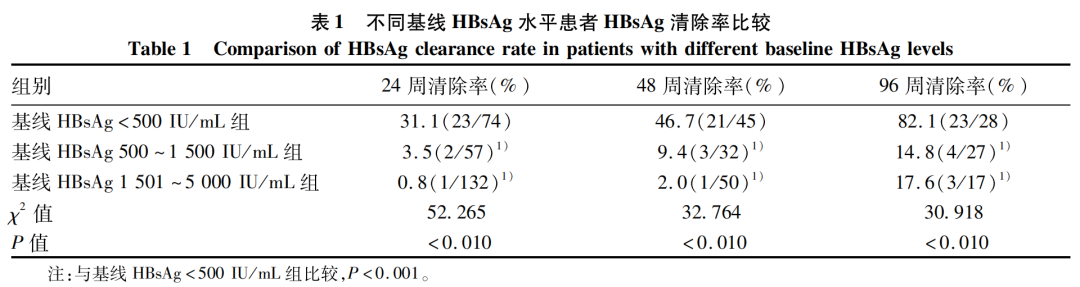
完成24周治疗患者263例,其中HBsAg转阴26例(9.9%);完成48周治疗患者127例,其中HBsAg转阴25例(19.7%);完成96周治疗患者72例(41.7%),其中HBsAg转阴30例(41.7%)。不同基线HBsAg水平患者治疗24、48及96周时HBsAg清除率比较差异均有统计学意义(P值均<0.01),随着治疗时间延长,HBsAg清除率逐渐升高,并且这种趋势有统计学意义(趋势χ2值分别为44.517、29.147、22.260,P值均<0.01)。进一步组内比较显示:随访24、48及96周时,HBsAg 500~1 500 IU/mL组和1 501~5 000 IU/mL组的HBsAg清除率较HBsAg<500 IU/mL组均明显下降(P值均<0.001)(表1)。
根据既往治疗情况(初治或经治)及治疗方案(单用或联合)对患者分组比较,仅初治与经治组在男女比例上差异有统计学意义(P=0.025),其他基线指标在初治或经治组间、单用或联合组间差异均无统计学意义(P值均>0.05)。在治疗24、48及96周时,初治或经治组间、单用或联合组间HBsAg清除率比较差异均无统计学意义(P值均>0.05)(表2)。

2.3 合并症和不良事件情况
411例CHB患者中,76例合并基础疾病,其中合并糖尿病7例(1.7%),高血压病15例(3.6%),吉尔伯特综合征27例(6.6%),低骨量47例(11.4%)。245例合并其他用药,粒细胞集落刺激因子180例(43.8%),甘草酸二胺112例(27.3%),氟哌噻吨美利曲辛87例(21.1%),氨氯地平11例(2.7%),硝苯地平4例(1.0%),二甲双胍6例(1.5%),胰岛素1例(0.2%)。主要不良事件为骨髓抑制、焦虑、失眠、乏力,167例患者出现中性粒细胞计数<2×109/L,给予粒细胞集落刺激因子治疗,11例患者因血小板计数<30×109/L,给予停药观察,87例患者出现焦虑症状,给予氟哌噻吨美利曲辛药物治疗,1例出现皮下软组织感染,给予停药观察后缓解,无进一步严重不良事件发生。
3 讨论
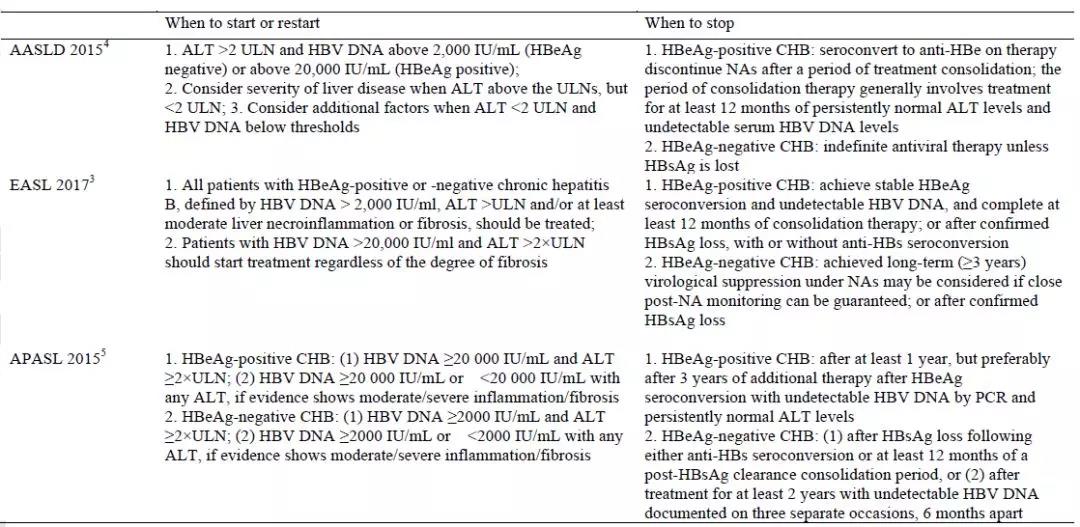
根据《2020中国卫生健康统计年鉴》[2]发布的最新数据显示,我国2019年仍然有超过100万的新发乙型肝炎患者。《慢性乙型肝炎防治指南(2019年版)》[1]中指出,我国慢性HBV感染者约7 000万例,其中CHB患者为2 000万~ 3 000万例。2020年最新数据[3]显示,2020年中国新发肝癌病例数为410 038例,因肝癌死亡人数为391 152例,而我国肝癌由HBV感染引起的比例高达92.05%。2015年《慢性乙型肝炎防治指南》[4]同国际接轨,将CHB的治疗终点分为基本终点(HBV DNA转阴)、满意终点(HBeAg血清学转换)及理想终点(HBsAg清除)。随着治疗目标的逐步实现,CHB患者的5年肝癌累积发生率逐步递减,从获得基本终点的3.6%~11.4%[5-7], 下降到获得满意终点的<2.58%[8],再到获得理想终点的仅1%左右[9-12]。
目前我国最新CHB防治指南也积极推荐为对于部分适合条件的患者,应追求临床治愈,即功能性治愈或称为临床治愈[2]。虽然目前CHB仍然不能完全治愈,但通过实现HBsAg转阴大大改善了患者远期结局。HBsAg清除成为CHB患者追求的主要目标及各项研究的主要疗效指标,且HBsAg被认为是共价闭合环状DNA转录活性的替代标志物,同时也是HBV感染肝细胞的标志物[13]。研究发现根据CHB患者早期HBsAg应答情况,可更好地预测临床治愈情况。
近期北京地坛医院的相关研究[14]发现24周HBsAg水平对临床治愈率的预测能力显著优于12周。2017年《聚乙二醇干扰素α治疗慢性乙型肝炎专家共识》[15]及《慢性乙型肝炎临床治愈(功能性治愈)专家共识》[16]中均采用了24周HBsAg水平来决策后续治疗。
相比核苷(酸)类似物,PEG-IFN具有直接抗病毒作用和免疫调节双重作用, 更容易使部分患者达到临床治愈。为实现这一目标,国内外专家对临床治愈的优化治疗方案的探索已经持续了10余年,研究发现以PEG-IFNα为基础的抗病毒治疗更容易实现临床治愈的目标。相比PEG-IFNα-2a,国内新药PEG-IFNα-2b(Y型, 40 kD) 采用新型Y型分支聚乙二醇分子,选择性修饰IFNα-2b 134位赖氨酸,在治疗HBeAg阳性CHB患者的方案中具有相当的疗效和安全性[17]。另一方面,优势患者的治疗策略在获得临床治愈方面随着循证医学证据的不断累积逐渐受到专家的认可和验证,OSST、S-C、NEW SWITCH等研究[18-21]证实了优势患者采用基于PEG-IFNα治疗后可获得30%~80%的临床治愈率。优势患者为HBsAg水平较低,和/或HBeAg、HBV DNA水平低,且在治疗过程中HBsAg指标下降幅度较大的患者。本研究中基线HBsAg<500 IU/mL患者在治疗同期的HBsAg清除率明显高于其他两组,可作为优势人群的分界点。对于HBsAg水平极低的非活动性HBsAg携带者接受短期的PEG-IFNα-2b治疗可获得高达93.8%的HBsAg清除率[22]。
一项随机对照研究[23]显示,与PEG-IFNα-2b单药相比,恩替卡韦和PEG-IFNα-2b联合治疗病毒学应答率更高,然而HBsAg阴转率两组间差异无统计学意义(9.5% vs 4.8%)。另一项荟萃分析[24]显示, 与核苷(酸)类似物单药治疗相比, 初始联合核苷(酸)类似物治疗HBsAg清除率显著升高,但与PEG-IFNα单药相比, 联合治疗没有显著升高HBsAg清除率。本研究中24、48及96周随访患者中IFN单用和联用并无统计学差异。本随访研究中完成96周治疗患者72例,其中HBsAg转阴30例(41.7%)。本研究发现HBsAg基线水平越低,在24、48及96周随访患者的HBsAg清除率越高,随着治疗时间的延长这种趋势有统计学意义(P值均<0.01)。因此对于48周未获得HBsAg清除的患者,除了依据HBsAg水平预测患者阴转率之外,可根据患者情况来适当延长PEG-IFNα疗程,但具体的cut-off值还未达成共识,而对于决定停药的这部分患者,如何来进一步追求临床治愈,这都是今后需要探索的重要研究方向。来自加拿大的最新研究[25]发现,IFNα治疗HBeAg阳性CHB患者21周(中位)可获得16.9%的HBsAg清除率,且IFNα治疗后随访10年的累积HBsAg清除率达32%,另外,也证实了HBeAg清除和HBsAg清除可显著改善CHB患者的长期临床结局。
另外在治疗过程中要关注IFN相关不良反应的出现及处理,其中最常见不良事件包括流感样症状、焦虑、骨髓抑制等,以轻度为主,及时给予对症药物治疗。尤其是对于合并肝硬化患者需密切观察。
对于PEG-IFNα序贯/联合治疗优势患者的研究和理念一直在推进和深入,CHB患者应积极采取有效的抗病毒治疗方案,追求临床治愈,降低肝癌发生风险,争取最大获益。对于相关各项检测指标的分层细化,需要进一步长期随访数据,将会使得治疗疗程更加明确化。
全文下载
李宽, 宁会彬, 靳慧鸣, 等. 聚乙二醇干扰素α-2b治疗慢性乙型肝炎患者血清HBsAg清除率的效果分析[J]. 临床肝胆病杂志, 2023, 39(8): 1819-1824
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言