Adv Drug Deliv Rev:核酸突变分析方法抉择: PCR、杂交、NGS?
2016-10-22 佚名 生物谷
日前,以"精细管理、精准医疗"为主题的2016届CSCO学术年会在厦门落下帷幕,精准检测作为临床实践中实施精准医学的第一步,成为本届CSCO学术年会的热点话题。来自不同企业的分子诊断技术百花齐放百家争鸣,面对新技术与成熟技术的较量,在"精准医学"时代下,如何选择合适的检测技术,实现精准治疗成为新医学形态下人们亟需解决的问题。 近期,美国莱斯大学DmitriyKhodakov教授在

日前,以"精细管理、精准医疗"为主题的2016届CSCO学术年会在厦门落下帷幕,精准检测作为临床实践中实施精准医学的第一步,成为本届CSCO学术年会的热点话题。来自不同企业的分子诊断技术百花齐放百家争鸣,面对新技术与成熟技术的较量,在"精准医学"时代下,如何选择合适的检测技术,实现精准治疗成为新医学形态下人们亟需解决的问题。
近期,美国莱斯大学DmitriyKhodakov教授在国际知名期刊《Advanced Drug Delivery Reviews》(IF=15.606)发表的综述文章,也许能给我们一个答案。该文对精准医学关键的基因检测技术手段进行了梳理,作者认为目前实现临床转化的核酸检测技术可以分为三大类:PCR技术、杂交技术和测序技术,介绍了这三类技术,并对其临床应用发表了自己的见解。以下是对该文主要内容的介绍。
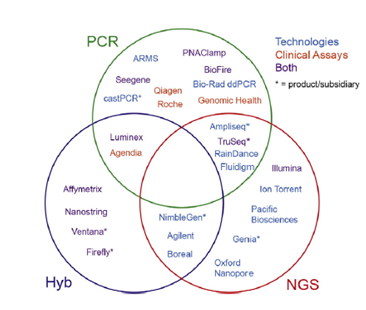
一、PCR技术
PCR技术是目前应用最广泛的DNA分子检测技术。与杂交技术和测序技术相比,PCR技术优势主要在于、高敏感度、易于推广。其主要局限在于多重基因联合检测时可涵盖的基因数量受限。
1、ARMS
扩增阻滞突变系统(ARMS)是使用广泛的一种核酸变异检测技术,已有多家公司开发出基于此技术的肿瘤突变基因检测试剂盒产品,如Qiagentherascreen、Roche Cobas、BiomerieuxTHxID以及中国的AmoyDx等。
2、Blocker PCR
Blocker PCR技术通过引入blocker序列来抑制野生型基因扩增从而达到检测核酸变异位点的目的。目前已有基于此技术的肿瘤基因突变检测试剂盒产品问世,如PNA Bio开发的PNAClamp试剂盒。
3、多重PCR
多重PCR技术需要解决扩增抑制、荧光基团的数量限制、引物二聚体等问题,其工程学解决方案主要通过开发设备和一次性芯片等来解决。Biofire Diagnostics(现被Biomerieux收购)和Cepheid都开发出用于感染性疾病诊断的多重PCR试剂和仪器。
4、数字PCR
数字PCR技术通过将一个样本分配到不同的反应单元,每个单元包含一个或多个拷贝的目标分子(DNA模板),在每个反应单元中分别对目标分子进行PCR扩增,扩增结束后对各个反应单元的荧光信号进行统计学分析,从而实现高灵敏的绝对定量检测。目前数字PCR主要用于科研及临床研究,也有开发LDT方法用于临床,如Trovagene PCMBRAFV600E试验。
二、杂交
杂交是一种将合成的DNA探针或引物与目标序列结合的过程。与PCR技术和NGS技术相比,杂交的主要优点在于操作简单、可多重检测、结果可靠,其缺点主要在于该方法不能进行序列扩增,因此必须依赖于信号放大技术或者高灵敏的检测设备。
1、微矩阵
微矩阵通过靶基因与固定在芯片上的探针发生特异性杂交,结合在芯片上不同位置的探针对应不同突变,荧光强度代表浓度,从而实现一次检测多种基因突变或者基因表达水平的目的。因此,其检测灵敏度取决于靶基因和探针的杂交效率及荧光显微镜的分辩能力。FDA已批准多个微矩阵技术产品,如Agendia开发的用于乳腺癌检测的MammaPrint试剂盒等。
2、荧光条形码单分子检测技术
荧光条形码单分子检测技术是一种高通量检测技术。可分为两大类:intensity barcodes和geometric barcodes,intensity barcodes在二氧化硅颗粒上标记不同密度的荧光标记,通过捕获有目标基因的颗粒的荧光信号来检测突变类型;而geometric barcodes是利用光谱上不同的荧光基团的组合来检测不同序列。其中Luminex开发的基于intensity barcodes方法的呼吸道疾病诊断技术已获得FDA批准。
3、原位杂交(ISH)
原位杂交不仅提供目标基因的序列和浓度信息,而且可实现目标基因的细胞定位,尤其适用于异质性细胞及组织样本的基因扩增检测。原位杂交技术有荧光原位杂交(FISH)、显色原位杂交(CISH)或者银染原位杂交(SISH)等,原位杂交技术可应用于DNA和RNA的检测,目前,FISH主要用于DNA扩增检测,如Roche和Abbot开发的HER2扩增检测试剂盒。
三、新一代测序技术(NGS)
NGS是一种高通量检测DNA和RNA变异的方法,与Sanger测序不同,NGS可检测多种样本,且可以同步提供大量的基因变异信息,因此该方法非常适合于并行检测和分析多种基因和变异信息。
没有一种方法是完美的,由于背景信号干扰、酶的扩增错误率、化学反应不彻底等问题,所有的NGS平台都有一定的内在错误率。而测序过程中的错误会增加突变检测的难度,特别是低频突变。
1、主流NGS平台
主流NGS平台有Illumina和IonTorrent的的NGS系统,Illumina在序列错误率和成本控制上处于领先地位。在诊断应用方面,Illumina开发有Miseq和NextSeq两个平台,其中MiseqDx是首个获得FDA许可用于IVD的NGS平台。
2、其他平台
其他平台还有:适用于长序列检测的SMRT NGS平台(Pacific Bioscience),以及Nanopores NGS平台(Oxford、Genia Technologies)等。
四、作者观点
NGS实验操作复杂且成本高,由于其高通量的序列分析能力,已经成为许多序列变异分析与科研应用的主要选择。然而,从临床诊断应用的角度,检测的目标位点必须具有明确的临床价值,因此相对于NGS技术而言,PCR技术的简便性、稳定性和使用的广泛程度意味着在未来一段时间内PCR技术依然是核酸突变位点检测的不二选择。
在可预见的未来里,技术的发展将扮演重要的角色。虽然NGS技术单位通量价格在近10年极大地降低,但是依然离整个基因组或转录水平的全面深度测序至少6个数量级的差距。DNA序列变异分析的优化和创新将主要集中在价格,准确性,运行周期,操作复杂度和实验室的规范化等方面。
原始出处
Khodakov D1, Wang C1, Zhang DY2.Diagnostics based on nucleic acid sequence variant profiling: PCR, hybridization, and NGS approaches.Adv Drug Deliv Rev. 2016 Oct 1
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#Drug#
65
#NGS#
61
#PCR#
74