Nature:铜催化细胞状态变化!或为新靶点?
2023-05-12 BioMed科技 BioMed科技 发表于上海
一种天然产物被报道可选择性地杀死癌症干细胞,在之前的作用机制研究中,研究者确定铁是其靶点。
细胞如何对环境中的物理和化学变化作出快速反应?虽然基因突变可导致细胞特性发生变化,但非遗传机制可驱动快速适应,这一现象被广泛称为细胞可塑性。细胞可塑性与健康和疾病的基本生物学过程有关。例如,肿瘤细胞可以从高度增殖状态转变为更具侵袭性的状态,从而导致癌症转移。在炎症过程中,免疫细胞可以转化为执行炎症反应和促进组织修复的细胞。在失调的炎症中,这些转化会出错,导致组织损伤。调节免疫细胞活化和驱动炎症的分子机制尚不完全清楚。是否存在可用于治疗干预的主要炎症调节因子?

近期Nature发表评论文章“Copper catalyses changes in cell state”称,一种天然产物被报道可选择性地杀死癌症干细胞,在之前的作用机制研究中,研究者确定铁是其靶点。这导致研究者发现,铁摄取在这些细胞中上调,并驱动癌症细胞的可塑性,在表观遗传水平发挥作用,即通过在不影响DNA序列的情况下影响基因表达。相关研究被法国巴黎PSL研究型大学居里研究所Raphaël Rodriguez教授以“A druggable copper-signalling pathway that drives inflammation”发表在《Nature》。

在这些细胞中,研究者还发现细胞膜蛋白CD44(透明质酸分子的主要受体)调节铁结合的透明质酸的摄取。这促使研究者寻找控制免疫细胞可塑性的类似分子机制。在这项研究中,研究者使用一种称为质谱的技术分析了巨噬细胞活化前后的金属含量。这表明活化的炎症巨噬细胞中铜和铁增加,这些增加主要由CD44和透明质酸介导。进一步的研究没有发现已知的铜依赖酶在炎症巨噬细胞中上调。这表明在活化的巨噬细胞中存在一种化学反应的铜离子池。研究者发现,称为线粒体的细胞器中的铜(II)离子直接催化称为NADH的代谢分子被过氧化氢氧化,从而产生NAD+离子(图1)。这驱动了作为免疫细胞激活基础的代谢和表观遗传编程。值得注意的是,研究者发现用于治疗2型糖尿病的药物二甲双胍可能会干扰巨噬细胞的活化,这可能是因为二甲双胍与线粒体中的铜离子结合,阻止它们催化NADH的氧化。利用热力学原理,研究者设计了一种二甲双胍分子二聚体,称为LCC-12(也称为二甲双胍),它在与铜结合和灭活线粒体中铜(ii)介导的催化方面甚至比二甲双胍更好。值得注意的是,LCC-12促进了急性炎症动物模型的生存。这些结果验证了生物学中的一个关键概念,即细胞可塑性的药理学控制可以带来治疗益处。
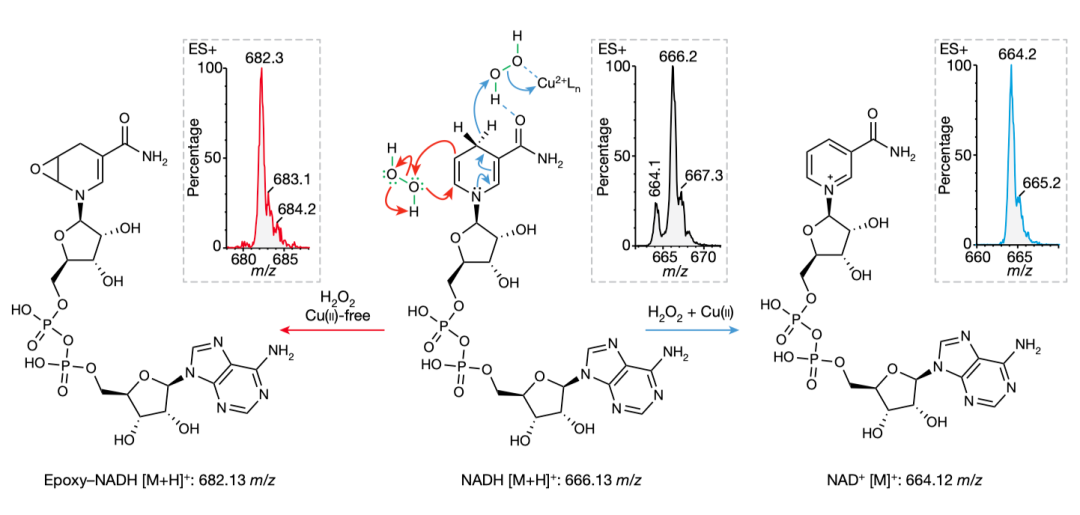
图1. 铜离子调节炎症的代谢程序
研究者发现了调控细胞可塑性的一般铜信号通路。这一途径与长期以来已知的铜离子作为变构辅因子的作用形成了对比:与蛋白质结合以改变其功能的分子或粒子。该研究显示了这一机制在各种疾病相关环境(如癌症和炎症)中的广泛相关性。它还阐明了炎症和癌症这两种明显不同的生物学问题共同的信号通路,从而提出了一个问题,即依赖于细胞可塑性的其他生物过程(包括正常发育、伤口愈合和衰老)是否也发生类似的事件分子链。研究者最初建立的治疗策略可能广泛适用于炎症的治疗,但涉及急性炎症的生物学过程很复杂。现在需要进一步的研究来确定这一铜信号通路是否可以作为临床治疗的靶点。
【小结】
Nature杂志高级编辑乔治·卡普塔称金属对细胞的功能至关重要。随着研究者对镁和铁等金属的生物学了解的越来越多,焦点已经转移到其他金属在关键细胞过程中的作用问题上。这项工作的新颖之处在于,它为铜的细胞作用及其调控提供了一个框架,这可以在无数其他细胞类型中进行研究。
原文链接:
https://www.nature.com/articles/d41586-023-01330-4
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言







