Blood:靶向VWF可预防创伤性脑损伤诱导性凝血病
2020-08-13 MedSci原创 MedSci原创
在急性TBI时释放的VWF在将细胞外囊泡介导至活性内皮细胞和血小板方面具有高粘附力。重组VWF A2结构域通过选择性阻断超粘附VWF的暴露的A1结构域来预防TBI诱发的凝血病。
创伤性脑损伤诱导性凝血病(TBI-IC)可导致危及生命的继发性颅内出血。现在只知道其发病机理与颅外损伤和失血性休克引起的凝血病的机理不同,但确切的发生机制仍不明确。
在该研究中,研究人员汇报了验证“急性TBI期间释放的von Willebrand因子(VWF)在本质上是高粘附性的,因其血小板结合A1结构域已暴露,可促进TBI诱导的血管渗漏和消耗性凝血病”这一假设的研究结果。
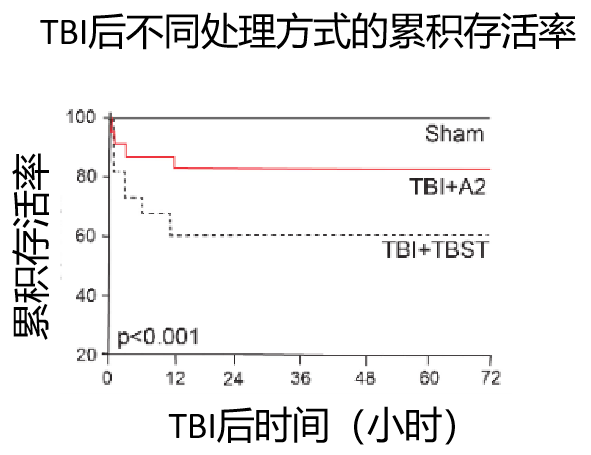
这种高黏附性的VWF可通过VWF A2结构域蛋白被选择性地阻断,以预防TBI-IC,改善神经功能,将出血风险降至最低。研究人员证实,通过腹膜内注射或静脉内输注给予A2结构域蛋白可使TBI诱导性死亡减少50%以上,并可显著改善遭受重度侧向液击伤的C57BL/6J雄性小鼠的神经功能。
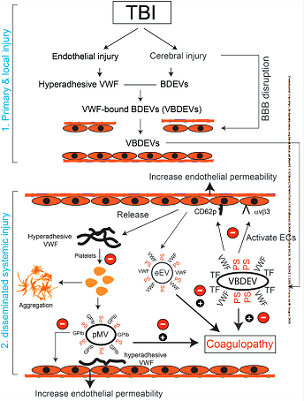
A2结构域蛋白保护内皮细胞免受细胞外小泡诱导的损伤,减少TBI诱导的血小板活化和微囊泡,从而预防TBI诱导的高凝状态。A2结构域蛋白是通过特异地阻断急性TBI期间释放的高粘附性VWF上暴露的A1结构域来实现此治疗功效。
综上所述,该研究结果表明VWF在TBI-IC的发展中具有因果作用,是TBI的这种危及生命的并发症的治疗靶点。
原始出处:
Xin Xu,et al. Conformation-Dependent Blockage of Activated VWF Improved Outcomes of Traumatic Brain Injury in Mice. Blood. August 4,2020.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#诱导性#
64
#创伤性#
58
未来必定成为靶向治疗的天下
117
#创伤#
44
#vWF#
66
#损伤#
67