Science:趋化因子CXCL13背锅,衰老引起轴突再生能力钝化
2022-05-28 周科 “神经周K”公众号
已有研究表明星形胶质细胞和背根神经节(DRG)神经元来源的CXCL13调控疼痛。生理状态下中枢神经系统几乎不产生CXCL13,但在自身免疫性脱髓鞘和原发性中枢神经系统淋巴瘤等病理状态下大脑和脊髓的CX
趋化因子CXCL13 通常在淋巴器官中表达,调控B 细胞和抗原呈递细胞的募集。CXCL13的受体为CXCR5,高度表达在B细胞,可被募集到CXCL13高表达的区域。
已有研究表明星形胶质细胞和背根神经节(DRG)神经元来源的CXCL13调控疼痛。生理状态下中枢神经系统几乎不产生CXCL13,但在自身免疫性脱髓鞘和原发性中枢神经系统淋巴瘤等病理状态下大脑和脊髓的CXCL13表达增加。

2022年5月13日帝国理工学院脑科学系Simone Di Giovanni研究团队揭示了神经元CXCL13- T细胞CXCR5信号介导衰老相关的轴突再生能力减弱。
1
衰老后神经元Cxcl13升高促进CXCR5阳性T细胞募集
研究人员对坐骨神经损伤的年轻小鼠和老年小鼠的DRG组织进行单细胞测序,发现老年小鼠差异性基因表达数量最多,主要为T细胞和细胞因子/趋化因子信号相关的基因。
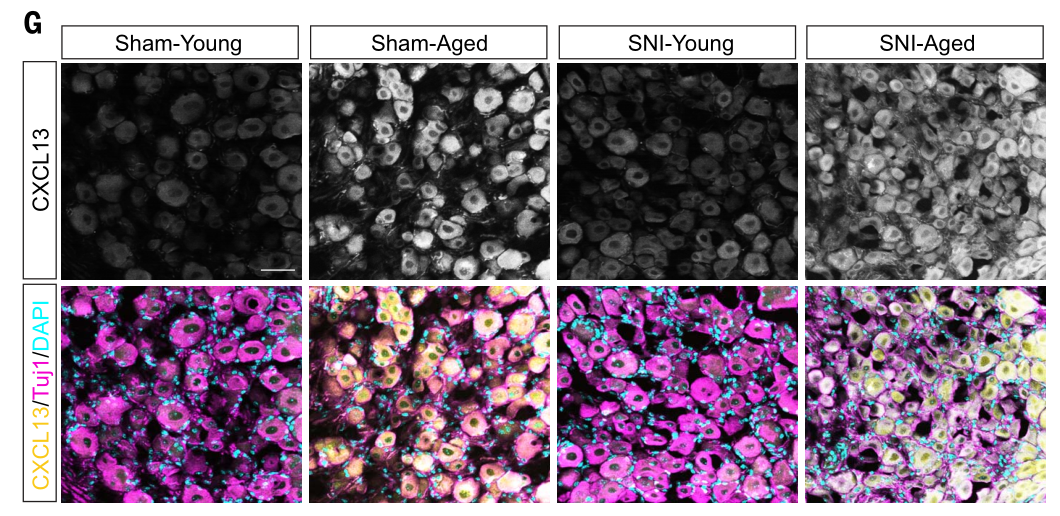
图1:Cxcl13在年轻和老年小鼠中的表达
更进一步来说,Cxcl13是老年小鼠坐骨神经损伤后上调表达最为显着的基因,其受体CXCR5表达也上调。与此同时坐骨神经损伤后老年小鼠DRG 区域CXCR5阳性B细胞和CXCR5/CD8双阳性T细胞数量明显增多。
即便未经历坐骨神经损伤,老年小鼠CXCR5/CD8双阳性T细胞也增多(与年轻小鼠相比)。
在神经损伤之前清除老年小鼠DRG 区域CXCR5/CD8双阳性T细胞能够改善老年小鼠轴突再生能力,而清除CXCR5阳性B细胞并不会发挥改善轴突再生的作用。这就表明CXCR5/CD8双阳性T细胞介导衰老相关的轴突再生能力减弱。
Rag2敲除小鼠缺乏成熟的T、B、NK细胞,巨噬细胞吞噬功能受抑制,为免疫缺陷程度较高的工具鼠。与老年野生型小鼠相比,老年Rag2敲除小鼠轴突再生能力更强一些。将CXCR5+CD8+ 双阳性T细胞分别移植到坐骨神经损伤后的年轻和老年 Rag2敲除小鼠中出现不同的结果。
具体表现为年轻Rag2敲除小鼠脾脏CXCR5+CD8+ 双阳性T细胞数量和CX3CL13水平明显高于DRG,轴突再生能力并未发生变化,而与之相反的是老年Rag2敲除小鼠DRG区域CXCR5+CD8+ 双阳性T细胞数量和CX3CL13水平明显高于脾脏,轴突再生能力减弱。
此外老年 Rag2敲除小鼠在接受敲除CXCR5的CD8+ 阳性T细胞移植后,其募集到脾脏和DRG区域数量均明显减少,并在一定程度上增强轴突再生能力。这些结果表明CXCR5+CD8+ 双阳性T细胞驱动衰老相关的轴突再生能力减弱。
2
转录因子Nfκb2驱动衰老相关的Cxcl13表达
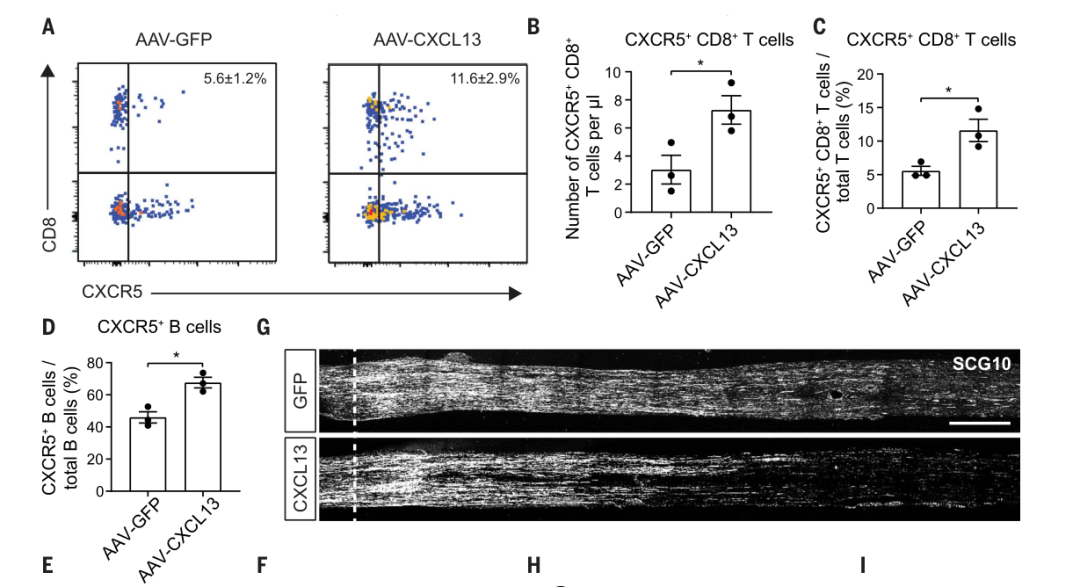
图2:过表达Cxcl13引起年轻小鼠轴突再生能力障碍
研究人员通过病毒工具特异性过表达年轻小鼠DRG神经元Cxcl13后促进CXCR5阳性B细胞和CXCR5/CD8双阳性T细胞的募集,轴突再生能力也减弱,能够模拟出衰老表型。此外,神经损伤老年小鼠在接受Cxcl13阻断后轴突再生能力增强,促进感觉功能恢复。
为进一步探究衰老进程中Cxcl13水平升高的分子机制,研究人员对可促进Cxcl13表达的转录因子Hif1a,Pou5f1, Rar, Nfkb, and Sp1等转录因子进行检测,发现老年小鼠DRG区域只有Nfκb2表达上调。
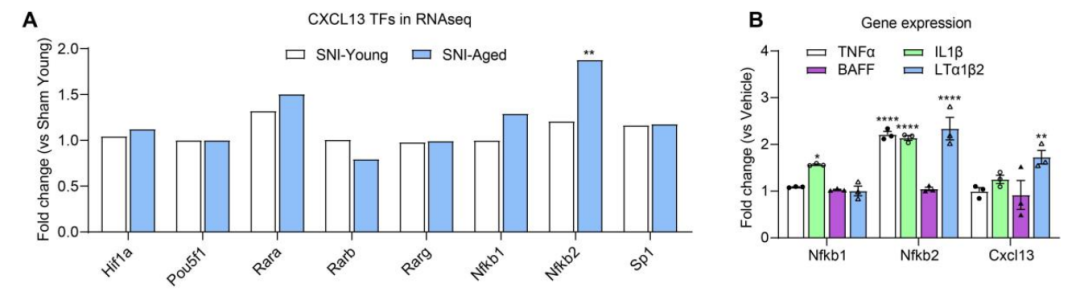
离体细胞实验发现经典的NF-κB激活剂肿瘤坏死因子-α或白细胞介素-1β可上调Nfκb2,但不能上调表达Cxcl13。而只有淋巴毒素LTα1β2上调Nfκb2的同时促进Cxcl13表达。抑制NF-κB酶活性后能够降低老年小鼠Cxcl13表达,这些结果表明Nfκb2调控衰老相关的Cxcl13表达。
总的来说,本文揭示了衰老进程中DRG神经元Cxcl13表达升高,进一步募集更多的CXCR5+CD8+ 双阳性T细胞,抑制轴突再生信号通路,损害轴突再生能力。
原始出处:
LUMING ZHOU, et al. Reversible CD8 T cell–neuron cross-talk causes aging-dependent neuronal regenerative decline. SCIENCE, 13 May 2022, Vol 376, Issue 6594.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#再生能力#
87
#CXCL1#
65
#CXCL13#
52
#轴突再生#
64
#SCIE#
56
#趋化因子#
66
#衰老#
96