有种病毒很狡猾,当你身体无恙时它在冬眠,当你免疫力下降的时候它就趁虚而入,在皮肤、口腔和眼睛等部位引起水泡、溃疡等伴有剧痛的症状。而这一切都是由单纯疱疹病毒(HSV)所引起的,包括1型(HSV-1)和2型(HSV-2)两种。HSV-1可以通过看起来完全正常的口腔或皮肤传播,传播之后也基本不会引起不适的症状,而是会在周围神经系统的神经细胞中蛰伏;HSV-2则主要通过性传播,隐居在生殖道中。
据世界卫生组织官网数据显示,HSV-1已经潜伏在全世界近70%的人体内,其中50岁以下人群的感染人数在2016年就达到了37亿。更令人无奈的是,疱疹病毒会在宿主外周神经系统中终身潜伏,永远无法根除。
HSV究竟是何方神圣?为何传播范围可以如此之广呢?《Nature》最近刊发的文章“Herpesviruses assimilatekinesin to produce motorized viral particles”为我们揭开了HSV的神秘面纱,揭示了该病毒进化出的分子机制,为开发预防针对单纯疱疹病毒1型(HSV-1)和2型(HSV-2)的疫苗开辟了道路。

参与该研究的Greg Smith教授指出,病毒感染的终极目标其实就是无限扩增并且不断扩大感染范围,达到这一目标的首要条件是抵达细胞核,而这一过程又离不开细胞内微管的参与。微管是细胞中存在的纤维结构,可以输送物质并维持细胞形态。
光有微管这条铁轨还不够,病毒们还需要列车轨道上的引擎——驱动蛋白和动力蛋白。HSV-1能编码一种特殊的蛋白pUL36,它能结合动力蛋白,并在初始感染期间促进病毒颗粒向细胞内转运。比如流感病毒在侵入上皮细胞后,就会带上这两个蛋白,来回地在微管上移动,直到接近细胞核的时候就入侵进去。
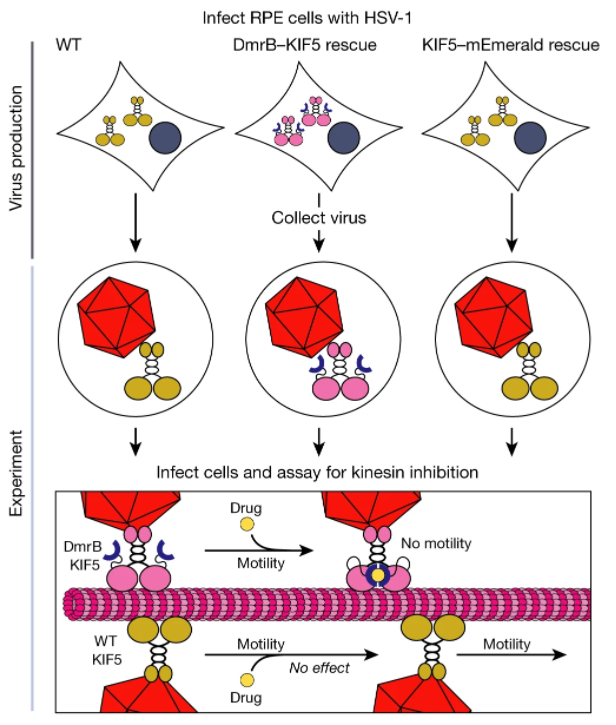
病毒捕获的驱动蛋白将衣壳运输到细胞核
但是研究发现pUL36的双向运输和外周积累除了表明 PRV 蛋白会结合动力蛋白外,还招募了一个“重要合伙人”——驱动蛋白。在相关实验中也直接证实了驱动蛋白存在的必要性:在病毒体产生和随后的感染过程中都没有驱动蛋白时,虽然产生了大量病毒粒子,但病毒颗粒多数会在中心体积聚,衣壳从中心体到细胞核的运输明显受损,因此这些病毒粒子传播感染的能力较弱。
综上所述,协助HSV感染的细胞蛋白分工明确。动力蛋白是将HSV-1从神经轴突末端带到神经元中心,而驱动蛋白则是带着病毒颗粒走向细胞核。
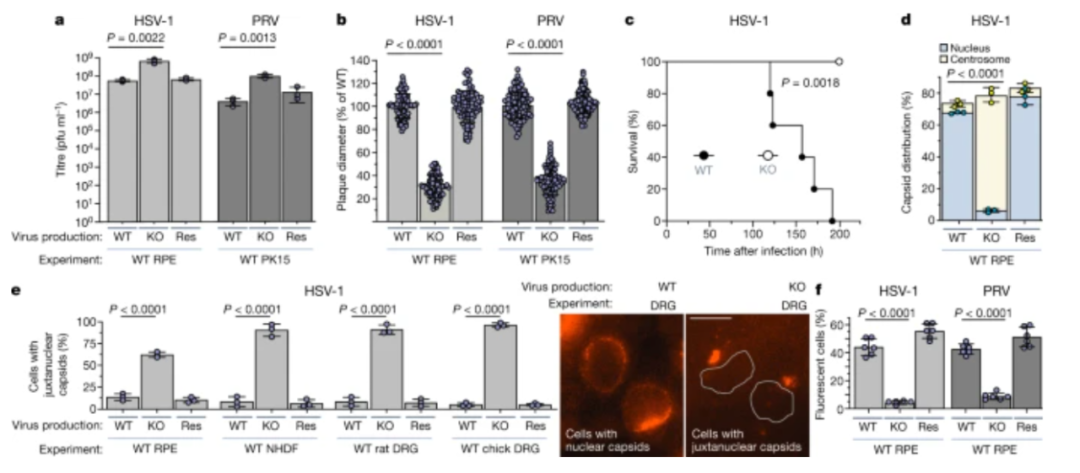
病毒组装期间驱动蛋白-1 的存在促进了随后感染期间衣壳向细胞核的运输
值得注意的是,驱动蛋白源自先前感染的上皮细胞而不是神经元内源性细胞,而被疱疹病毒pUL36蛋白“同化”的驱动蛋白通过将病毒颗粒从中心体穿梭到细胞核来促进所有细胞的感染。如此一来,HSV的传染可谓是如虎添翼,看似低调的HSV做起事来却一点也不低调。
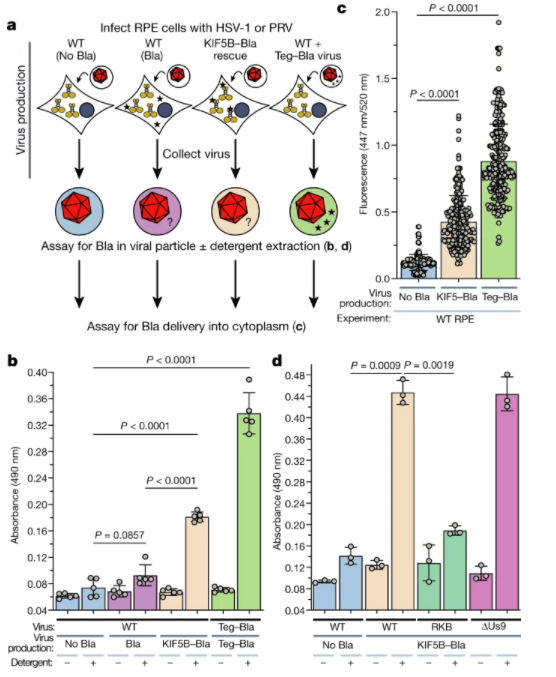
驱动蛋白被病毒颗粒捕获并传递给其他细胞
“这是首次发现病毒会利用细胞蛋白来完成一轮又一轮的感染,它们看起来是目前演化得最成功的病原体之一,”主要研究者Caitlin Prgg博士表示,“通过此次研究了解HSV病毒是如何实现这一令人难以置信的操作后,我们现在可以考虑如何夺走它们入侵神经系统的能力。这对于研究其他病毒性感染以及开发相关预防性疫苗可以提供新的思路和方向。”
参考资料:
[1]https://doi.org/10.1038/s41586-021-04106-w
[2]https://zhuanlan.zhihu.com/p/434679338
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#Nat#
74
#疱疹#
105
学习了
118