PNAS:让T细胞“喝红酒”,帮助其更好地消灭癌细胞
2021-08-22 “生物世界”公众号 “生物世界”公众号
2021年8月18日,叶海峰团队在《美国科学院院刊》PNAS上发表了题为:Engineering genetic devices for in vivo control of therapeutic
2019年10月24日,华东师范大学生命科学学院叶海峰团队在 Science 子刊 Science Translational Medicine 发表封面论文,提出了一种“喝绿茶治疗糖尿病”的新型方法。
当人体植入某种定制化细胞后,人们只需通过饮用特制的浓缩绿茶,便可使其在体内产生代谢物原儿茶酸进而控制细胞中目的基因的表达。而这种目的基因可按照需求调整改变,可以变为提高人体免疫力的抗体,也变为清除体内有害分子的酶,还可以变为降低血糖的胰岛素。
如今,这项研究有了续集——“喝红酒”治癌症。
2021年8月18日,叶海峰团队在《美国科学院院刊》PNAS上发表了题为:Engineering genetic devices for in vivo control of therapeutic Tcell activity triggered by the dietary molecule resveratrol 的研究论文。
研究团队经过六年半科研攻关,成功开发出了一种红酒成分白藜芦醇调控转基因表达的控制系统,并利用该系统调控T细胞以提高肿瘤免疫治疗的安全性。
叶海峰研究员强调:“‘喝红酒’是通俗的说法,其实我们利用的是红酒中的有效成分白藜芦醇。在我们的设计中,白藜芦醇就像‘按开关的手’,能够决定T细胞去不去围攻肿瘤细胞。”

华东师大生命科学学院2016级博士生杨林凤(已毕业)为该论文的第一作者,叶海峰教授为该论文的通讯作者。
为CAR-T细胞装上“按开关的手”
嵌合抗原受体T细胞疗法(CAR-T疗法)作为一种新兴的肿瘤免疫精准疗法,发展极其迅速,被普遍认为是人类最有潜力攻克癌症的疗法之一。2012年,CAR-T疗法成功治愈了一位名叫Emily的晚期白血病患者的案例更是点燃了全世界科学家探索CAR-T疗法和推广其临床应用的热情。
随着CAR-T疗法临床研究的深入,CAR-T疗法带来的副作用却让人始料未及,例如CAR-T疗法引发的细胞因子风暴严重影响了该疗法的安全性,限制了其临床推广。目前解决细胞因子风暴最有力的策略是控制CAR-T细胞活性,而如何安全、精准控制其活性是全球科学家共同面临的挑战。
在临床治疗中,虽然该类CAR-T细胞回输至体内后可快速识别并杀伤肿瘤细胞,但T细胞快速且剧烈的响应过程会引发大量细胞因子的释放,会导致细胞因子风暴、肿瘤溶解综合征等致命副作用。因此,如何在体内调控CAR-T细胞这一“活体药物”成为了当前肿瘤免疫治疗的重点和难点。
以此临床问题为导向,叶海峰团队构建了一种保健口服药白藜芦醇调控转基因表达的转录调控系统(ON/OFF),并将其用于可控的肿瘤免疫治疗,旨在实现CAR-T疗法的可控性。(注:研究中口服或注射用的白藜芦醇为化学制剂,并不是通过红酒给予的。)
白藜芦醇“开关”如何实现?
白藜芦醇(Resveratrol, RES)是一种有益于人类健康的非黄酮类多酚化合物,在葡萄、花生、虎杖等植物中普遍存在,具有抗氧化、抗炎、抗癌及心血管保护等作用,已被广泛用于保健品、化妆品、饮料、食品等领域。
鉴于白藜芦醇的安全性和有益性,研究团队设计构建了由白藜芦醇调控的转基因表达系统,通过白藜芦醇调控T细胞中CAR的表达(ON)与抑制(OFF),从而实现可控的CAR-T细胞免疫治疗(见图1)。
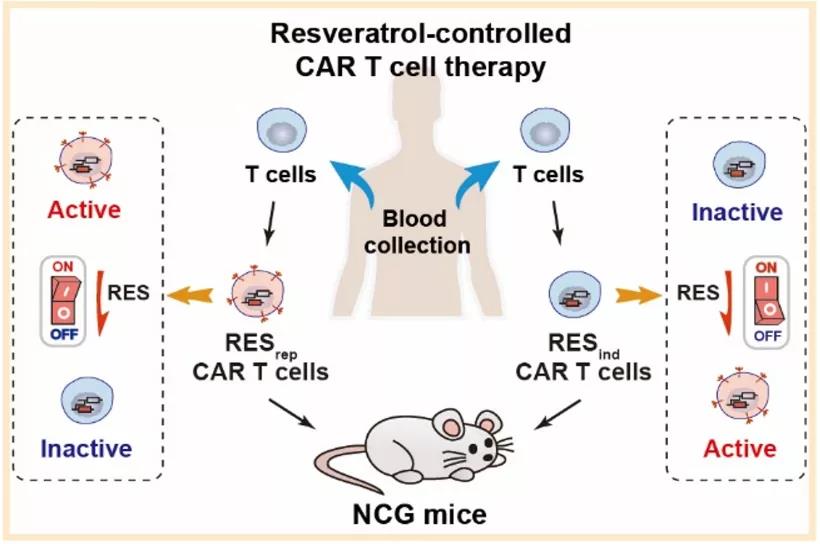
图1 白藜芦醇调控系统在CAR-T肿瘤免疫治疗中的应用
白藜芦醇调控转基因表达系统的构建
研究人员首先将来自于一种恶臭假单胞菌(Pseudomonas putida)中响应白藜芦醇的转录阻遏蛋白TtgR、TtgR特异识别的操纵子DNA序列OTtgR和转录抑制子(KRAB)/激活子(VPR)等生物功能元器件进行理性设计、组装和重编程,分别构建了白藜芦醇调控转基因表达的抑制系统(RESrep device)和诱导系统(RESind device)(见图2)。通过元件优化,最终分别获得了灵敏度高、诱导倍数高的基因表达抑制系统和诱导系统,并在哺乳动物细胞及小鼠体内均证实了优异的基因表达调控效果。
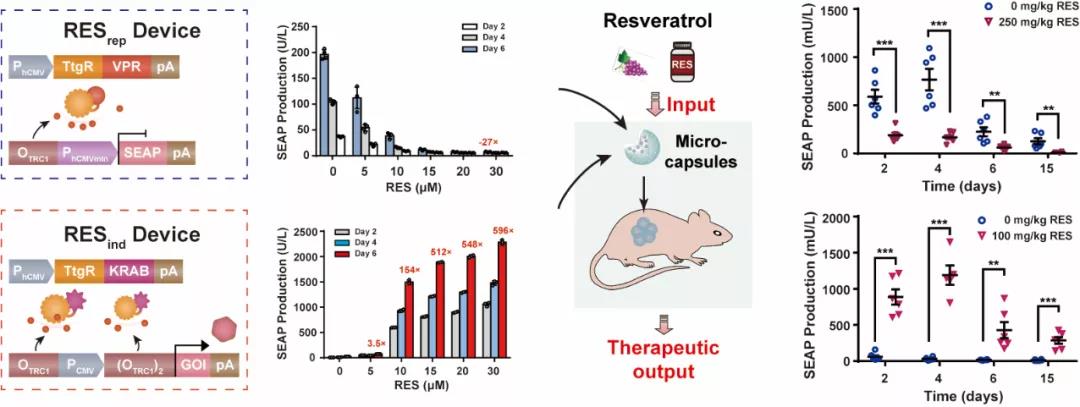
图2 白藜芦醇调控的抑制系统和诱导系统设计原理图以及在HEK293T细胞中的基因表达调控效果
白藜芦醇抑制CAR表达控制系统(RESrep-CAR)在体内、外对肿瘤细胞的杀伤
研究人员分别将白藜芦醇抑制系统和诱导系统安装至人的原代T细胞中,用于调控CAR受体的表达,从而实现通过白藜芦醇的剂量调控CAR-T细胞对肿瘤细胞的响应程度。
首先,研究人员设计通过白藜芦醇抑制转基因表达系统调控CAR受体的表达(RESrep-CAR),使白藜芦醇调控的抑制型CAR-T细胞在白藜芦醇不存在的情况下可以持续性表达CAR并杀伤肿瘤细胞,而当加入白藜芦醇时,则抑制CAR受体的表达,关闭CAR-T细胞的功能。通过优化,研究人员在T细胞中实现了可逆调控CAR的表达、细胞因子释放及肿瘤细胞杀伤(见图3)。

图3 RESrep-CAR装置在T细胞中的抑制CAR表达的调控效果
将工程化RESrep-CAR T细胞移植至人白血病小鼠模型(免疫缺陷型鼠NCG)体内,可通过调节白藜芦醇给药剂量来可控抑制细胞因子释放及肿瘤杀伤(见图4)。
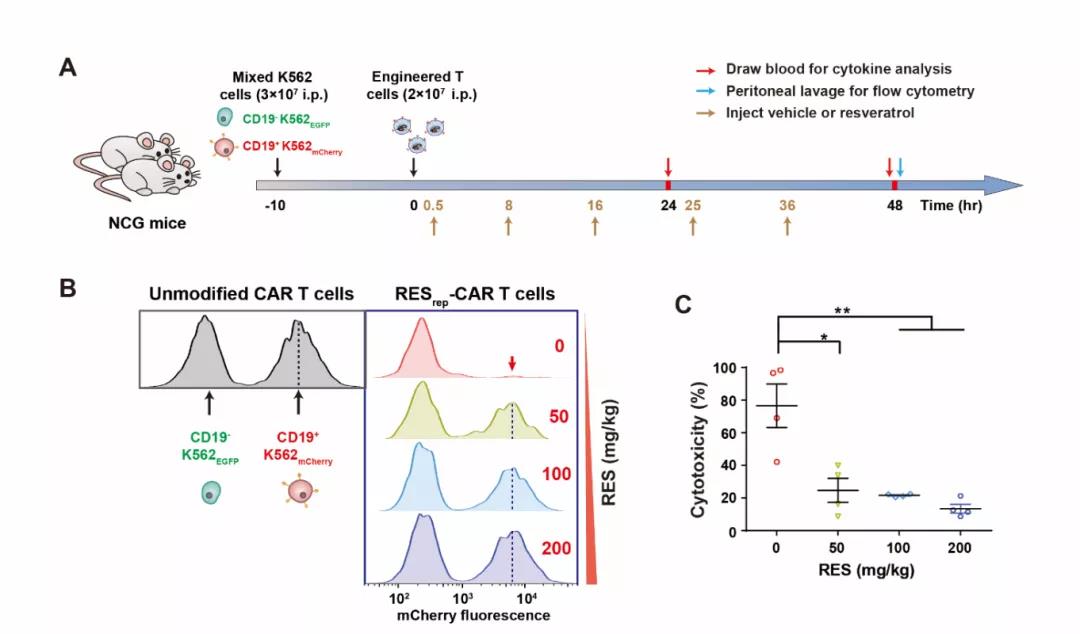
图4 RESrep-CAR装置在小鼠体内调控T细胞功能的效果
白藜芦醇诱导CAR表达控制系统(RESind-CAR)在体内、外对肿瘤细胞的杀伤
接下来,团队通过白藜芦醇诱导基因表达系统调控CAR受体的表达(RESind-CAR),实现了通过白藜芦醇剂量调控CAR受体表达及CAR依赖的T细胞功能激活。体外及体内白血病肿瘤模型鼠的实验结果也展示了RESind-CAR对CAR-T细胞激活的优异调控效果。在白血病小鼠模型中,通过口服或者腹腔注射白藜芦醇都可以精准调控RESind-CAR T细胞对肿瘤细胞的杀伤,从而延长了小鼠的生存时间(见图5)。
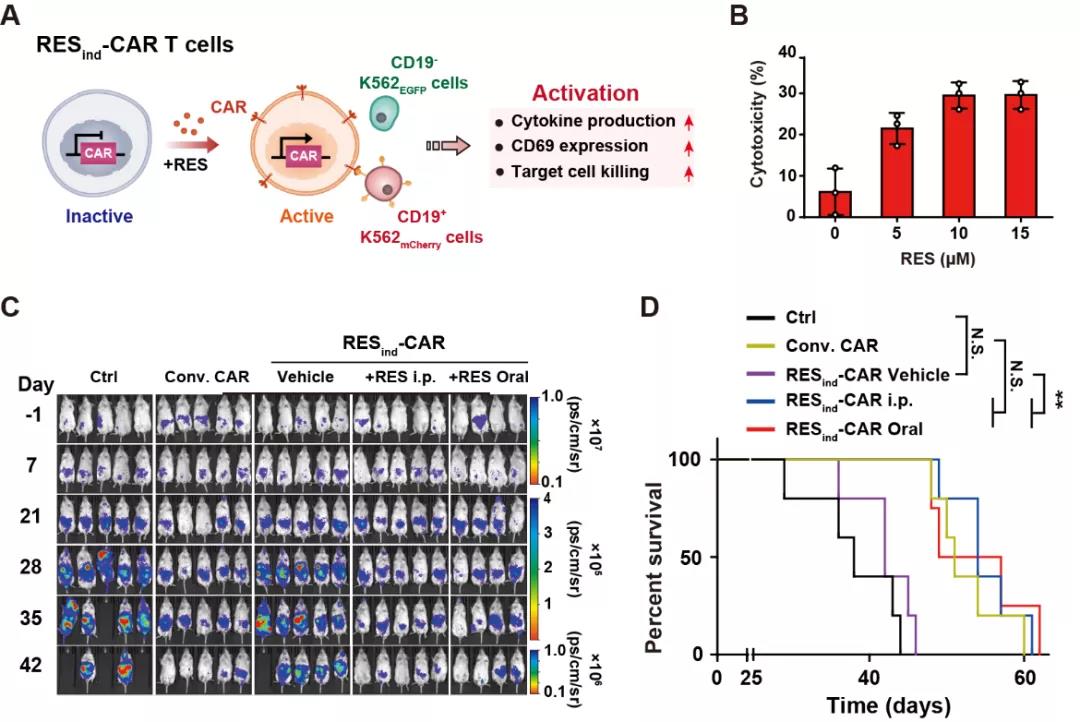
图5 RESind装置在T细胞和NCG鼠中杀伤肿瘤的效果
综上,该研究成功开发了白藜芦醇调控转基因表达的抑制系统(RESrep)和诱导系统(RESind),为合成生物学研究增添了一个有力的基因控制工具。同时研究人员提供了一种安全可控的CAR-T细胞肿瘤免疫治疗新方法。
更重要的是,白藜芦醇具有极高的保健和药用价值,被视为一种特别适合临床应用的触发分子开关。该研究所构建的白藜芦醇调控基因表达系统也可用于精准调控任意基因编码的治疗蛋白(酶、抗体、激素等),有望用于其它精准可控的药物递送,为未来基于基因和细胞治疗的精准医学提供一种安全、精准可控的新工具。
原始出处:
Linfeng Yang, Jianli Yin, Jiali Wu, et al. Engineering genetic devices for in vivo control of therapeutic T cell activity triggered by the dietary molecule resveratrol. PNAS August 24, 2021 118 (34) e2106612118.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言









#PNAS#
103
#癌细胞#
62
#红酒#
0
学习了,期待人体食用吸收代谢后的效果
113
学习了
141
#儿茶酸##阿魏酸##白藜芦醇#这些#中药#中重要的成分,在体内效果都不错,但是大部分在体内很难被吸收和利用,因此,几乎起不到实际的价值。也许将来有一天,通过药物化学对这些成分进行改进,使得保持药物活性同时,又方便地能吸收和利用。
183