自身免疫性胰腺炎 or 胰腺癌?把握要点,准确鉴别!
2019-08-14 李婉玉 齐月 吴娜 肝脏疾病疑难与经典病例(第四辑)
患者男性,64岁,因“腹痛、腹胀1个月余”于2013年11月15日入院。该患者1 个月前无明显诱因出现腹痛、腹胀,进食后加重,偶有恶心,无呕吐,自行口服“健胃消食片”等无明显好转,10天前就诊于某院,CT检查提示胰腺占位,遂于某医院住院给予保肝等对症治疗,但上述不适未见明显缓解。为明确诊断入笔者所在医院。病程中偶有恶心,无鼻出血、齿龈出血,无发热、咳嗽、咳痰,无胸闷、气短,无呕吐,无呕血、黑便,无
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言




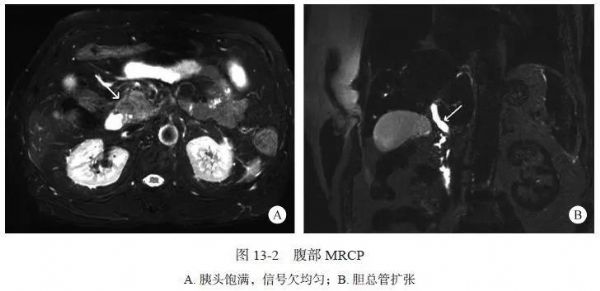
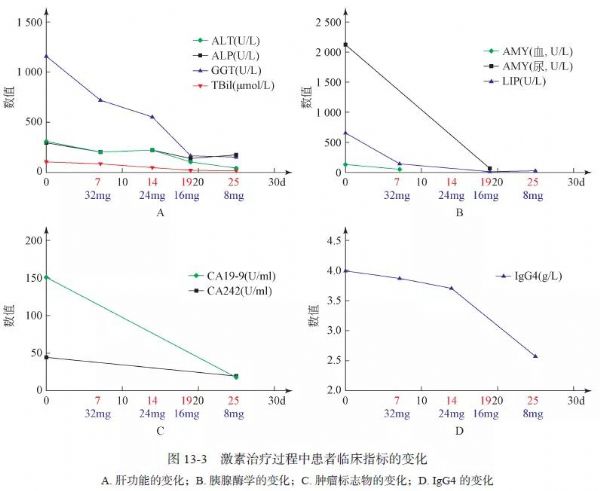
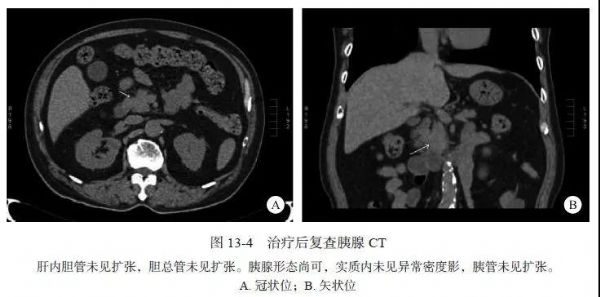

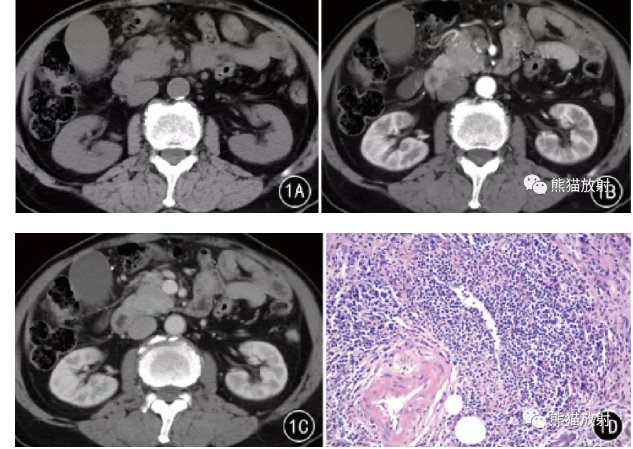






#自身免疫性胰腺炎#
90