Front. Neurosci|神经退行性疾病研究新方向:Nrf2和铁死亡
2022-09-16 brainnew神内神外 brainnew神内神外
通过靶向Nrf2来调节神经元铁死亡,或将成为预防和治疗神经退行性疾病的新方向
铁死亡(ferroptosis)是一种由谷胱甘肽(GSH)过氧化物酶4(GPX4)控制的细胞内微环境的氧化还原状态失调引起的一种调节性细胞死亡(RCD),铁螯合剂和亲脂性抗氧化剂可以抑制该过程。核转录因子E2相关因子2(Nrf2 / NFE2L2)已被证明在神经退行性疾病的治疗和铁死亡调节中起关键作用。
铁死亡促进神经退行性疾病的发展,而Nrf2及其靶基因(Ho-1,Nqo-1和Trx)的表达随着年龄的增长而下降。这篇综述简要概述了铁死亡的调节机制,尤其是Nrf2在铁死亡过程中的调节作用。
1铁死亡的调控网络
铁死亡有三大主要调节机制,包括脂质过氧化、氨基酸代谢紊乱及铁蓄积。

1.脂质过氧化
铁死亡选择性地优先氧化特定的含多不饱和脂肪酸(PUFA)的多磷酸化磷脂酰乙醇胺(PE),例如花生四烯酸(AA)和肾上腺素,最终导致脂质过氧化,因此脂质过氧化途径在调节铁死亡中起关键作用。酰基辅酶A合成酶长链家族成员4(ACSL4)是调节脂质组成的关键酶。在脂质过氧化途径中,ACSL4通过在内质网(ER)相关的氧合作用中心产生氧化的PE来促进铁死亡,而ACSL4催化AA或肾上腺素(AdA)的附着以产生AA或AdA酰基Co-A衍生物。然后通过溶血磷脂酰胆碱酰基转移酶3(LPCAT3)酯化为PE(AA-PE和AdA-PE)。随后,AA-PE和AdA-PE被15-脂氧合酶(15-LOX)氧化以产生脂质氢过氧化物,最终导致铁死亡。
P53在铁死亡中发挥双向调节作用。一方面,P53的丢失阻止了二肽基肽酶4(DPP4)的核积累,从而促进了质膜相关的DPP4依赖性脂质过氧化作用,最终导致了铁死亡。另一方面,亚精胺/亚精胺N1-乙酰基转移酶1(SAT1)作为p53的转录靶标,其表达诱导脂质过氧化,并在ROS诱导的压力下使细胞发生铁死亡,而敲除SAT1或抑制ALOX15的表达则部分阻断了p53介导的铁死亡。
2.氨基酸代谢
氨基酸代谢在铁死亡调节中也发挥至关重要的作用。GPX4是我们体内的脂质修复酶,并且被认为是铁死亡的关键调节因子。GPX4通过将脂质过氧化物(L-OOH)转化为无毒脂质来抵抗铁和氧依赖性的脂质过氧化。GSH是GPX4的辅助因子和合成底物,是GPX4发挥脂质修复功能所必需的。GSH是由谷氨酸,半胱氨酸和甘氨酸合成的重要胞内抗氧化剂。通过抑制胱氨酸/谷氨酸逆向转运体(system xc-)导致半胱氨酸消耗和GSH合成底物缺乏,进而削弱了抗氧化酶GPX4的功能,最终导致体细胞内氧稳态失衡,从而导致铁死亡。
3.铁代谢
铁是一种氧化还原活性金属,可以参与自由基的形成和脂质过氧化的进展。因此,铁的含量可以增加对铁死亡的敏感性。铁对于线粒体功能、突触可塑性和认知功能发展也是必需的。过量的细胞内铁通过破坏DNA并阻断基因组修复系统来加速衰老,这种过程被定义为铁老化的发生。当体内铁稳态失衡时,由核受体共激活因子4(NCOA4)介导的铁自噬释放铁结合到铁蛋白上,或由于转铁蛋白和转铁蛋白受体(来自细胞外环境的铁)失调导致不稳定铁库(LIP)异常增加。然后通过Fenton反应,产生羟基和过氧自由基,然后从PUFA二烯丙基碳中获取氧原子并诱导PUFA-PLs过氧化,最后诱发了铁死亡。
2核因子E2相关因子2在促铁调控中的研究进展
Nrf2是众所周知的转录因子,在抗氧化中起关键作用。Nrf2的下游基因包括Ho-1、Nqo-1、II期解毒酶(例如GSH S-转移酶、GPX4、GSH还原酶和谷氨酸-半胱氨酸连接酶亚基GCLc和GCLm),以及几种与多药耐药相关的转运蛋白。因此,Nrf2被认为是促铁作用的重要调节因子。Nerf2的活性受到Keap1的严格调控。
在常氧条件下,Nrf2与Keap1结合并随着在蛋白酶体中的泛素化和降解而失活。一旦人体处于氧化应激状态,或者如果存在大量亲电体或细胞毒性因子,Nrf2就会从Keap1结合位点释放并迅速转移至细胞核,随后与启动子区域的抗氧化反应元件(ARE)相互作用并通过激活转录途径来平衡氧化应激并维持细胞氧化还原稳态。此外,许多铁死亡相关基因受Nrf2转录调控,包括与GSH调控相关的基因、NADPH再生和铁调节(包括铁输出和存储,血红素的合成和分解代谢)等。
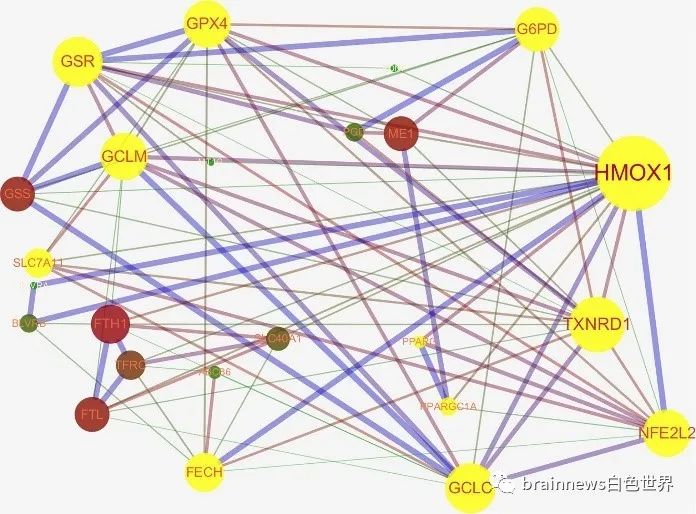
通过STRING数据库网站和Cytoscape 3.7.1软件分析发现Nrf2可以直接或间接调节与铁死亡相关的蛋白质
3阿尔茨海默病中的铁死亡
AD是最常见的神经退行性疾病,其特征在于由Tau蛋白组成的神经原纤维缠结(NFT)。脑组织中铁和铁蛋白(铁存储蛋白)的水平与淀粉样蛋白的沉积量有关。通过诱导成年小鼠的GPX4缺失发现海马神经元缺失和星形胶质细胞的增殖,这种变化将AD与铁死亡联系起来。
α硫辛酸(LA)是存在的具有抗氧化作用的天然酶辅助因子和铁螯合剂,研究发现,LA可以阻断tau蛋白诱导的铁过载、脂质过氧化和铁死亡相关炎症,从而稳定AD患者的认知功能。
双链RNA依赖性蛋白激酶(PKR)是能够介导多种应激信号,包括氧化应激和内质网应激的信号转导途径的一个组成部分,并被认为与神经退行性疾病相关。研究人员发现抑制HT22细胞中的PKR可以有效抑制内源性氧化应激诱导的铁死亡并保护HT22海马神经元。
此外,现有大量证据表明铁失稳态与淀粉样斑块的形成之间有因果关系。因此,在AD疾病的过程中,铁死亡可能发挥的重要作用值得进一步探索。
4总结与展望
铁死亡是一种由依赖于ROS和细胞内铁超载的脂质过氧化作用引起的新的独特的程序性细胞死亡形式,但其许多生理作用尚待明确。目前已经有足够的证据表明,在神经退行性疾病期间确实发生了铁死亡,并且通过靶向铁死亡的调节剂治疗神经退行性疾病已被证明是可靠的。
本文综述了铁死亡调控机制的新发现、Nrf2与铁死亡的关系及铁死亡在神经退行性疾病中的研究进展。作者建议,通过靶向Nrf2来调节神经元铁死亡,将成为预防和治疗神经退行性疾病的新方向。这对于研究人类神经系统疾病和衰老——尤其是在PD,AD和HD等神经退行性疾病中具有重要意义。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











#疾病研究#
69
#退行性疾病#
75
#神经退行#
56
#ROS#
0
#Nrf2#
129