Circulation 上海大学贝毅桦/肖俊杰团队发现抑制Hmbox1防治心肌缺血/再灌注损伤的新机制
2024-05-10 论道心血管 论道心血管 发表于加利福尼亚
该研究揭示了转录抑制因子Hmbox1在运动诱导的生理性心肌肥厚中的新作用,还明确了靶向Hmbox1改善心肌I/R损伤后心肌存活和葡萄糖代谢的治疗效果。
冠心病是全世界心血管疾病相关死亡的主要原因之一。尽管介入治疗急性心肌梗死的方法取得了进步,但在临床实践中仍然缺乏有效的预防心肌缺血/再灌注(I/R)损伤的药物。研究发现,运动诱导的生理性心肌肥厚调节因子可以保护心脏抵抗I/R损伤。Hmbox1是同源盒家族成员之一,被认为是一种转录抑制因子,在运动心脏中表达下调。然而,其在运动诱导的生理性心肌肥厚及其对心肌I/R损伤的潜在保护作用尚不清楚。
2024年5月6日,上海大学贝毅桦/肖俊杰团队在Circulation发表了题为“Inhibition of Hmbox1 Promotes Cardiomyocyte Survival and Glucose Metabolism Through Gck Activation in Ischemia/Reperfusion Injury”的研究性论文。该研究揭示了转录抑制因子Hmbox1在运动诱导的生理性心肌肥厚中的新作用,还明确了靶向Hmbox1改善心肌I/R损伤后心肌存活和葡萄糖代谢的治疗效果。

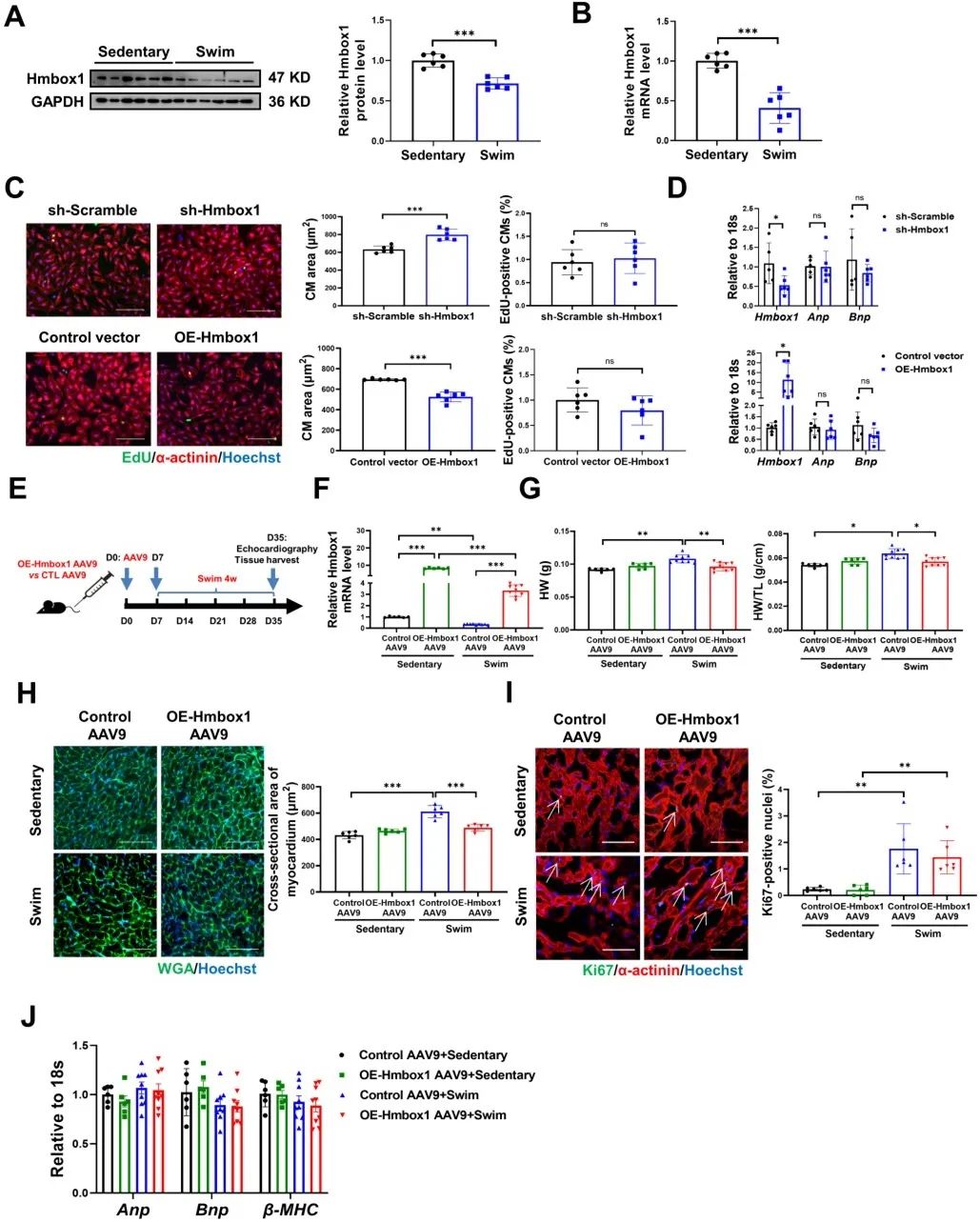
首先,该研究对C57/BL6J小鼠进行游泳运动,发现Hmbox1在游泳组心脏中表达显著下调。敲低Hmbox1促进心肌细胞生理性肥大,但不影响心肌细胞增殖。小鼠尾静脉注射表达Hmbox1的AAV9 (OE-Hmbox1-AAV9)后进行游泳运动,发现Hmbox1下调是运动诱导生理性心肌肥厚所必需。
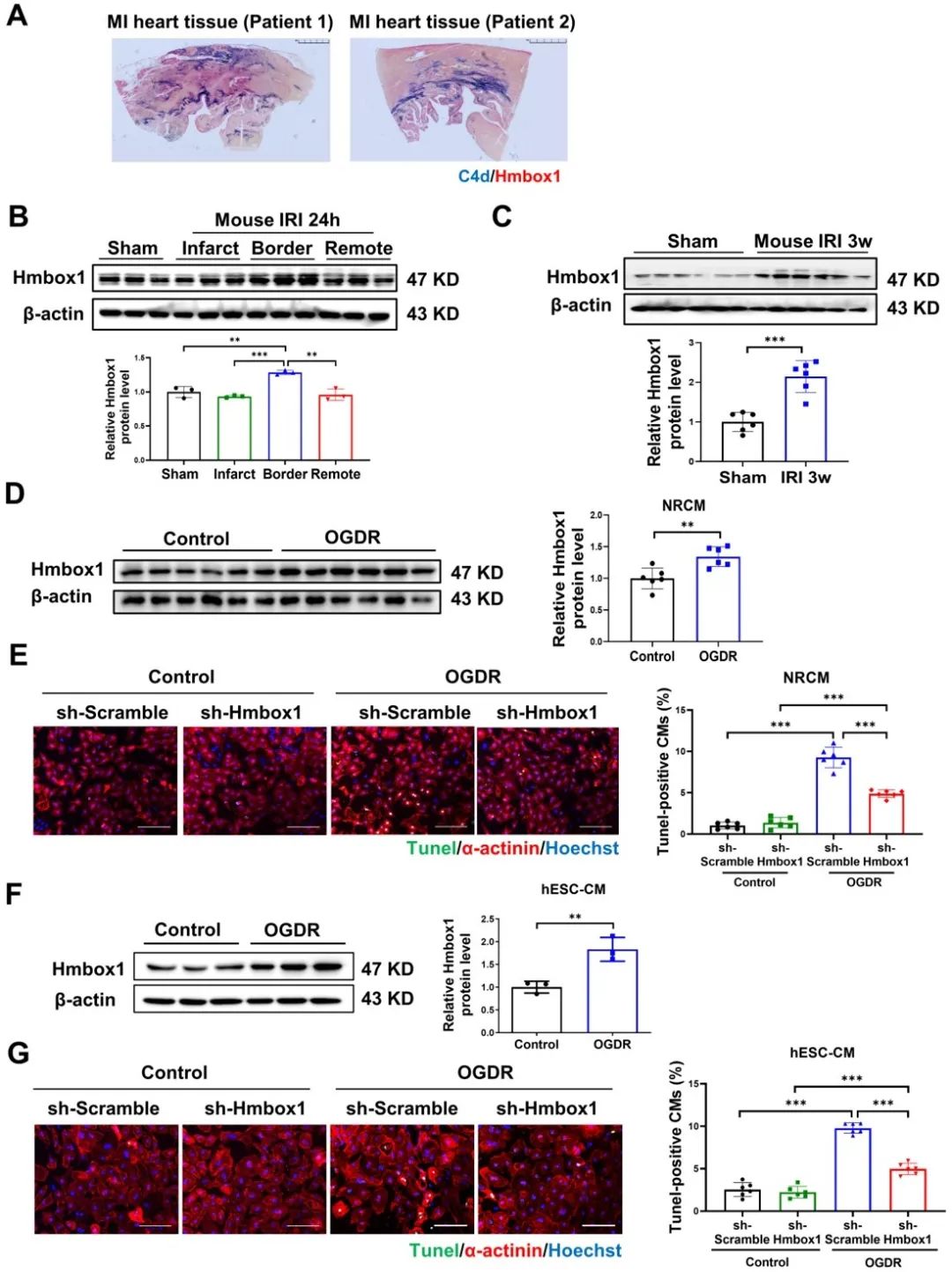
接着,研究者发现Hmbox1在已故心肌梗死患者的心脏样本、小鼠心脏急性I/R损伤(IRI 24h)边界区和慢性心脏重构(IRI 3W)中均表达上调。基于人胚胎干细胞来源的心肌细胞(hESC-CM),敲低Hmbox1抑制氧糖剥夺/恢复(OGDR)诱导的心肌细胞凋亡。
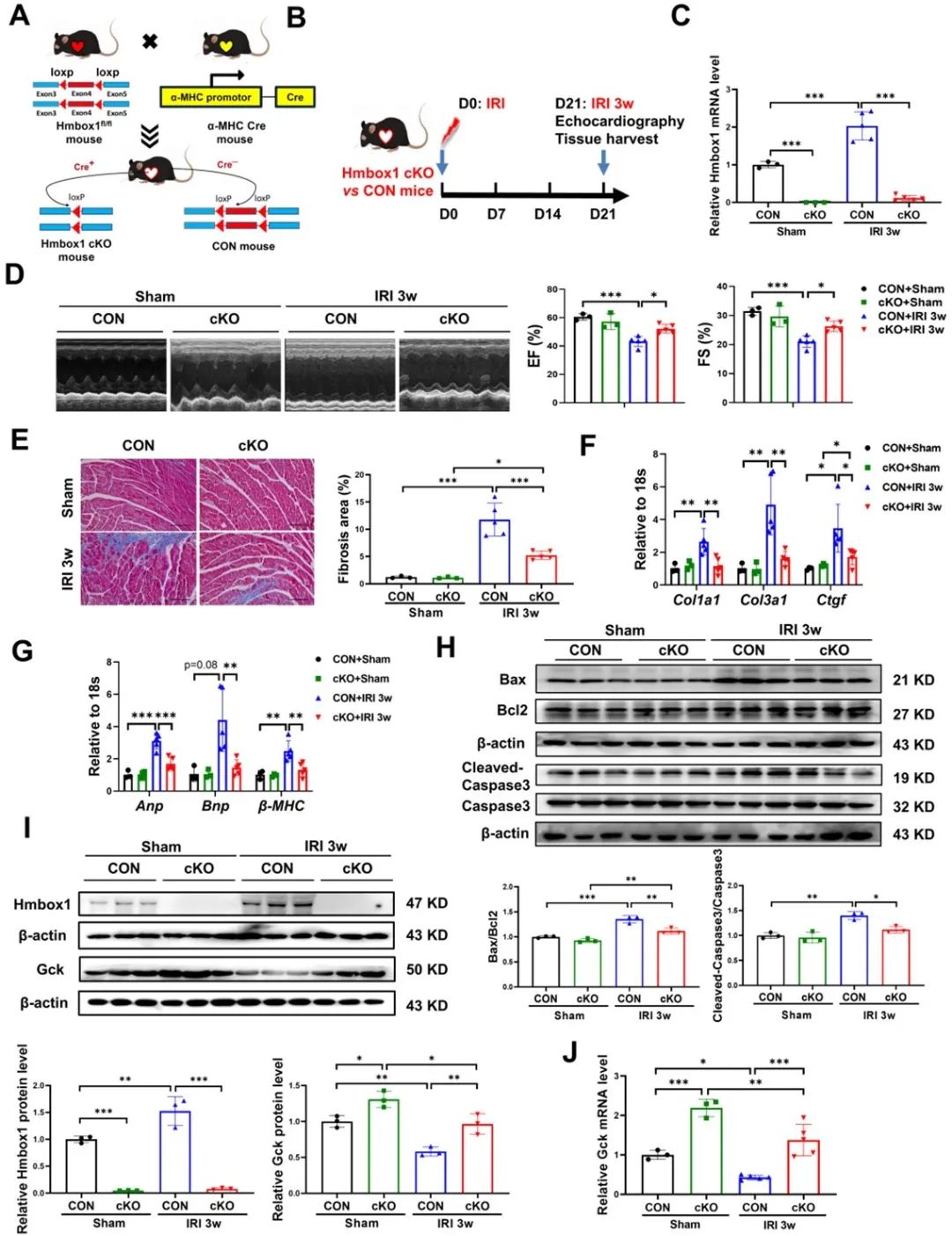
接着,基于尾静脉注射sh-Hmbox1-AAV9介导Hmbox1下调或者心肌特异性Hmbox1敲除小鼠,发现抑制Hmbox1可以减少I/R损伤诱导的梗死面积和心肌细胞凋亡,改善心功能。
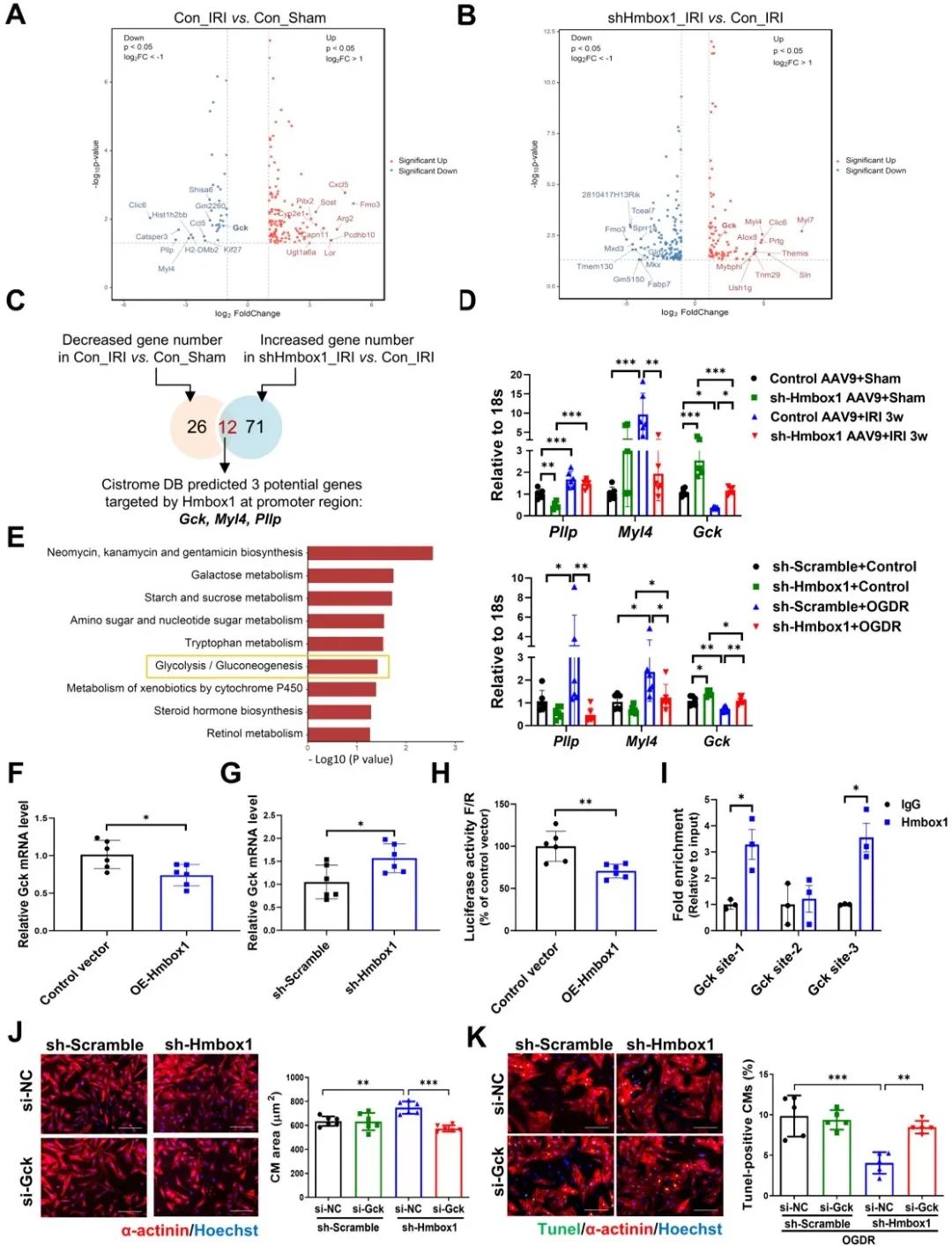
进一步,通过RNA-Seq和Cistrome Data Browser预测,发现葡萄糖激酶Gck是Hmbox1的下游分子。荧光素酶和染色质免疫共沉淀实验证明Hmbox1和Gck的相互作用。功能逆转实验证明,抑制Hmbox1通过激活Gck促进心肌细胞生理性肥大和抑制心肌细胞凋亡。
Gck编码葡萄糖激酶(Glucokinase),是己糖激酶蛋白家族的一员,该酶催化糖酵解的第一步:葡萄糖磷酸化形成6-磷酸葡萄糖。Seahorse实验结果表明,抑制Hmbox1通过激活Gck改善OGDR诱导的心肌细胞线粒体呼吸和糖酵解。
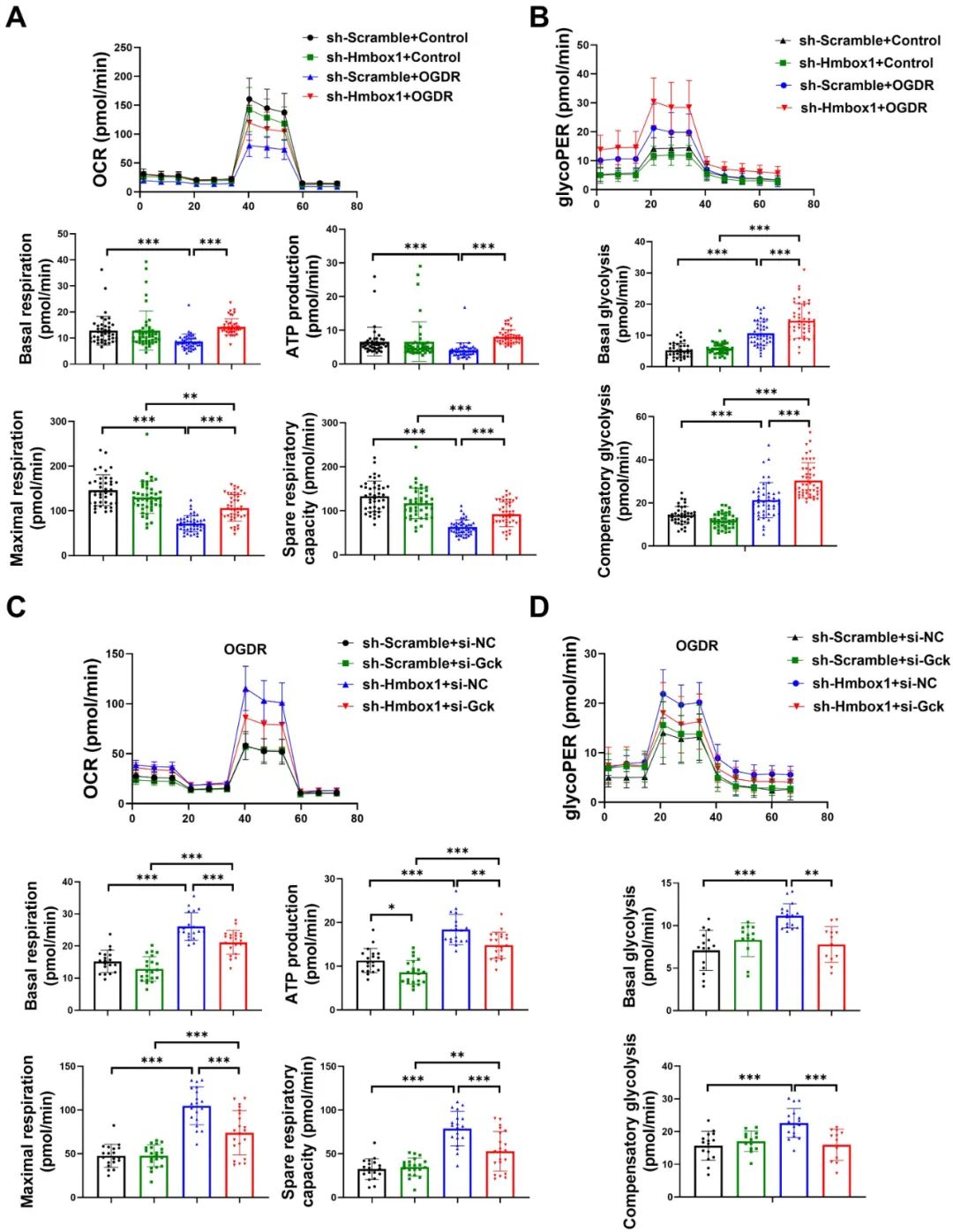
通过PROMO网站进行转录因子预测和分子实验,明确了ETS1可以负调控Hmbox1的表达。ETS1在小鼠IRI心脏组织中下调,而过表达ETS1可以改善心肌I/R损伤和心力衰竭。
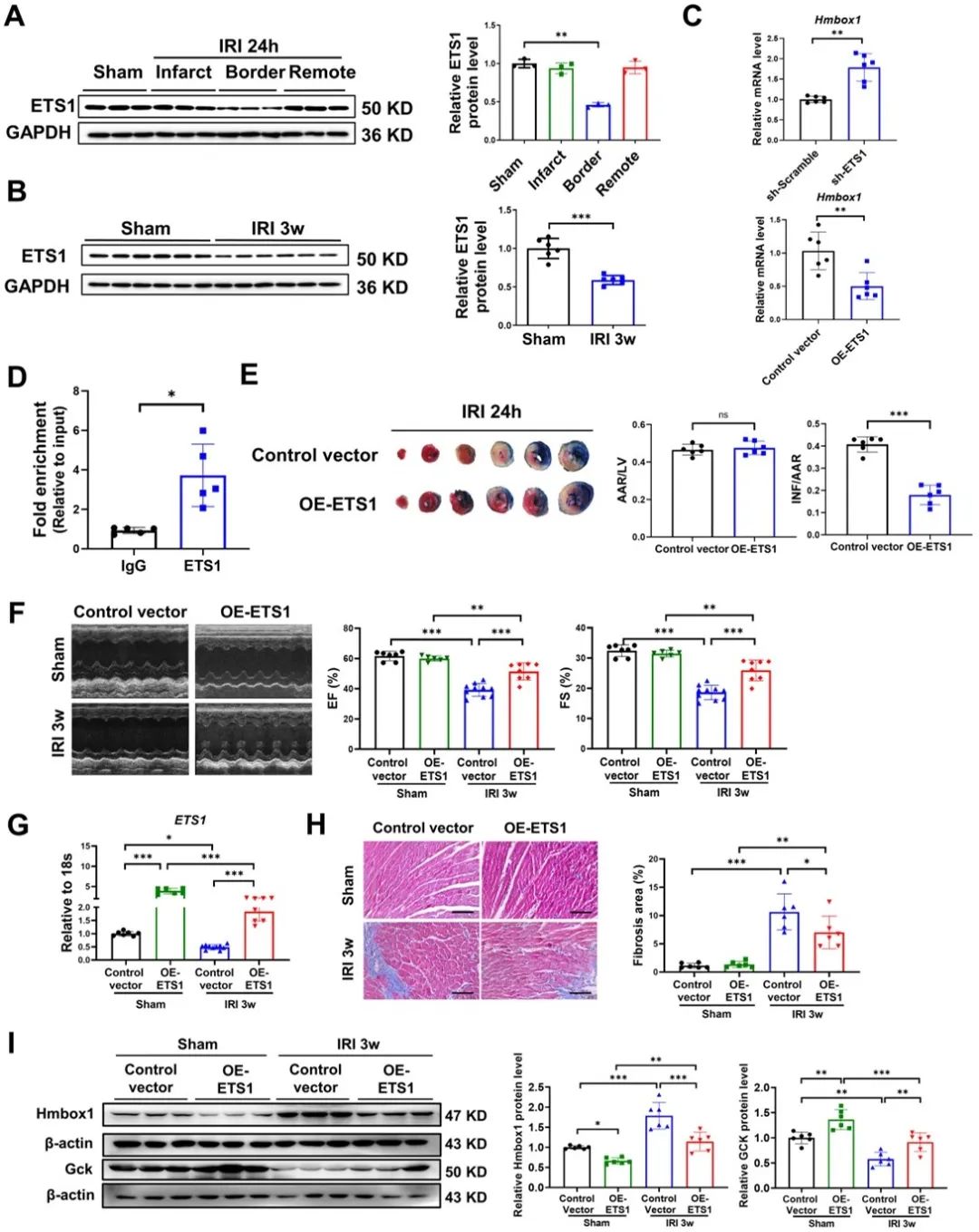
考虑到临床治疗方法多在心肌I/R损伤发生后应用,研究人员进一步研究Hmbox1敲低对I/R损伤的治疗效果。小鼠在心肌再灌注后30分钟内注射sh-Hmbox1-AAV9,结果表明AAV9介导的Hmbox1敲低对心肌I/R损伤具有治疗作用。
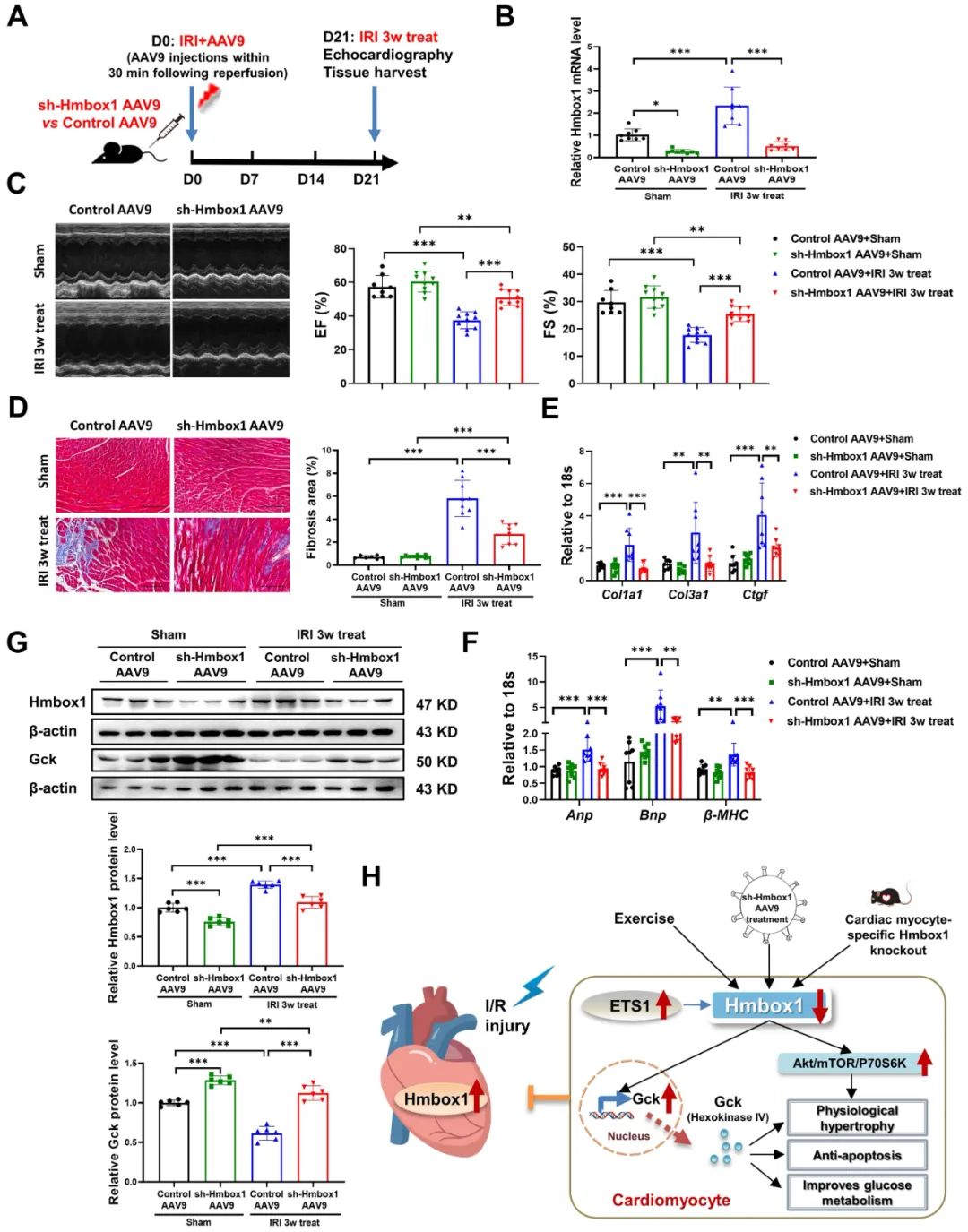
综上,该研究明确了Hmbox1作为一种转录抑制因子,参与了生理和病理的心脏改变。抑制Hmbox1对运动诱导的生理性心肌肥厚至关重要,并对心肌I/R损伤和心力衰竭提供保护。研究还揭示了抑制Hmbox1通过激活Gck改善心肌细胞线粒体呼吸和糖酵解的新机制,靶向Hmbox1及其相关通路有望提高心肌I/R损伤的心肌存活和葡萄糖代谢。
上海大学贝毅桦教授、朱玉娇博士后为该文共同第一作者;上海大学贝毅桦教授和肖俊杰教授为该文共同通讯作者。该研究得到了国家自然科学基金项目等项目支持。
原文链接:
https://www.ahajournals.org/doi/abs/10.1161/CIRCULATIONAHA.123.067592
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#冠心病# #心肌缺血# #葡萄糖代谢# #Hmbox1#
0