European Radiology;如何利用影像学预测低级别胶质瘤的ATRX突变状态?
2022-11-17 shaosai MedSci原创
与高级别胶质瘤(HGGs,CNS WHO 3级和4级)患者相比,低级别胶质瘤(LGG,CNS WHO 1级和2级)患者的死亡率较低,预后较好。

胶质瘤是最常见的原发性脑肿瘤类型,起源于肿瘤性胶质细胞或神经胶质细胞。根据世界卫生组织(WHO)对中枢神经系统(CNS)肿瘤的分类,胶质瘤在组织病理学上被分为1、2、3和4级。与高级别胶质瘤(HGGs,CNS WHO 3级和4级)患者相比,低级别胶质瘤(LGG,CNS WHO 1级和2级)患者的死亡率较低,预后较好。然而,低级别胶质瘤有时会发生恶性转化,这大大缩短了患者的生存时间。因此,早期诊断和及时干预是非常关键和重要的。
在2016年WHO中枢神经系统分类的基础上,新的2021年WHO中枢神经系统分类引入了重大变化,推动了分子诊断在中枢神经系统肿瘤分类中的作用。ATRX的突变首次在α地中海贫血X连锁智障综合征患者中发现。ATRX突变可能导致胶质瘤细胞的端粒酶失活,从而影响星形细胞肿瘤细胞的生物学行为,诱发LGG的恶性进展。遗憾的是,ATRX突变的状态主要通过手术或活检来检测,具有侵入性。因此,非侵入性地预测ATRX突变状态对于术前提供诊断和预后信息具有重要意义。
近日,发表在European Radiology杂志的一项研究建立了一个基于[18F]FDG PET和多模态MRI的临床放射组学综合模型,以实现IDH突变LGG的ATRX突变状态的无创术前评估。
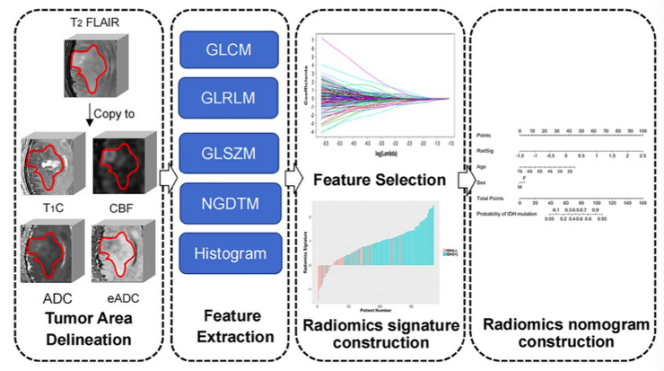
本研究纳入了诊断为IDH突变型LGG(CNS WHO 1级和2级)的122名患者(47名ATRX突变型,55名ATRX野生型)进入研究。从结构性MR(sMR)图像(增强T1加权成像,CE-T1WI;T2加权成像,T2WI)、功能性MR(fMR)图像(表观弥散系数,ADC;脑血容量,CBV)和代谢性PET图像([18F]FDG PET)共提取了5540个放射组学特征。使用随机森林算法建立了一个临床放射组学综合模型,将最佳的多模式放射组学模型与三个临床参数相结合。通过接收器操作特征(ROC)和决策曲线分析(DCA)评估了模型的预测效果。
最佳的多模式模型结合了sMR(CE-T1WI)、fMR(ADC)和代谢([18F]FDG)图像([18F]FDG PET+ADC+CE-T1WI),训练组和测试组的曲线下面积(AUCs)分别为0.971和0.962。整合了[18F]FDG PET+ADC+CE-T1WI、三个临床参数(KPS、SFSD和ATGR)的临床放射学综合模型在训练组和测试组显示出最佳预测效果(分别为0.987和0.975)。
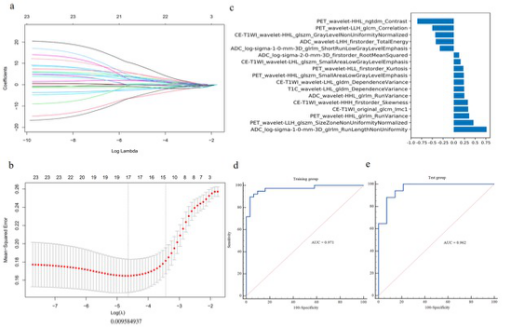
图 a, c LASSO. b [18F]FDG PET+CE-T1WI+ADC放射学模型中的特征系数. d, e 模型[18F]FDG PET+CE-T1WI+ADC在训练组和测试组的ROC曲线
本研究建立了一个基于[18F]FDG PET和多模式MRI的多中心临床放射学综合模型,该模型可同时提供结构、功能和代谢信息,并可应用于预测IDH突变的LGG的ATRX突变状态。
原文出处:
Liqiang Zhang,Hongyu Pan,Zhi Liu,et al.Multicenter clinical radiomics-integrated model based on [ 18 F]FDG PET and multi-modal MRI predict ATRX mutation status in IDH-mutant lower-grade gliomas.DOI:10.1007/s00330-022-09043-4
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言