NAT CHEM BIOL:科学家发现新的细菌通讯“语言”
2013-07-22 NAT CHEM BIOL bio360
发光杆菌显微镜图像。标为红色的细胞产生聚集因子 自然界中,细菌并不独居,而是和其它细菌形成群体生活。它们通过化学过程相互沟通,不仅能感应到其它细菌群体的存在,甚至彼此能建立合作网络。慕尼黑大学的研究人员对一种以前未知的细菌通信方式首次做出了解释,研究结果对医药研究有积极的推动。 慕尼黑大学的微生物学家黑尔曼(Ralf Heermann)博士和法兰克福歌德大学波德(Helge Bode)教授
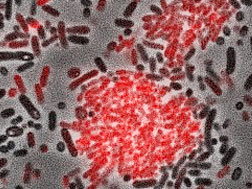
发光杆菌显微镜图像。标为红色的细胞产生聚集因子
自然界中,细菌并不独居,而是和其它细菌形成群体生活。它们通过化学过程相互沟通,不仅能感应到其它细菌群体的存在,甚至彼此能建立合作网络。慕尼黑大学的研究人员对一种以前未知的细菌通信方式首次做出了解释,研究结果对医药研究有积极的推动。
慕尼黑大学的微生物学家黑尔曼(Ralf Heermann)博士和法兰克福歌德大学波德(Helge Bode)教授合作,发现了一种以前未知的细菌通讯“语言”。
不同的细菌有不同的沟通方式。到目前为止得到较深入研究的细菌通信系统是使用N-酰基高丝氨酸内酯(N-acylhomoserine lactones)类信号分子。这些信号分子由鲁西族合酶(LuxI-family synthases)组中的酶产生。发送信息的细菌细胞分泌出信号,相邻细胞通过LuxR蛋白型受体识别浓度,信号感知功能使接收细胞改变基因表达模式,这导致细胞的功能特性或行为发生改变。但是,很多细菌具有LuxR蛋白受体但缺乏鲁西蛋白受体,因此,不能产生信号分子。这些受体被称为LuxR蛋白独体。
新类信号分子
黑尔曼和波德现在已经发现一种能够结合LuxR蛋白独体的配体。他们选择发光杆菌(Photorhabdus luminescens)作为研究模型系统,这是一种对昆虫致命的致病细菌。
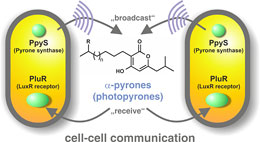
细菌通过化学过程沟通。慕尼黑大学的微生物学家黑尔曼(Ralf Heermann)博士和法兰克福歌德大学波德(Helge Bode)教授已经发现了一种新的细菌细胞与细胞间的通信系统,采用α-吡喃酮作为信号。吡喃酮由合酶PpyS产生,由LuxR独体受体PluR接收。
波德说,“我们已经发现了一种新的细菌信号分子,由一种前所未知的生化途径产生。”事实证明,这种细菌的LuxR蛋白独体响应称为α-吡喃酮的化合物,特别是对照片吡喃酮(photopyrones)作出响应。此外,研究人员已经识别出合成照片吡喃酮的催化物吡喃酮合酶(PpyS)。吡喃酮信令系统使细菌相互感应,从而产生导致细胞聚集的表面因子。黑尔曼和波德认为集体行为使得细菌细胞得以对抗昆虫的先天免疫系统,并允许它们生产各种毒素杀死昆虫。黑尔曼说,“发光杆菌是一个非常有用的有机物模型,因为它与许多人类病原体有关,包括肠出血性大肠杆菌(EHEC)和鼠疫菌。”
推动医药研究
新的研究结果引起医学界的极大兴趣,因为细菌病原体的通信系统对开发抗菌药物提供了方向。干扰细菌“聊天”的药剂可以抑制毒素的产生或防止生物膜的形成,这些药物只防止病原性状的表达,而不是像抗生素一样杀死细菌,抗药物性的危险将被极大地削弱。
黑尔曼说:“我们的研究结果表明,细菌之间的沟通比以前想像的要复杂得多。”研究结果发表在最新一期《自然化学生物学(Nature Chemical Biology)》杂志上。
Brachmann AO, Brameyer S, Kresovic D, Hitkova I, Kopp Y, Manske C, Schubert K, Bode HB, Heermann R.Pyrones as bacterial signaling molecules.Nat Chem Biol. 2013 Jul 14. doi: 10.1038/nchembio.1295.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#Biol#
48
#Bio#
52
#科学家发现#
64
#Nat#
44
#语言#
54