Cell Metab:多吃n-3和n-6多不饱和脂肪酸可以促进铁死亡介导的抗癌作用
2021-06-20 haibei MedSci原创
最近,研究人员进行了一项探究,他们没有阻断酸性癌细胞对FA的利用,而是研究了过量吸收特定的FA是否能导致抗肿瘤作用。
过去十年中,不同营养物质对癌细胞的生物合成、生物能量和抗氧化需求的贡献得到了广泛的研究。特别是,人们对癌症遗传学和新陈代谢重构之间的全新认知推动了多个重大发现,为特定癌症类型提供了新的治疗思路。
在许多这样的研究中,研究人员发现,癌细胞可以根据突变和微环境驱动的代谢偏好获得它们所需要的东西。然而,今天,研究人员越来越多地提出这样的问题:饮食是否可以通过调节肿瘤细胞对营养物质的获取和利用来影响癌症的发展。
关于以上问题的现有研究结果是矛盾的,部分研究认为,特定饮食有显著的肿瘤生长抑制作用,但也有相当数量的研究显示,大幅度的饮食选择变化对于缓解小鼠肿瘤进展的效果不佳,甚至适得其反。这些饮食研究大多是基于减少肿瘤主要营养物质的供应可以限制癌细胞增殖的原始假设。最常见的是通过低碳水化合物含量来限制热量,最近还研究了排除特定氨基酸的饮食。这些方法在癌症患者中的应用,包括通过生酮饮食,使脂肪生成酮体以保留健康器官,面临着明显的问题,包括体重减轻、相关的疲劳和虚弱,以及在癌症患者的日常生活中实施这些饮食的实际困难。

目前为止,旨在补充特定营养物质而不是限制饮食的策略较少。最近的研究发现,膳食组氨酸的补充是有希望的低风险干预措施,此外,膳食ω-3(n-3)多不饱和脂肪酸(PUFAs)多年来因其潜在的抗癌作用吸引了最多的关注。已有的研究也显示,肿瘤小鼠服用PUFA的结果确实振奋人心。然而,虽然饮食中的PUFAs比限制热量的饮食更容易处理,但对去潜在益处的临床验证仍处于起步阶段,试验数量少,入选患者有限,而且由于PUFA性质、数量和给药方式的变化,数据解释混乱。已有的对超过1000名结直肠癌患者的队列进行的研究显示,诊断后摄入更多的海洋n-3 PUFAs与较低的癌症相关死亡和更长的无病生存期有关。
已有的研究显示,肿瘤酸化可以通过刺激癌细胞的脂肪酸(FA)代谢促进疾病的发展。最近,研究人员进行了一项探究,他们没有阻断酸性癌细胞对FA的利用,而是研究了过量吸收特定的FA是否能导致抗肿瘤作用。
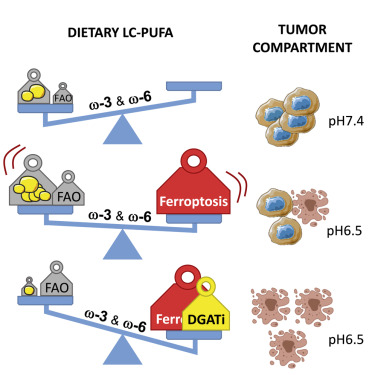
富含n-3和n-6多不饱和脂肪酸可以促进铁死亡介导的抗癌作用
结果显示,在肿瘤酸性环境的情况下,n-3和n-6多不饱和脂肪酸(PUFA)选择性地诱导了癌细胞的铁死亡。当超过甘油三酯储存在脂滴中的缓冲能力时,n-3和n-6 PUFA过氧化导致的细胞毒性作用与双键数量成正比,在二酰基甘油酰转移酶抑制剂(DGATi)的存在下更是如此。
此外,与富含单不饱和脂肪酸的饮食相比,富含n-3长链PUFA的饮食明显延缓了小鼠肿瘤的生长,这种效果在服用DGATi或铁蛋白酶诱导剂后进一步增强。
因此,这些数据指出,饮食中的PUFA是一种选择性的辅助性抗肿瘤方式,可以有效地补充药理学方法。
原始出处:
Emeline Dierge et al. Peroxidation of n-3 and n-6 polyunsaturated fatty acids in the acidic tumor environment leads to ferroptosis-mediated anticancer effects. Cell Metabolism (2021).
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#饱和脂肪酸#
88
#不饱和脂肪酸#
94
#Cell#
79
#Meta#
87
#MET#
67
#CEL#
76
#多不饱和脂肪酸#
71
#饱和脂肪#
87
#铁死亡#是热点,不过#ω-3#与ω-6的作用是相反的哦
162