HER2阳性乳腺癌又一ADC药物Enhertu,在中国申请临床试验
2020-04-16 MedSci MedSci原创
中国国家药监局药品审评中心(CDE)信息显示,第一三共(Daiichi Sankyo)和阿斯利康(AstraZeneca)在中国提交了新的一项抗体偶联药物Enhertu(fam-trastuzumab
中国国家药监局药品审评中心(CDE)信息显示,第一三共(Daiichi Sankyo)和阿斯利康(AstraZeneca)在中国提交了新的一项抗体偶联药物Enhertu(fam-trastuzumab deruxtecan-nxki,DS-8201,DXd)的临床试验申请,并在4月15日获受理。这是双方达成69亿美元合作后首次共同在中国提交临床试验申请!这也是继2020年1月,赫赛莱(T-DM1)在中国获批上市后,第二个ADC类药物。T-DM1是在中国上市的第一个ADC类药物,适应症也是HER2+的乳腺癌。
Enhertu (DXd)是一款靶向HER2的抗体偶联药物(ADC),曾获得美国FDA授予的突破性疗法认定、优先审评资格,于2019年12月在美国获批治疗HER2阳性乳腺癌。
Enhertu由第一三共开发,利用了其特有的ADC技术,将人源HER2抗体曲妥珠单抗通过四肽接头与一种新型拓扑异构酶1抑制剂链接,靶向癌细胞,并将药物递送至细胞内部。相比通常的化疗方式,这类新型药物可以降低化疗药的毒副作用。2019年3月,阿斯利康斥69亿美元巨资与第一三共达成合作,在全球范围内共同开发和商业推广Enhertu。
2019年12月,美国FDA加速批准上市,治疗无法切除或接受过2种以上抗HER2疗法治疗的转移性HER2阳性乳腺癌患者,比之前预期的获批时间提前了数月。EvaluatePharma也在去年的预测报告中,将Enhertu列为了2024年十大潜在重磅疗法之一。此前报道:阿斯利康携手第一三共开发的trastuzumab deruxtecan研究结果喜人,HER2阳性转移性乳腺癌患者中位无进展生存期达16.4个月
Enhertu之所以能够得到阿斯利康的青睐,并受到业界如此高的关注,是因为它具有以下几大特色:
-
具有很高的药物抗体比例(Drug Antibody Ratio, DAR)。Enhertu在一个抗体分子上能够偶联7-8个化疗药物,是已经获批ADC的2-4倍。这为它的抗癌疗效提供了坚实的基础。
-
具有稳定并能够被特异性切割的连接子。Enhertu的连接子不但在血液中表现出良好的稳定性,而且可以被肿瘤细胞中的组织蛋白酶(cathepsin)特异性切断,从而保证化疗药物在癌细胞中的释放。
-
具有独特作用机制的细胞毒性药物。Enhertu使用的细胞毒性药物是一种创新DNA拓扑异构酶I抑制剂(DXd),它的活性是常见化疗药物伊利替康的10倍,这意味着它能够以更小的剂量获得同样的疗效。
-
具有很强的细胞膜渗透能力:可以让DXd在杀伤吞进ADC的癌细胞之后,穿过附近的其它癌细胞的细胞膜,杀伤靶向细胞旁边的其它癌细胞,产生“旁观者效应”(bystander effect)
- 能够特异性被肿瘤中高度表达的溶酶体蛋白酶切割。
- DXd在血液中的半衰期显著缩短,可以让其很快被排泄出体外,减少毒副作用的发生。
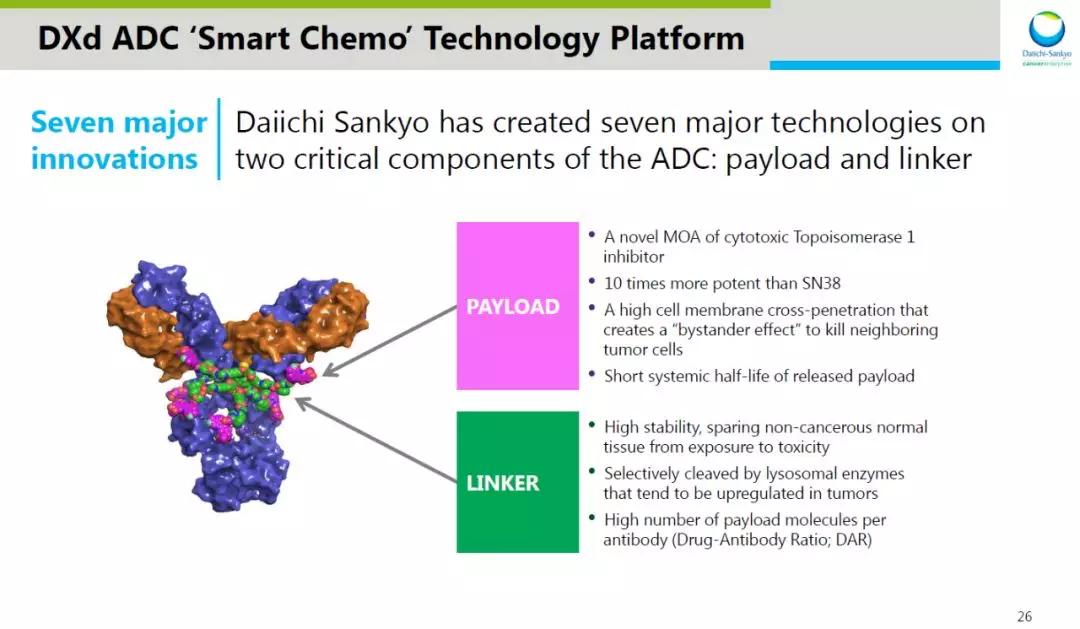
图片来源:第一三共官网
Enhertu独特的设计,也使其取得了很好的治疗效果。
美国FDA批准上市是基于包含184名患者的关键性2期临床数据。近日公布的数据表明,在治疗平均接受过6种前期疗法(包括ado-trastuzumab emtansine,trastuzumab,pertuzumab等)的HER2阳性乳腺癌患者中,Enhertu达到60.9%的客观缓解率(ORR)和97.3%的疾病控制率(DCR)。患者的中位缓解时间(DOR)为14.8个月,中位无进展生存期(PFS)为16.4个月。

Enhertu显著缩小患者肿瘤的大小
不过,阿斯利康和第一三共对Enhertu的期待远非HER2阳性乳腺癌这个适应症。在2019年的研发日活动上,第一三共曾表示,他们将与阿斯利康联合进行43项临床试验,不但全面覆盖多种乳腺癌患者,而且涵盖肺癌、胃癌、结肠癌、以及“不限癌种”适应症患者。阿斯利康和第一三共的雄伟目标是用它来变革HER2阳性肿瘤的治疗。
目前,Enhertu在其它癌种中的研究也取得了一些积极的结果。根据双方在今年3月26日发布的数据,在一项评估Enhertu治疗先前接受过治疗的HER2过度表达癌症患者的1期临床试验中,有55.6%的非小细胞肺癌(NSCLC)患者在接受治疗后出现肿瘤缩小。而在携带HER2突变的NSCLC患者中的疗效更为明显,Enhertu的治疗使该组中72.7%的患者得到缓解。
而且,Enhertu在治疗HER2低表达乳腺癌患者和表达HER2的胃癌和其它癌症类型中也表现出良好的疗效。第一三共在日前进行的研发日活动上表示,这款创新ADC将是该公司近期药物开发的重中之重。将与阿斯利康联合进行43项临床试验,不但全面覆盖多种乳腺癌患者,而且涵盖肺癌、胃癌、结肠癌、以及“不限癌种”适应症患者。阿斯利康和第一三共的雄伟目标是用它来变革HER2阳性肿瘤的治疗。
前不久刚刚在国内上市赫赛莱,是罗氏旗下基因泰克开发的一款抗体偶联药物,它的一端是靶向HER2的抗体trastuzumab,另一端则连有化疗药物DM1,称为T-DM1。这种药物能结合表达HER2的癌细胞,并对其进行杀伤。赫赛莱已在美国获批治疗HER2阳性乳腺癌。2020年1月,赫赛莱在中国获批上市,单药用于符合特定条件的 HER2阳性早期乳腺癌患者的辅助治疗,成为了中国首个获批上市的抗体偶联药物。
梅斯医学认为,这两个药物可能面临激烈的竞争。罗氏在乳腺癌领域既有传统优势,又有先发优势,但是阿斯利康在中国的深厚底蕴,不容小觑。同时,阿斯利康在肿瘤领域将会大干一场,如此大的蛋糕,不会放手不管的。
内容来自医药观澜,第一三共官网,以及网络等。
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言










#Enhertu#
67
#HER2阳性#
65