ERJ:诱导型一氧化氮合酶的骨髓细胞特异性缺失可保护小鼠免受烟雾诱导的肺动脉高压
2021-10-13 刘少飞 MedSci原创
慢性阻塞性肺疾病 (COPD) 是全球五种主要死亡原因之一。 COPD的病理变化是由吸入有害物质如香烟烟雾引起的,包括慢性气道炎症和进行性肺泡破坏,导致慢性支气管炎和肺气肿。


根据目前的 WHO 分类,COPD 相关性肺动脉高压 (COPD-PH) 被包括在 PH 的第 3 组(肺病/缺氧导致的 PH)中。尽管 PH 与 COPD 患者的急性加重风险增加和生存期降低有关,但尚无有效的药理学选择。 COPD-PH 发病机制中涉及的一些机制是内皮功能障碍、缺氧、血管修剪和毛细血管床丢失。此外,炎症细胞的激活可能有助于 COPD 的 PH 发展,因为肿瘤坏死因子 (TNF)-α、C 反应蛋白 (CRP)和白细胞介素 (IL)-6 等几种细胞因子的全身水平增加与 COPD 患者的 PH 相关,血管周围炎症细胞的数量与肺血管改变相关。这些发现更令人感兴趣,因为炎症在肺血管重塑中的突出作用已经在其他形式的 PH 中得到认可,尽管之前已经表明 COPD-PH 中发生的血管基因调控与其他类型大不相同这种肺血管疾病。此外,最近发现诱导型一氧化氮合酶 (iNOS) 是烟雾诱导的 PH 和肺气肿发病机制中的关键参与者。在暴露于烟雾的小鼠中,iNOS 抑制可预防和逆转实质破坏、PH 和肺血管重塑。此外,我们证明骨髓衍生细胞中的 iNOS 表达正在驱动肺血管改变,而不是肺气肿的发展。然而,尚不清楚哪种骨髓衍生细胞类型驱动该过程以及各自的机制是什么。我们在这里假设,导致烟雾诱导 PH 的病理信号是由骨髓细胞中 iNOS 表达升高触发的,巨噬细胞起着关键作用,并且人类可能会发生与小鼠类似的过程。 iNOS 是一氧化氮合酶的诱导型、钙非依赖性和高通量亚型,一氧化氮合酶是一种从 L-精氨酸和分子氧产生一氧化氮的酶。这种酶在免疫系统中具有突出的作用,它超越了其抗菌和抗真菌活性,涉及对表达细胞的表型以及相邻免疫细胞的功能和组成的影响。
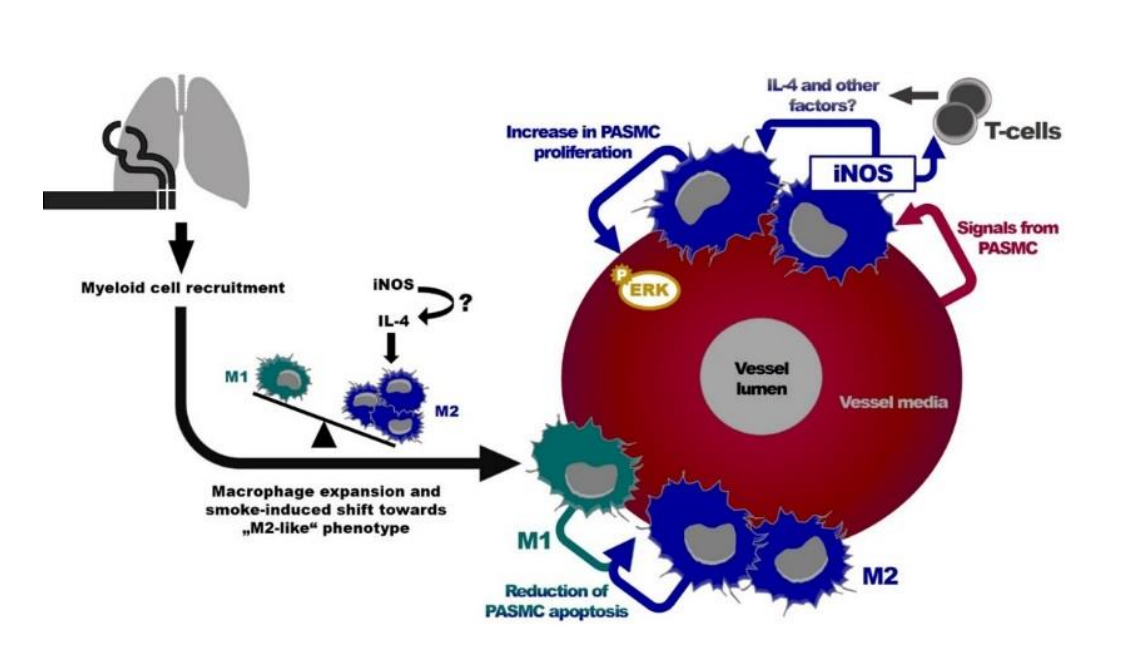
在这项研究中,确定驱动烟雾诱导 PH 的 iNOS 表达细胞类型并破译所涉及的促增殖途径。
为了解决这个问题,该研究使用了 1) 慢性烟雾暴露中的骨髓细胞特异性 iNOS 敲除小鼠,2)巨噬细胞和肺动脉平滑肌细胞 (PASMC) 的共培养以破译潜在的信号通路。骨髓细胞特异性 iNOS 敲除可防止小鼠烟雾诱导的 PH,但不能防止肺气肿。此外,骨髓细胞中的 iNOS 缺失改善了 CD206(M2 极化的标志物)在间质巨噬细胞上表达的增加。重要的是,观察到的对肺巨噬细胞的影响与缺氧无关,因为这些小鼠会出现缺氧诱导的 PH。在与 M2 极化巨噬细胞的共培养物中,烟雾诱导的 PASMC 增殖可以通过吞噬细胞中的 iNOS 缺失以及 PASMC 中的 ERK 抑制来消除。至关重要的是,CD206 阳性和 iNOS 阳性巨噬细胞积聚在 COPD 患者肺部重塑血管附近,如免疫组织化学所示。 研究结果表明,骨髓细胞中的 iNOS 缺失赋予烟雾暴露小鼠和为 M2 样巨噬细胞和 PASMC 在潜在肺血管重塑中依赖 iNOS 的通讯提供证据。
文章出处:
Gredic M, Wu CY, Hadzic S, Pak O, Savai R, Kojonazarov B, Doswada S, Weiss A, Weigert A, Guenther A, Brandes RP, Schermuly RT, Grimminger F, Seeger W, Sommer N, Kraut S, Weissmann N. Myeloid cell-specific deletion of inducible nitric oxide synthase protects against smoke-induced pulmonary hypertension in mice. Eur Respir J. 2021 Sep 2:2101153. doi: 10.1183/13993003.01153-2021. Epub ahead of print. PMID: 34475225.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言












#动脉高压#
60
#特异性#
80
#骨髓细胞#
84
#细胞特异性#
73
#一氧化氮#
79
#髓细胞#
84