Molecular Cell:难治性乳腺癌的潜在药物靶点:RNA结合蛋白YTHDF2
2021-07-04 网络 网络
研究员发现破坏 YTHDF2 依赖性 mRNA 降解会触发三阴性乳腺癌 (TNBC) 细胞和肿瘤的细胞凋亡。
在癌症研究中,一个共同的目标是找到关于癌细胞的一些东西——某种分子——驱动它们的生存能力,并确定该分子是否可以被药物抑制,阻止肿瘤生长。更好的是:该分子不存在于健康细胞中,因此它们不会受到新疗法的影响。
这种方法已经取得了很多进展,称为分子靶向癌症治疗。目前的一些癌症治疗方法会抑制变得过度活跃的酶,从而使细胞增殖、扩散和存活超出正常范围。挑战在于许多已知的癌症驱动分子是“不可成药的”,这意味着它们的类型、形状或位置阻止药物与其结合。
我们知道,在癌症进展过程中发生的细胞生长速率和特性的变化是由特定基因表达特征驱动的,这些基因表达特征由 DNA 结合转录因子 (TF) 和 RNA 结合蛋白 (RBP) 的活性编程。为了支持高致癌生长率,癌细胞通常需要增加转录水平和由 TF 控制的全局前 RNA 合成,从而增加细胞对 RBP 转录后处理的依赖。尽管 TF 突变已经研究了几十年,但 RBP 作为疾病的驱动因素和治疗相关的目标一直被忽视。RNA 结合蛋白 (RBP) 是转录后基因表达的关键调节因子,异常的 RBP-RNA 相互作用可促进癌症进展。
2021 年 7 月 2 日发表在Molecular Cell 上的最新研究中,加州大学圣地亚哥分校医学院团队在人体细胞和小鼠模型中发现,RNA 结合蛋白代表了一类新的癌症药物靶点,包括三阴性乳腺癌,一种特别难以治疗的癌症,因为它缺乏大多数其他分子药物靶点。研究员发现一种特别突出的 RNA 结合蛋白:YTHDF2。当研究人员从移植到小鼠体内的人类三阴性乳腺肿瘤中通过基因去除 YTHDF2 时,肿瘤体积缩小了大约 10 倍。

研究人员使用 CRISPR 基因编辑技术一个一个地系统地沉默了这些癌细胞中的RNA 结合蛋白。他们发现了 57 种 RNA 结合蛋白,当这些蛋白被抑制时,会杀死具有已知过度活跃的癌症驱动因子的癌细胞。合成致死方法的优点是不产生致癌分子的正常细胞应该不受治疗影响。
在这 57 种 RNA 结合蛋白中,YTHDF2 似乎最有前途。研究员发现破坏 YTHDF2 依赖性 mRNA 降解会触发三阴性乳腺癌 (TNBC) 细胞和肿瘤的细胞凋亡。翻译 mRNA 的 scRibo-STAMP 分析揭示了 YTHDF2 耗尽实体瘤中单细胞翻译组的独特改变,这选择性地促进了 TNBC 细胞中内质网应激诱导的细胞凋亡。
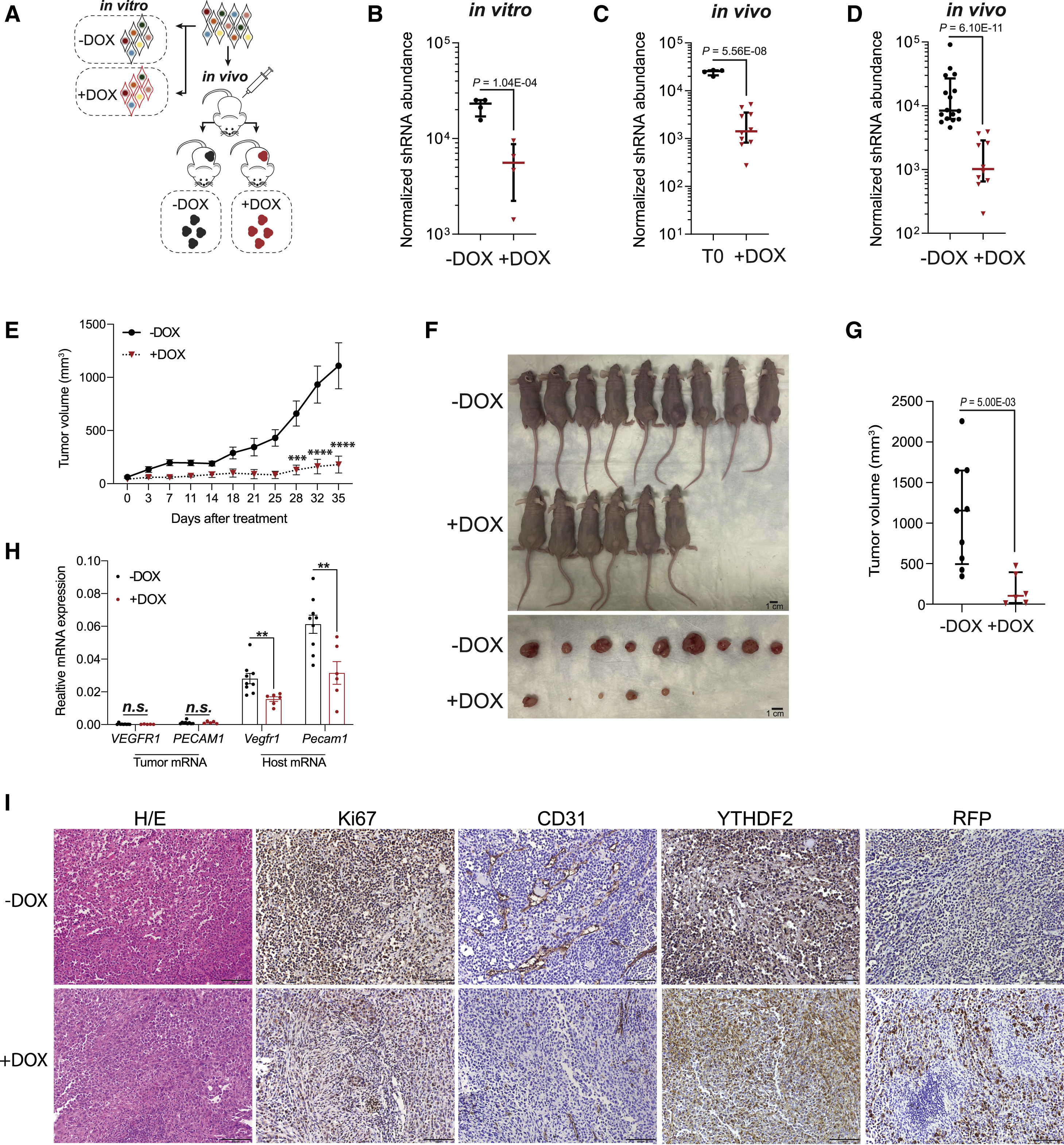
TNBC细胞中YTHDF2的消耗抑制体内肿瘤生长
研究人员在这项研究中使用 STAMP 来详细了解构成乳腺肿瘤的各种细胞在没有 YTHDF2 的情况下如何表现。该方法揭示了缺乏 YTHDF2 的癌细胞因压力诱导的细胞凋亡而死亡,这是细胞用来自我破坏的一种精心控制的机制。细胞凋亡应该关闭故障细胞,因此不会出现肿瘤,但它并不总是有效。通过去除 YTHDF2,他们设法重新激活了这种细胞死亡信号。
为了测试通过抑制 YTHDF2 治疗癌症的安全性,研究人员设计了在成年身体的每个细胞中都缺乏 YTHDF2 的小鼠,而不仅仅是移植的乳腺癌细胞。这些小鼠看起来完全正常——不仅没有肿瘤,体重或行为也没有变化。
综上,该研究结果通过揭示 YTHDF2 在抵消MYC 驱动的乳腺癌中mRNA 合成的全球增加中的关键作用,突出了 RBP 的治疗潜力。
参考文献:Jaclyn M. Einstein, Mark Perelis,Inhibition of YTHDF2 triggers proteotoxic cell death in MYC-driven breast cancer,
Molecular Cell,2021,https://doi.org/10.1016/j.molcel.2021.06.014.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言


















#潜在药物#
69
#RNA结合蛋白#
0
#Cell#
82
#CEL#
74
#药物靶点#
101
#难治性#
74