CELL:乔杰汤富酬团队发现人类原始生殖细胞中基因表达网络和DNA甲基化调控规律
2015-06-05 MedSci MedSci原创
封面设计源于中国古代象征生殖的图腾——玄武,寓意哺乳动物通过有性生殖(蛇和龟)来维持完整的生命周期(圆形),而中心处的生殖细胞(红色)则在遗传信息的世代沿袭中起着非常关键的作用。 2015年6月4日,国际知名学术期刊CELL(细胞)以封面文章的形式发表了北京大学第三医院乔杰研究组和北京大学生命科学学院汤富酬研究组的合作研究成果——人类原始生殖细胞中基因表达的表观遗传调控相关研

封面设计源于中国古代象征生殖的图腾——玄武,寓意哺乳动物通过有性生殖(蛇和龟)来维持完整的生命周期(圆形),而中心处的生殖细胞(红色)则在遗传信息的世代沿袭中起着非常关键的作用。
2015年6月4日,国际知名学术期刊CELL(细胞)以封面文章的形式发表了北京大学第三医院乔杰研究组和北京大学生命科学学院汤富酬研究组的合作研究成果——人类原始生殖细胞中基因表达的表观遗传调控相关研究。该项工作系统、深入地研究了人类多个发育阶段原始生殖细胞(PGC)的转录组和DNA甲基化组,发现人类原始生殖细胞不同于小鼠原始生殖细胞的关键独特特征。
基因组DNA甲基化作为一种重要的表观遗传修饰方式,是调控细胞分化过程中基因表达的主要机制之一。它虽然不改变基因序列但可以遗传给后代。而且,易受外界环境的影响而发生改变,在胚胎发育、干细胞分化、癌症的发生等方面发挥着重要作用。研究发现,在哺乳动物胚胎发育过程中,有两次大规模的DNA甲基化组重编程,分别在受精后植入前的胚胎和植入后胚胎的生殖细胞中。而既往通过小鼠作为模式动物进行的研究发现,复杂基因表达调控网络以及大规模的DNA甲基化重编程对于早期胚胎以及原始生殖细胞的发育非常重要。
2014年,乔杰、汤富酬研究团队在NATURE(自然)杂志上首先报告了人类植入前胚胎的DNA甲基化特征:精卵结合后,父母的表观遗传记忆信息(基因组DNA甲基化)被大规模擦除,而印记基因的甲基化得以精确维持、重复序列元件上也保留了大量DNA甲基化,从而传递给后代;胚胎着床后,基因组DNA重新甲基化。国际表观遗传学专家Wolf Reik和Gavin Kelsey在NATURE杂志同期发表述评,称此项工作“为研究人类胚胎发育的表观遗传调控奠定了基础,有助于评估辅助生殖技术对人类健康的长期影响”。
在此前的植入前胚胎研究基础上,该团队对植入后的人类原始生殖细胞(PGC)DNA甲基化组重编程过程进行了研究。正常情况下,一个植入后胚胎大部分组织器官的基因组DNA加上甲基化标记后将基本维持稳定,不再擦去。而含有要传递给后代遗传信息的原始生殖细胞则要经历大规模的DNA甲基化擦除和重建过程。
PGC产生于胚胎发育的早期,是发育为成熟的精子和卵母细胞的前体细胞。该研究发现,与小鼠原始生殖细胞类似,处于发育早期的人类原始生殖细胞会表达与干细胞多能性相关及与生殖细胞发育相关的基因。而与小鼠不同的是,人类原始生殖细胞并不表达关键的转录因子基因SOX2,却表达SOX家族的另外两个基因SOX15和SOX17;进入减数分裂阶段的人类原始生殖细胞其转录组发生明显改变,同一个胚胎的不同生殖细胞处于显著不同的发育状态。其次,在人类植入后雌性胚胎中,每个细胞的两条X染色体中的一条会随机失活,以保持两性的X染色体剂量相同(两性都保持每个细胞中只有一条活跃转录的X染色体)。在人类雌性胚胎的原始生殖细胞中失活的那条X染色体会被重新激活。此研究发现,第4周的雌性原始生殖细胞已完成X染色体重新激活,明显早于小鼠。第三,人类原始生殖细胞在发育过程中会经历大规模的DNA甲基化擦除,在胚胎发育到第10-11周时,DNA甲基化水平降至最低点,仅有7%左右保留下来。这是人类所有已知类型的体内正常细胞中DNA甲基化程度最低的细胞类型,说明原始生殖细胞的DNA甲基化组具有鲜明的独特性。第四,虽然人类原始生殖细胞基因组中绝大部分区域的DNA甲基化被完全擦除,但在一些重复序列元件上仍然残留大量DNA甲基化,尤其是微卫星序列ALR以及一些进化上比较年轻的元件,为人类隔代遗传现象的表观遗传学分析提供了有用的线索。
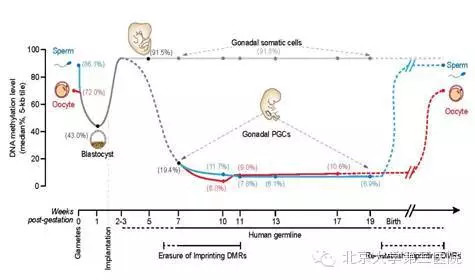
人类生殖细胞(精子、卵母细胞及原始生殖细胞)、囊胚以及着床后胚胎体细胞的DNA甲基化水平示意图
该项研究首次为人类提供了一个原始生殖细胞发育过程中基因表达的表观遗传调控坐标,加深了人们对人类早期胚胎发育特征及表观遗传重编程过程的认识。为人类生殖细胞的表观遗传重编程、早期胚胎全能性的建立、干细胞向精卵定向分化以及DNA甲基化的隔代遗传等问题的探究提供了理论基础。对辅助生殖技术的安全性评估、生殖内分泌与代谢性疾病是否会遗传给后代或隔代遗传、反复流产与胚胎停育、以及临床上生殖细胞发育异常相关疾病等的研究具有非常重要的意义。CELL杂志同期发表评述“Forget the Parents: Epigenetic Reprogramming in Human Germ Cells”。
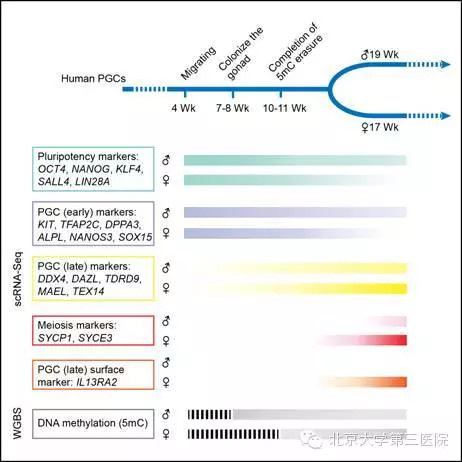
人类原始生殖细胞代表性基因的表达水平以及DNA甲基化随发育时间变化的示意图
该项工作由北京大学第三医院联合北京大学生命科学学院生物动态光学成像中心完成,郭帆博士、闫丽盈博士、郭红山和李琳博士研究生是这篇论文的并列第一作者。乔杰教授和汤富酬研究员是该论文的共同通讯作者。该项研究得到了国家自然科学基金、国家重大科学研究计划、北京市科委基金、以及北大清华联合中心基金等支持。
同日,CELL杂志还刊发了美国与台湾的合作研究团队、英国剑桥大学团队关于人类原始生殖细胞发育过程的基因表达及DNA甲基化表观遗传特征的研究结果。在同一期同时发表三个来自不同国家的团队独立开展的研究,充分体现了该研究在科学领域的重要性。这三个研究,内容与结果略有不同,但又相互验证,共同为人类认识自身配子发生的特征做出了突出贡献。
文章链接:
Fan Guo*, Liying Yan*, Hongshan Guo*, Lin Li*, Boqiang Hu, Yangyu Zhao, Jun Yong, Yuqiong Hu, Xiaoye Wang, Yuan Wei, Wei Wang, Rong Li, Jie Yan, Xu Zhi, Yan Zhang, Hongyan Jin, Wenxin Zhang, Yu Hou, Ping Zhu, Jingyun Li, Lin Zhang, Sirui Liu, Yixin Ren, Xiaohui Zhu, Lu Wen, Yi Qin Gao,Fuchou Tang & Jie Qiao.The Transcriptome and DNA Methylome Landscapes of Human Primordial Germ Cells.Cell 161,1437-1452.(2015) (*co-first author)
Guo H, Zhu P, Yan L, Li R, Hu B, Lian Y, Yan J, Ren X, Lin S, Li J, Jin X, Shi X, Liu P, Wang X, Wang W, Wei Y, Li X, Guo F, Wu X, Fan X, Yong J, Wen L, Xie SX, Tang F, Qiao J.The DNA methylation landscape of human early embryos. Nature. 2014 Jul 31;511(7511):606-10
乔杰、汤富酬的其它文献:
Lu S, Zong C, Fan W, Yang M, Li J, Chapman AR, Zhu P, Hu X, Xu L, Yan L, Bai F, Qiao J, Tang F, Li R, Xie XS.Probing meiotic recombination and aneuploidy of single sperm cells by whole-genome sequencing. Science. 2012 Dec 21;338(6114):1627-30
Hou Y, Fan W, Yan L, Li R, Lian Y, Huang J, Li J, Xu L, Tang F, Xie XS, Qiao J.Genome analyses of single human oocytes. Cell. 2013 Dec 19;155(7):1492-506
Wen L, Li X, Yan L, Tan Y, Li R, Zhao Y, Wang Y, Xie J, Zhang Y, Song C, Yu M, Liu X, Zhu P, Li X, Hou Y, Guo H, Wu X, He C, Li R, Tang F, Qiao J.Whole-genome analysis of 5-hydroxymethylcytosine and 5-methylcytosine at base resolution in the human brain.Genome Biol. 2014 Mar 4;15(3):R49.
Yan L, Yang M, Guo H, Yang L, Wu J, Li R, Liu P, Lian Y, Zheng X, Yan J, Huang J, Li M, Wu X, Wen L, Lao K, Li R, Qiao J, Tang F.Single-cell RNA-Seq profiling of human preimplantation embryos and embryonic stem cells. Nat Struct Mol Biol. 2013 Sep;20(9):1131-9
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








#表达网络#
63
赞,
161
赞,
128
赞,
142
牛人啊,
162
牛人啊,
159
女神
107
很值得好学习
135
#CEL#
47
#Cell#
53