Journal of Hematology & Oncology:CAR-HEMATOTOX评分作为接受BCMA指导的CAR-T复发/难治性多发性骨髓瘤患者的毒性和反应的预后模型
2023-11-13 Jenny Ou MedSci原创 发表于上海
本文突出了CAR-HEMATOTOX评分对接受BCMA指导的CAR-T的多发性骨髓瘤患者的毒性和治疗反应的预后效用。
BCMA指导的CAR-T代表了r/r多发性骨髓瘤患者的改变实践的免疫治疗平台。尽管如此,它与独特的毒性概况有关,包括细胞因子释放综合征(CRS)和免疫效应细胞相关神经毒性综合征(ICANS)。现实世界的证据进一步强调了血液毒性的重要性,指的是严重和/或长期的细胞减少,这种细胞减少在淋巴细胞化疗和临床CRS解决后可以持续很长时间。
血毒性不仅代表了CAR-T最常遇到的≥3级毒性,而且还极大地促进了驱动传染性并发症的多模式免疫抑制(例如细胞和体液结合)。随着CRS和ICANS毒性管理的进步,致命感染现在是CAR-T治疗后非复发死亡(NRM)的最常见原因。
早期血液毒性是由于CAR-T给药前应用的淋巴排毒化疗,在其他没有CAR T细胞的疾病环境中也有报道。此外,CAR-T相关血毒性的独特特征源于观察到中性粒细胞和血小板恢复通常遵循双相轨迹,瞬时恢复后有第二次下降。此外,最近的报告将高级CRS和相关的炎症标志物与长期的细胞减少症联系起来,支持炎症侮辱发挥相关病理生理学作用的观点。
之前开发了CAR-HEMATOTOX(HT)评分,以模拟r/r大型B细胞淋巴瘤(LBCL)患者队列中的CAR-T相关血毒性。该分数是在淋巴结肿之前计算的,并整合了与CAR-T前造血储备(如血红蛋白、绝对中性粒细胞计数[ANC]、血小板计数)和炎症状态(例如C反应蛋白[CRP],铁蛋白)。值得注意的是,该评分与重症感染率增加,特别是细菌感染,以及LBCL患者在三线接受商业CD19指导的CAR-T治疗结果不佳有关。
然而,目前还不清楚HT评分是否也对接受十二囊肿(ide-cel)或胞嘧啶酶原细胞(cytta-cel)的多发性骨髓瘤患者的毒性事件和临床结果的风险分层。此外,BCMA CAR-T后细胞减少症和感染率的真实世界报告仍然很少。2023年7月31日发表在Journal of Hematology & Oncology的文章,研究了CAR-HEMATOTOX(HT)评分对预测接受标准护理的十二钴基因和自体白细胞雄酮患者的毒性和生存结果的实用性。

研究人员追溯收集了2021年4月至2022年7月期间在六个国际CAR-T中心接受治疗的113名r/r多发性骨髓瘤患者的数据。HT评分由与造血储备和基线炎症状态相关的因素组成,在淋巴排瘫化疗之前确定。
研究结果显示,在淋巴结肿时,63名患者为HT低(得分0-1),50名患者为HT高(得分≥2)。与HTlow患者相比,HThigh患者表现出长期严重的中性粒细胞减少(中位数9与3天,p < 0.001),严重感染率增加(40%与5%,p < 0.001),以及更严重的ICANS(等级≥3:16%与0%,p <0.001)。
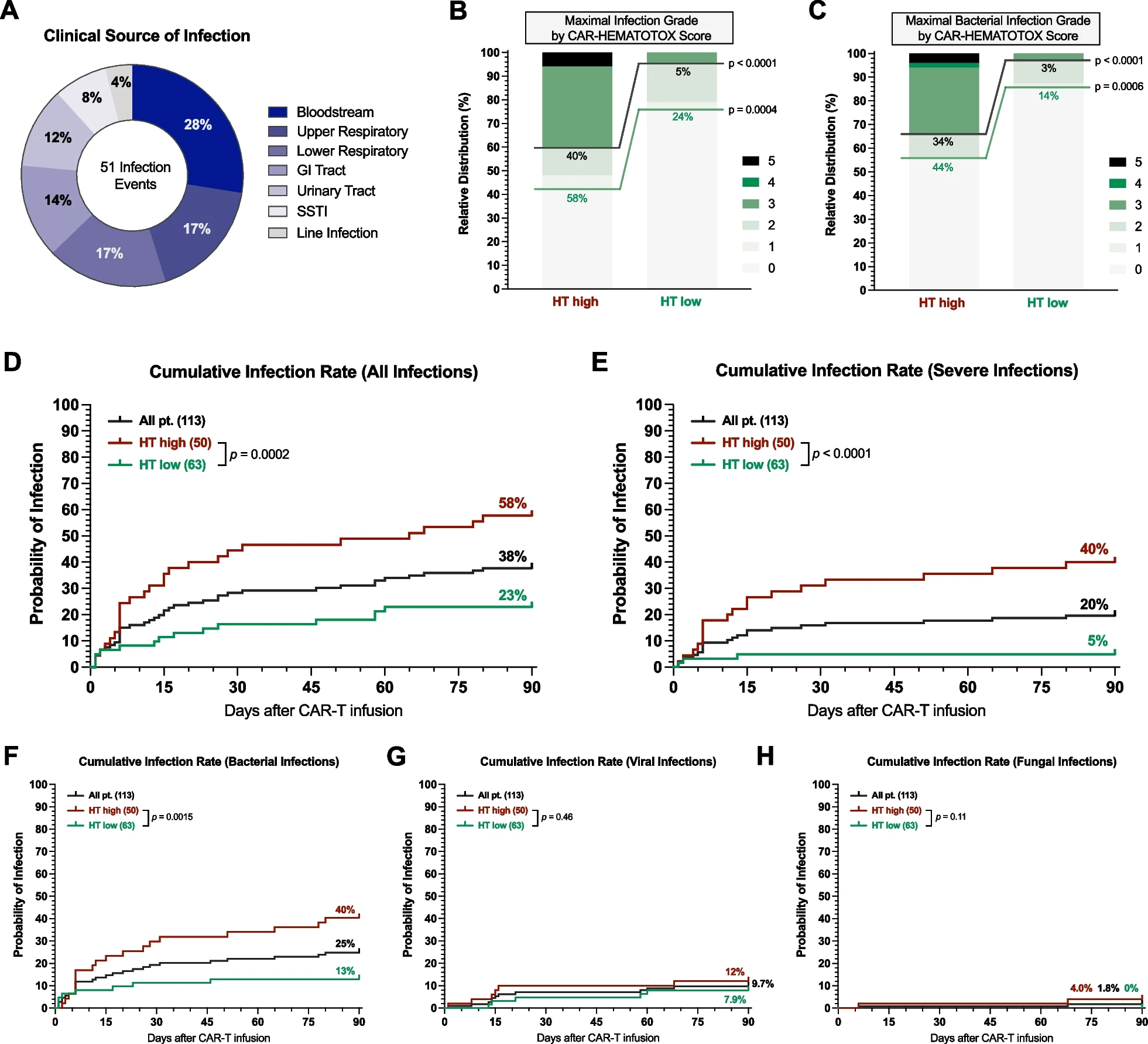
CAR-HEMATOTOX评分确定了有严重传染性并发症风险的患者
HThigh组一年非复发死亡率更高(13%对2%,p = 0.019),主要归因于致命感染。根据IMWG标准,HTlow患者的响应率更高(≥VGPR:70%对44%,p = 0.01)。相反,HThigh患者表现出较低的无进展(中位数5与15个月,p <0.001)和总生存率(中位数10.5个月与未达到,p <0.001)。
综上所述,CAR-HEMATOTOX评分代表了淋巴结肿之前严重毒性和临床结果的有力风险分层因素,值得进一步的前瞻性验证。该分数可以根据每个患者的个人风险状况为CAR-T相关毒性提供量身定制的干预措施,并帮助确定需要组合和/或新型治疗策略的CAR-T候选人。
原始出处
Rejeski, K., Hansen, D.K., Bansal, R. et al. The CAR-HEMATOTOX score as a prognostic model of toxicity and response in patients receiving BCMA-directed CAR-T for relapsed/refractory multiple myeloma. J Hematol Oncol 16, 88 (2023). https://doi.org/10.1186/s13045-023-01465-x
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言











