痛风治疗重磅 3 期数据公布,引领靶向治疗新格局
2024-06-20 梅斯风湿新前沿 梅斯风湿新前沿 发表于上海
多替诺雷片(Dotinurad)是一种促使尿酸排泄的药物,此前已于2020年在日本上市,用于治疗高尿酸血症和痛风。2024年1月20日,卫材中国已成功申报多替诺雷片的上市,该药品属于注册分类5.1类,
多替诺雷片(Dotinurad)是一种促使尿酸排泄的药物,此前已于2020年在日本上市,用于治疗高尿酸血症和痛风。2024年1月20日,卫材中国已成功申报多替诺雷片的上市,该药品属于注册分类5.1类,并已受到正式受理。
2024年EULAR大会上北京大学第一医院张卓莉教授作为Leading PI 汇报了最新的中国三期临床试验数据。基于此背景,梅斯风湿新前沿特邀参与此项临床试验的张卓莉教授、中国科学技术大学附属第一医院安徽省立医院厉小梅教授和华中科技大学同济医学院附属同济医院董凌莉教授接受访谈,与我们一起共话痛风的临床管理以及治疗进展。
点击观看三位专家的访谈合集
基于实际
剖析痛风诊疗现状
Q:我国痛风的发病率和患病率呈逐年上升趋势,逐渐成为一个重要的公共卫生问题。请您谈一谈目前我国高尿酸血症以及痛风的诊疗现状。
A:张卓莉教授:
当前,我国高尿酸血症和痛风的患病状况呈现出两大显著特征:一是发病率呈逐年上升趋势,我国成人高尿酸血症的患病率已高达14%,痛风发病率为 1.1%1;二是患者群体日益年轻化。继“三高”之后,高尿酸已然成为威胁健康的“第四高”,亟待引起社会广泛关注并予以解决。
在当前的诊疗实践中,我们面临着三大主要问题:首先,患者普遍缺乏对疾病的重视和治疗依从性,加强患者教育至关重要。其次,临床诊疗规范化水平有待提高。需加强医生培训和教育,提高疾病认知和诊疗技能。最后,在风湿免疫疾病的治疗领域,痛风的治疗进展相对滞后,针对痛风的治疗手段仍显不足。
然而,值得欣喜的是,最近一款新型药物——选择性URAT 1抑制剂(多替诺雷)已在中国成功申报上市并得到了正式受理。多替诺雷在多项临床试验中已展现出良好的有效性和安全性。作为该药物三期临床试验的Leading PI,我对其未来的上市前景充满期待,并相信它将为广大痛风患者带来更为显著的疗效和福祉。
知己知彼
痛风对人体的影响远不止关节
Q:请问痛风对人体的影响体现在哪些方面?有哪些危害?
厉小梅教授:
痛风作为一种常见的炎症性关节疾病,在临床中,往往伴随着高尿酸血症的出现。血尿酸随着血液循环遍布人体各个组织部位,当尿酸盐结晶沉积在滑膜上时,可能导致关节炎症的急性发作;当沉积在软组织中,形成痛风石。
同时,尿酸在血液循环过程中,通过肾小球滤过肾小管排泌的过程中,可能积聚在肾小管内,形成尿酸盐结晶,部分患者甚至可能出现肾结石,表现为急性肾绞痛,小便中可能出现血尿或蛋白尿。在严重的情况下,患者可能发展为严重的痛风性肾病甚至肾功能不全,需要接受透析治疗。
此外,高尿酸血症也是糖尿病的独立危险因素之一2,血尿酸每增加1 mg/dL,糖尿病的新发风险增加17%3;在心血管事件中,高尿酸血症患者冠心病的发生率更高4;高尿酸血症也是动脉粥样硬化的主要诱发因素之一5。
翻开新篇
达标治疗引领痛风治疗新风向
Q:降尿酸贯穿着痛风治疗的始终,请问如何制定降尿酸治疗的目标?
厉小梅教授:
2016年欧洲抗风湿病联盟(EULAR)首次在痛风领域内推出达标治疗的理念6,标志着痛风治疗进入了一个全新的阶段,为痛风治疗提供了明确的目标和方向,使得治疗更加精准、有效。
合理的药物选择是痛风达标治疗的关键,目前,临床上仅有几种药物,远不能满足当下的治疗需求。而新的药品多替诺雷的出现,为我们控制尿酸提供了一种新的武器,能够帮助我们将血尿酸平稳控制在理想范围内。
一般来说,将血尿酸控制在360 μmol/L以下有助于尿酸盐结晶的释放,同时抑制其合成7。然而,对于伴有痛风石或肾结石的患者,我们要求血尿酸水平控制在300 μmol/L以下,以促进结晶的溶解7。
需要注意的是,血尿酸水平并非越低越好,为防止增加患阿尔茨海默病等神经退行性疾病的风险,降尿酸治疗时,血尿酸不低于180 μmol/L7。
精准直击
高选择性关键靶点安全又有效
Q:现有哪些药物可以用于降尿酸治疗,它们的作用机制是什么,未来是否有哪些新药值得我们期待?
董凌莉教授:
当前我国可使用的降尿酸药物主要包括抑制尿酸合成的别嘌醇和非布司他,以及促进尿酸排泄的苯溴马隆。别嘌醇和非布司他同为黄嘌呤氧化酶抑制剂,主要适用于尿酸生成增多的患者群体。苯溴马隆通过抑制肾近端小管尿酸转运蛋白1(URAT 1),进而抑制肾小管对尿酸的重吸收,从而促进尿酸的排泄,更适用于肾尿酸排泄减少所致的高尿酸血症及痛风患者。
总体而言,当前临床上针对降低尿酸水平的药物选择范围相对有限。然而,值得欣慰的是,目前已有众多具有广阔应用前景的新型药物正处于积极研发阶段。其中,针对URAT1靶点的研究已成为研发热点之一。选择性URAT 1抑制剂多替诺雷已顺利完成中国的三期临床试验,并已递交上市申请,其潜在疗效和应用前景值得期待。
尿酸转运蛋白(URAT)作为参与尿酸重吸收的主要蛋白,承担着约90%的尿酸重吸收任务8,因此在维持血尿酸水平方面发挥着至关重要的作用。其中,URAT 1通过与其他阴离子交换实现尿酸转运,对尿酸转运具有高度特异性。因此,通过抑制URAT 1可有效减少尿酸的重吸收,成为促进尿酸排泄药物研发的关键靶点。
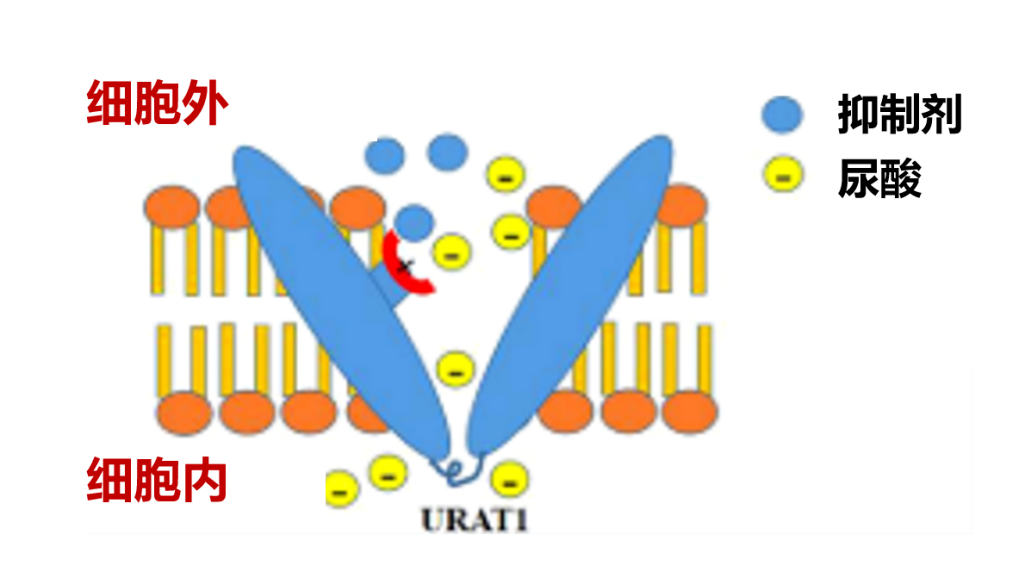
URAT1抑制剂通过与尿酸竞争相同的结合位点来抑制尿酸转运
除了肾脏外,肝脏、脂肪组织以及血管内皮细胞等亦存在URAT 1的表达,这解释了尿酸为何能进入这些细胞并引发一系列病理生理反应,如细胞功能障碍、细胞因子分泌增加、炎症反应及脂代谢紊乱等。
在药物研发领域,URAT 1选择性抑制剂与非选择性抑制剂的主要区别在于其靶点作用的精准性。非选择性抑制剂在抑制URAT 1的同时,亦可能对OAT 1/3和ABCG 2产生抑制作用。然而,这些蛋白同样参与尿酸的转运过程,并在肾脏排泄尿酸中发挥着关键作用。因此,非选择性抑制剂在抑制尿酸重吸收的同时,亦可能干扰尿酸的正常排泄过程。
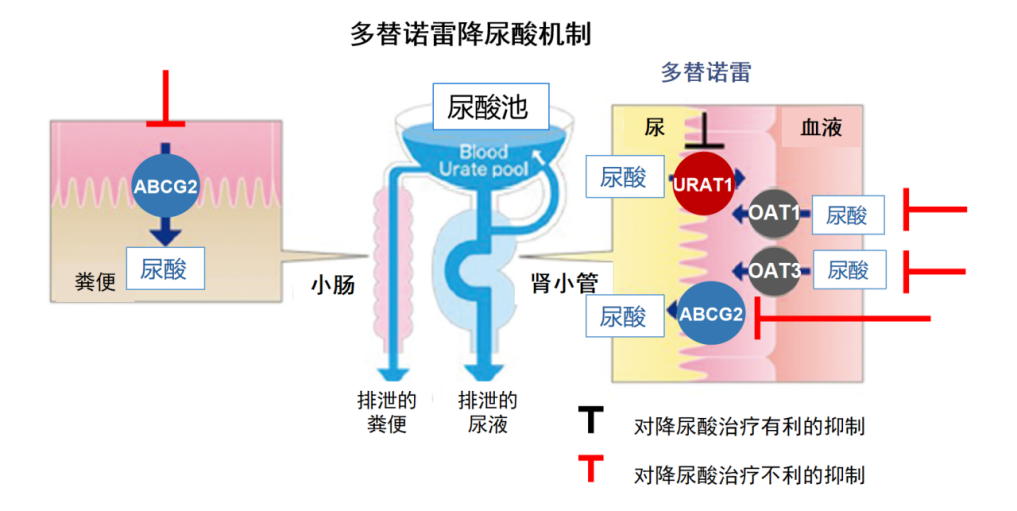
ULT, urate lowering therapy, 降尿酸治疗;urate, 尿酸盐; URAT1, urate transporter 1, 尿酸转运体1; OAT1/3, organic anion transporter 1/3,有机阴离子转运蛋白1/3; ABCG2, ATP-binding cassette subfamily G member 2, ATP 结合盒G亚家族成员2
而选择性URAT 1抑制剂展现出更高的URAT 1选择性,对ABCG 2的抑制作用相对微弱9。因此,该类药物在降低血尿酸方面表现出更高的效率,且不会对肠ABCG 2及小肠相关的肾外排泄产生负面影响,从而减轻肾脏负担。
另一方面,ABCG 2和OAT 1/3还承担着尿毒症毒素(如硫酸吲哚酚,IS)的排泄功能5。抑制这些通路可能对肾脏和血管内皮细胞产生不利影响,进而参与慢性肾脏病(CKD)和心血管疾病(CVD)的进展。而选择性URAT1抑制,如多替诺雷,其特性在于不抑制ABCG 2和OAT 1/3,因此不会引发血中毒素的增加,并有助于减少肾内尿酸的蓄积9。因此,多替诺雷的使用可能有助于降低CKD和CVD的发生和发展风险。
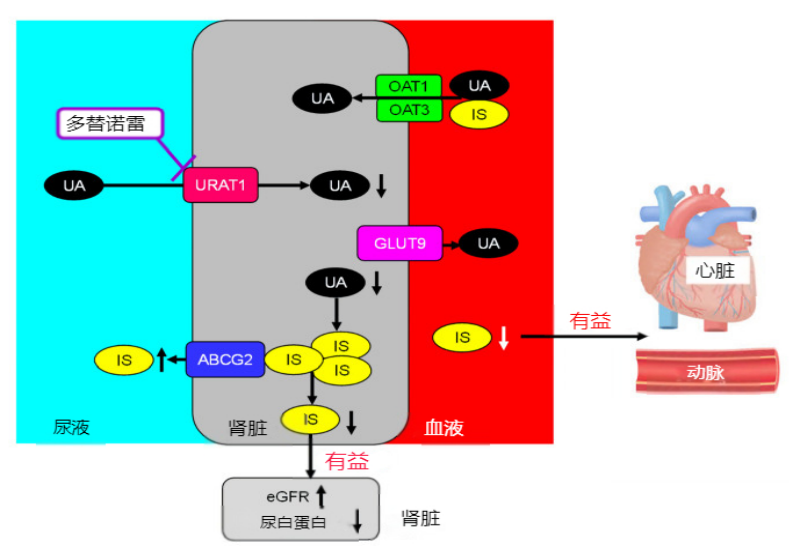
UA, Uric Acid,尿酸;GLUT9,glucose transporter 9,人葡萄糖转运蛋白9;IS, Indoxyl sulfate, 硫酸吲哚酚
前景广阔
多替诺雷中国三期数据新鲜出炉
Q:您在本次EULAR会议上公布了多替诺雷中国最新的三期临床试验数据,能否请您为我们划一下重点?
多替诺雷三期临床试验数据解读
张卓莉教授:
多替诺雷作为一种选择性的URAT 1抑制剂,其在尿酸代谢调控方面的作用已得到广泛认可。目前,多替诺雷在中国已完成三期临床研究10,我有幸作为中国的Leading PI参与了此项研究。该研究主要聚焦于多替诺雷与非布司他之间的优效性对比。研究覆盖了全国30个中心,共纳入451例合并有高尿酸血症的痛风患者,历时24周。
研究的主要终点设定为在24周时血尿酸小于等于6mg/dl的患者的比例。研究结果显示,多替诺雷4mg组在24周时的达标率高达73.6%,而非布司他40 mg组的达标率仅为38.1%,显示出多替诺雷在降尿酸方面的显著优势。
此外,研究还关注了其他次要终点,如12周时多替诺雷2mg组与非布司他40mg组在血尿酸水平降低方面的比较。尽管在统计学上未达到显著差异,但多替诺雷2mg组在12周时的达标率仍略高于非布司他组,显示出其良好的疗效。
除了疗效外,多替诺雷的安全性也是研究关注的重点。在24周的临床研究中,多替诺雷组和非布司他组治疗期间出现的不良事件(TEAE)发生率相似,重度和严重不良事件发生率较低,且多替诺雷组无研究药物相关的SAE。这表明多替诺雷在治疗高尿酸血症痛风患者时具有相对较好的安全性。
综上所述,多替诺雷作为一种新型的URAT 1抑制剂,在降尿酸方面表现出优异的疗效和安全性。其三期临床研究结果的公布为中国痛风患者的降尿酸治疗带来了新的希望。
作为首个在中国完成的关于URAT 1抑制剂在痛风中的临床研究,该研究不仅引起了广泛关注,也为未来痛风治疗领域的发展奠定了坚实基础,目前,多替诺雷已经成功申报多替诺雷片的上市,并已受到正式受理。
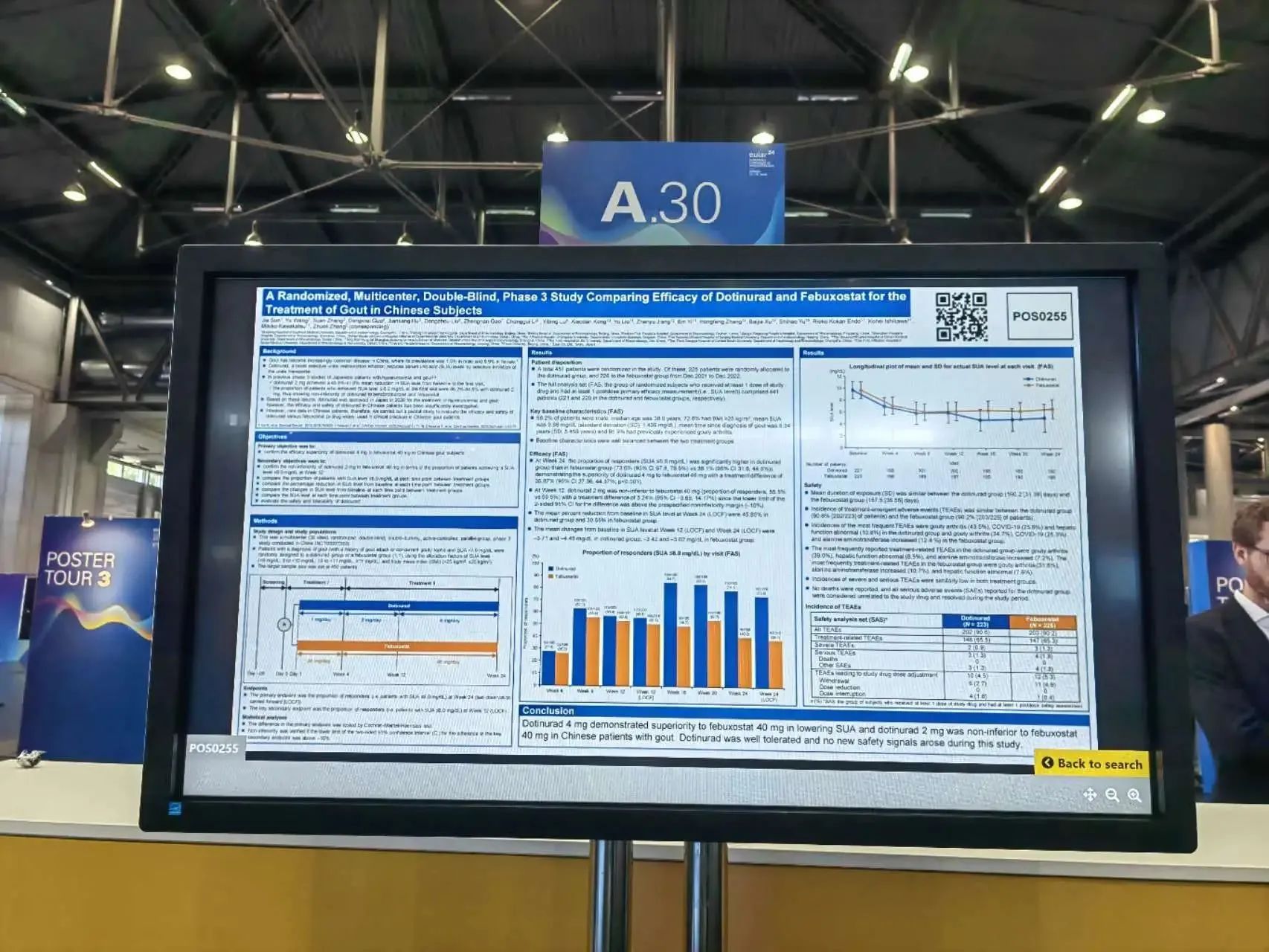
在EULAR上展示的相关壁报
展望未来
拓展精准治疗版图,助推个体化疾病管理
Q:目前痛风还有哪些未被满足的临床需求,您认为未来在痛风领域的突破口在哪里?
董凌莉教授:
针对痛风发病机制的深入研究将是关键所在。通过深入探索痛风的发病机理,有望为痛风的治疗提供更为精准和有效的靶点,从而开发出更具针对性的治疗药物。基于多替诺雷的精准、明确的作用机制,坚实的疗效证据以及可靠的安全性,若能够在中国顺利获批,则能在痛风的临床治疗中占有一席之地,助力中国痛风诊疗的发展,造福于更多的痛风患者。
厉小梅教授:
痛风作为一种普遍存在的炎症性关节疾病,其临床治疗在药物选择方面目前仍显有限。当前主要的治疗手段包括抑制尿酸合成的药物、促进尿酸排泄的药物以及部分尿酸酶类药物。然而,这些药物并不能完全解决所有痛风患者的治疗需求。
尽管药物的多样化为临床医生在治疗痛风过程中提供了有力的支持,但值得注意的是,痛风患者的发病过程因个体差异而异,并非所有患者都适用相同的药物。近期,我们参与了新上市药物多替诺雷的三期临床研究,这是一种排尿酸药物。从现有的数据来看,其在降尿酸治疗痛风方面的三期临床结果令人鼓舞。
多替诺雷的加入,无疑为我们在临床治疗痛风方面增添了一个有力的新武器,有望为更多患者带来福音。
张卓莉教授:
加强痛风疾病的预防和控制工作是至关重要的。为了从源头上减少痛风的发生,我们应致力于提升公众对痛风疾病的认识,积极推广健康的生活方式和饮食习惯,并加强高尿酸血症等痛风前驱疾病的筛查与管理。
同时,我们必须高度重视医生队伍的建设,特别是广大普内科医生以及其他相关领域的医生。通过加强规范化的患者管理教育,我们旨在提升医生对高尿酸血症及痛风患者群体的认知,进而增强其早期诊断和规范化治疗的能力。
总之,只有医生和患者共同努力、携手合作,我们才能更有效地管理高尿酸血症和痛风患者,从而改善他们的长期健康状况和预后。
文章审核:张卓莉丨厉小梅丨董凌莉
张卓莉教授

厉小梅教授

董凌莉教授

[1] 中华医学会内分泌学分会. 中国高尿酸血症与痛风诊疗指南(2019)[J]. 中华内分泌代谢杂志,2020,36(1):1-13. DOI:10.3760/cma.j.issn.1000-6699.2020.01.001.
[2] Dehghan A, van Hoek M, Sijbrands EJ, Hofman A, Witteman JC. High serum uric acid as a novel risk factor for type 2 diabetes. Diabetes Care. 2008 Feb;31(2):361-2. doi: 10.2337/dc07-1276. Epub 2007 Oct 31. PMID: 17977935.
[3] Kodama S, Saito K, Yachi Y, Asumi M, Sugawara A, Totsuka K, Saito A, Sone H. Association between serum uric acid and development of type 2 diabetes. Diabetes Care. 2009 Sep;32(9):1737-42. doi: 10.2337/dc09-0288. Epub 2009 Jun 23. PMID: 19549729; PMCID: PMC2732137.
[4] 孙沙沙, 等. 中华老年心脑血管病杂志, 2020, 22(4): 368-371
[5] Yu W, Cheng JD. Uric Acid and Cardiovascular Disease: An Update From Molecular Mechanism to Clinical Perspective. Front Pharmacol. 2020 Nov 16;11:582680. doi: 10.3389/fphar.2020.582680. PMID: 33304270; PMCID: PMC7701250.
[6] Richette P, Doherty M, Pascual E, Barskova V, Becce F, Castañeda-Sanabria J, Coyfish M, Guillo S, Jansen TL, Janssens H, Lioté F, Mallen C, Nuki G, Perez-Ruiz F, Pimentao J, Punzi L, Pywell T, So A, Tausche AK, Uhlig T, Zavada J, Zhang W, Tubach F, Bardin T. 2016 updated EULAR evidence-based recommendations for the management of gout. Ann Rheum Dis. 2017 Jan;76(1):29-42. doi: 10.1136/annrheumdis-2016-209707. Epub 2016 Jul 25. PMID: 27457514.
[7] 徐东, 朱小霞, 邹和建, 等. 痛风诊疗规范[J]. 中华内科杂志, 2023, 62(9): 1068-1076. DOI: 10.3760/cma.j.cn112138-20221027-00796.
[8] Terkeltaub R, et al. Arthritis Res Ther. 2006;8 Suppl 1(Suppl 1):S4
[9] Ishikawa T, Takahashi T, Taniguchi T, Hosoya T. Dotinurad: a novel selective urate reabsorption inhibitor for the treatment of hyperuricemia and gout. Expert Opin Pharmacother. 2021 Aug;22(11):1397-1406. doi: 10.1080/14656566.2021.1918102. Epub 2021 Apr 30. PMID: 33926357.
[10] Z. Zhang,et al. Presented at EULAR 2024; Abstrac tPOS0255.DOI:10.1136/annrheumdis-2024-eular.104
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言














#痛风# #高尿酸血症#
62