南京大学医学院甘振继教授课题组揭示骨骼肌线粒体UPRmt 调控整体代谢的新机制
2022-07-31 南京大学医学院 南京大学医学院
骨骼肌线粒体UPRmt 通过ATF4 非依赖的机制长距离调节肝脏和脂肪代谢决定整体代谢健康。
代谢疾病已经成为我国重大的公共健康问题。肥胖、2型糖尿病、脂肪肝等代谢性疾病目前在我国呈迅猛高发之势,这严重影响国民身体健康和生活质量,造成了沉重的社会负担。作为人体最大的能量代谢和内分泌器官,骨骼肌对机体代谢平衡维持至关重要。研究表明骨骼肌代谢重塑是代谢疾病发生的控制器,对骨骼肌代谢重塑的调控模式深入研究有望为代谢性疾病的防治提供新理论和新策略。
骨骼肌是人体最大的糖脂代谢和内分泌器官,骨骼肌糖脂代谢及其与其他器官之间的代谢交流在机体代谢稳态维持中起着至关重要的作用。线粒体对骨骼肌代谢功能至关重要,骨骼肌线粒体需要精细的、多层次的质量监控系统来保障其功能。此前,甘振继教授课题组揭示了骨骼肌线粒体自噬通路在调节骨骼肌线粒体功能以及机体代谢稳态中起着至关重要的作用,发现了骨骼肌代谢调控中不为人知的“线粒体自噬调控肌肉-脂肪间的代谢交流”的重要作用模式。在此研究基础上,该课题组进一步探索骨骼肌线粒体质量控制的第一道防线——线粒体蛋白质稳态控制对肌肉代谢的影响。尽管线粒体UPRmt 在线虫中已经被广泛研究,但在哺乳动物体内的作用机制和生理功能仍不清楚。针对这一难题,作者综合应用了体内线粒体蛋白周转Mito-timer报告系统、未折叠蛋白化学小分子探针、高通量转录组/代谢组、基因敲除/转基因等遗传操作方法进行系统研究。发现骨骼肌线粒体蛋白酶LONP1的缺失可导致线粒体蛋白周转减缓,引起骨骼肌线粒体形态和功能异常。然而出乎意料的是,骨骼肌特异性的LONP1敲除小鼠显著抵抗高脂饮食诱导的肥胖,胰岛素抵抗和肝脏脂肪变性。为了确证线粒体蛋白质稳态控制与高脂饲喂诱导的肥胖之间的机制关联,作者还构建了另一种转基因小鼠模型,在肌肉中特异性过表达一种线粒体驻留的错误折叠蛋白——突变形式的鸟氨酸转氨甲酰酶(ΔOTC)。该转基因小鼠也展现出与LONP1肌肉缺失小鼠类似的整体代谢改善表型。进一步通过高通量的转录组学分析发现,骨骼肌中线粒体蛋白稳态失衡激活了UPRmt,介导了肌肉与脂肪及肝脏间的长距离交流,促进了高脂状态下脂肪和肝脏的代谢改善。此外,为了进一步探究骨骼肌UPRmt的机制,作者通过转录组学及代谢组学的联合分析,并结合骨骼肌特异性LONP1和转录因子ATF4双敲除的小鼠模型,系统阐明了骨骼肌线粒体UPRmt的作用模式。简言之,骨骼肌线粒体UPRmt通过ATF4通路调控肌肉氨基酸代谢和一碳代谢,而通过ATF4非依赖的方式长距离调节整体代谢稳态。
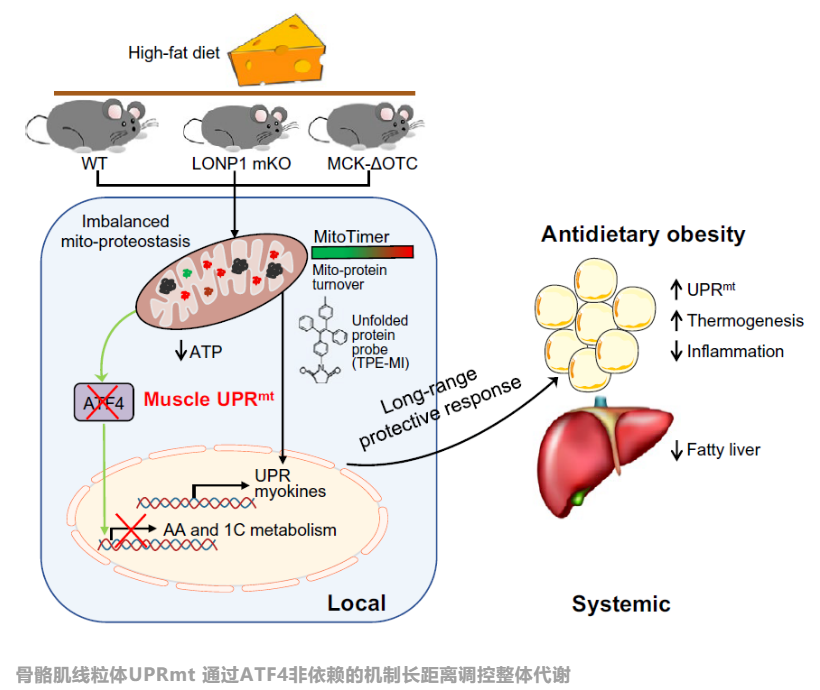
2022年7月27日,南京大学医学院甘振继课题组在Science Advances上在线发表了题为“Mitochondrial proteostasis stress in muscle drives a long-range protective response to alleviate dietary obesity independently of ATF4”的最新研究成果。这项研究定义了骨骼肌线粒体UPRmt, 揭示了UPRmt 在哺乳动物体内的新生理功能和作用机制,阐明了骨骼肌线粒体UPRmt 通过ATF4 非依赖的机制长距离调节肝脏和脂肪代谢决定整体代谢健康。南京大学医学院博士研究生郭奇奇和徐志圣为本文的共同第一作者,甘振继教授为该篇论文的通讯作者。该研究得到了国家自然科学基金委、科技部、教育部、江苏省科技厅以及中央高校等基金的支持,同时也得到合作实验室的大力协助与支持。

原文链接:
https://www.science.org/doi/10.1126/sciadv.abo0340
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言








好文
82
#南京大学#
65
#医学院#
71
#骨骼肌#
112
好文章,值得一读。
103