病例分享 | 腹膜后巨大去分化脂肪肉瘤一例
2024-04-24 上海阿克曼病理 上海阿克曼病理 发表于陕西省
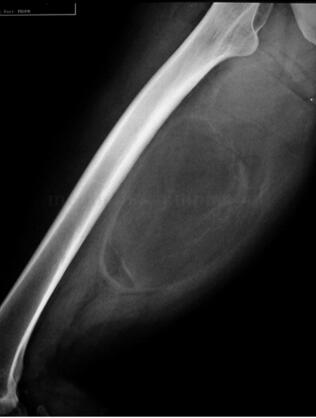
影像资料:MR提示腹腔巨大囊实性肿块并腹腔多发淋巴结转移,考虑来源于腹膜后恶性肿瘤。
病 史:
59岁,男性,因腹腔巨大占位来院治疗
影像资料:MR提示腹腔巨大囊实性肿块并腹腔多发淋巴结转移,考虑来源于腹膜后恶性肿瘤。
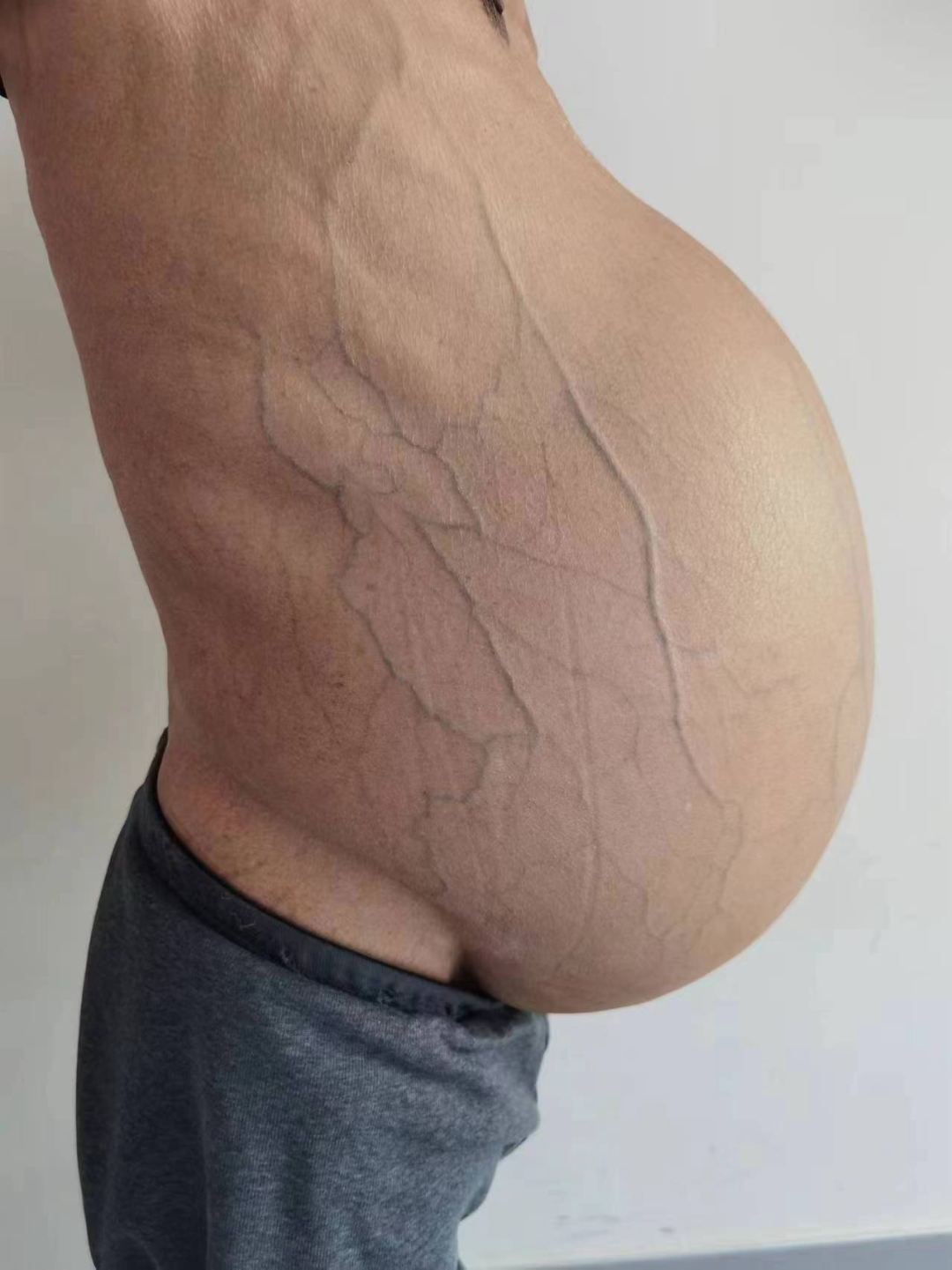
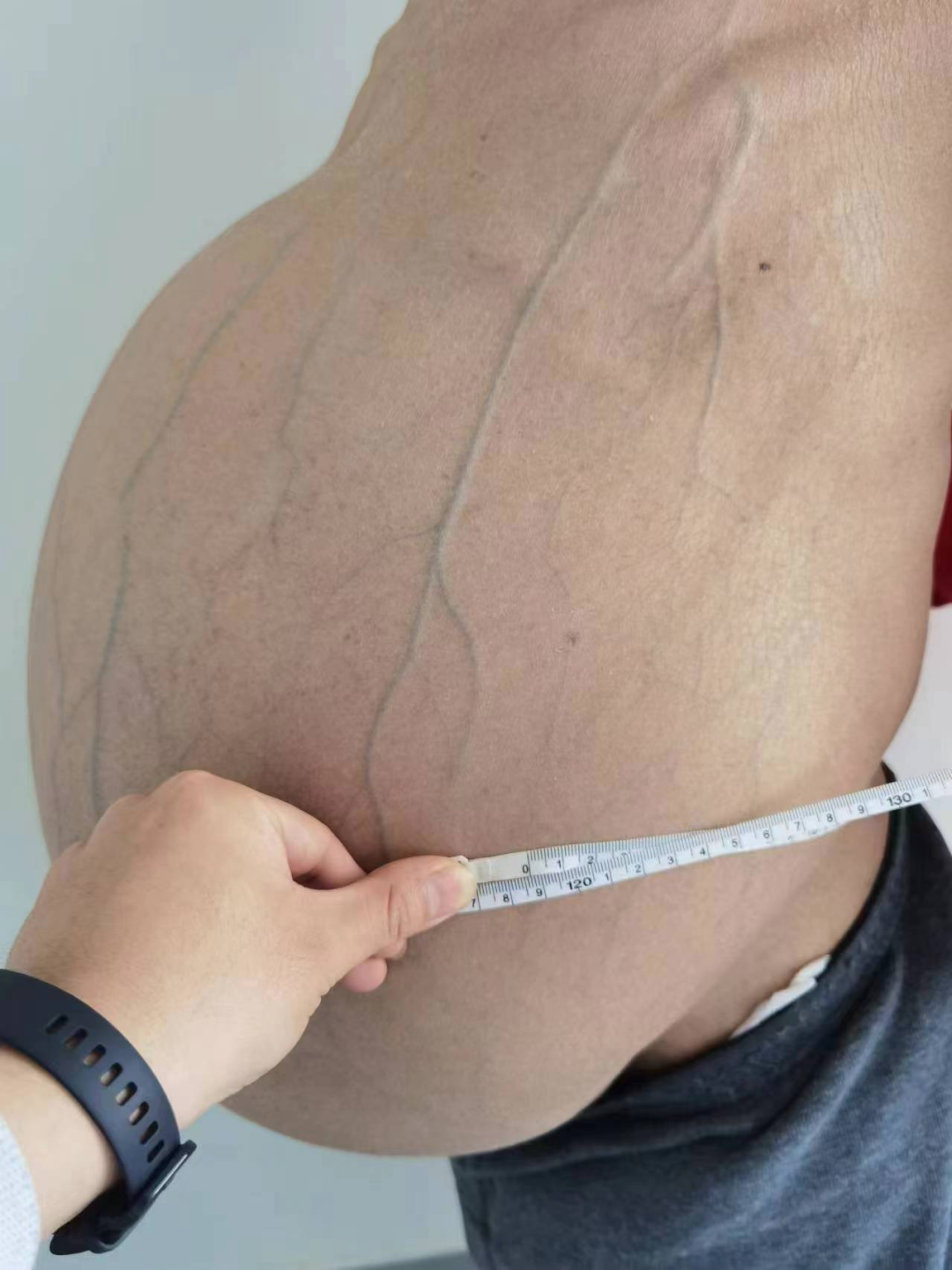
术前照:患者腹围达119cm,占据全腹腔和盆腔,腹壁静脉明显扩张。
手术所见:腹膜后巨大肿物,包膜完整,质软,活动度可,左肾、脾胃、小肠、结肠等脏器挤压移位严重,与部分结肠及系膜紧密相连,包裹左肾动静脉及部分降结肠。
病理检查:
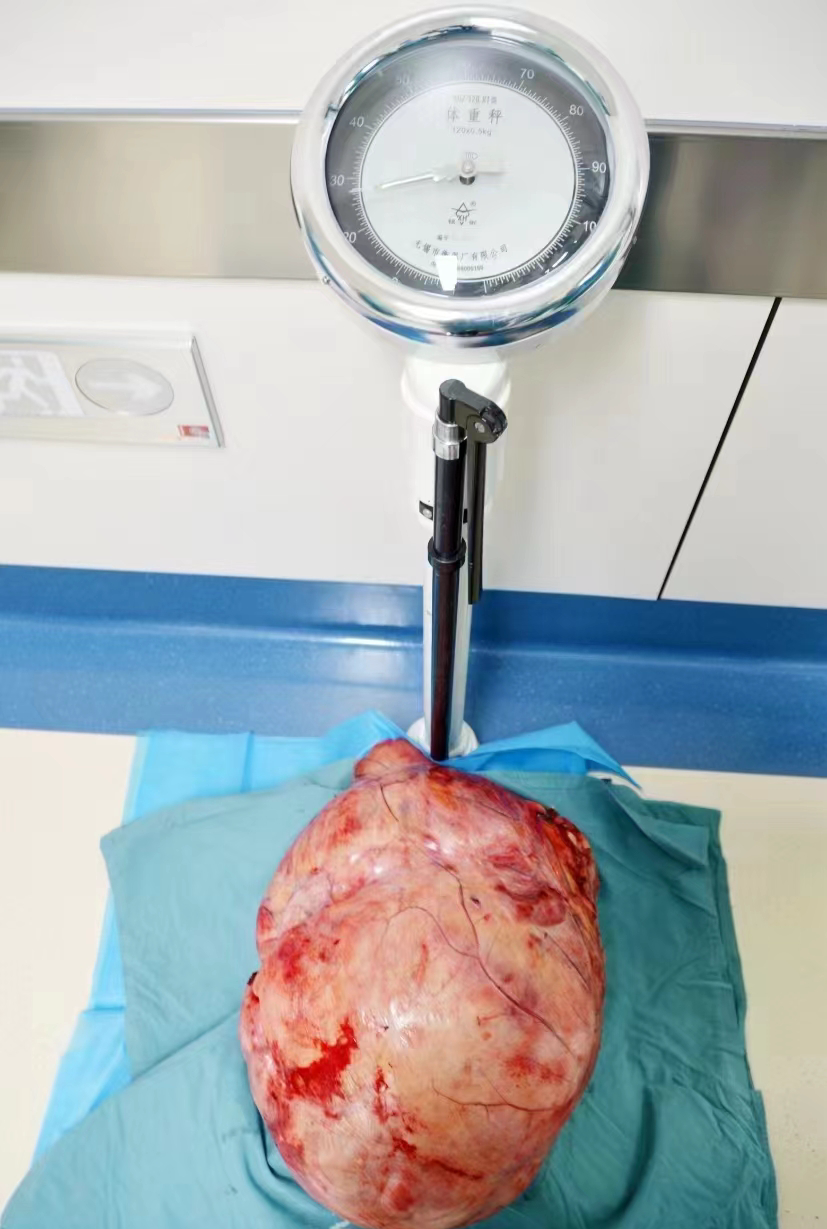
肉眼观:巨大灰黄包块一枚,体积:53cm×35cm×27cm,包膜完整,局部呈分叶状(图A),切面灰黄至灰褐,质软至韧,有油腻感,局部出血坏死,重约26kg(图B)。包块一侧局部粘连肠管一段,肠管长27cm,管径2cm;局部包裹粘连肾脏组织,肾脏体积:15cm×12cm×10cm,切面呈多房囊性,内充灰黄色液体,输尿管结构不清。

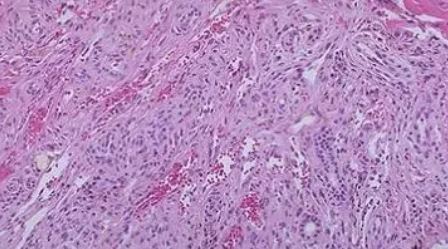
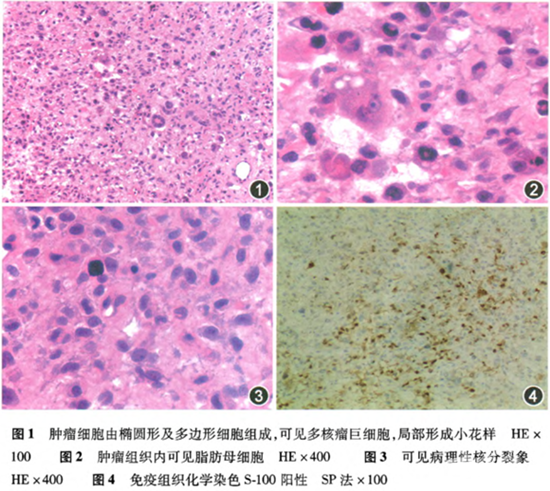
镜下特征:可见形态多样的高分化脂肪肉瘤区域与黏液纤维肉瘤成分或未分化多形性肉瘤成分混合存在,部分区域可见存在均匀的梭形细胞束状排列,伴有轻度异型性,表现为中等细胞密度部分区域瘤细胞密度增高,也可出现显著的黏液样间质形态及丰富的瘤巨细胞,异型性明显,核分裂象活跃伴片状坏死;局部出现脑膜皮细胞样形态,瘤细胞呈漩涡状排列,类似于神经增生或脑膜瘤形态。
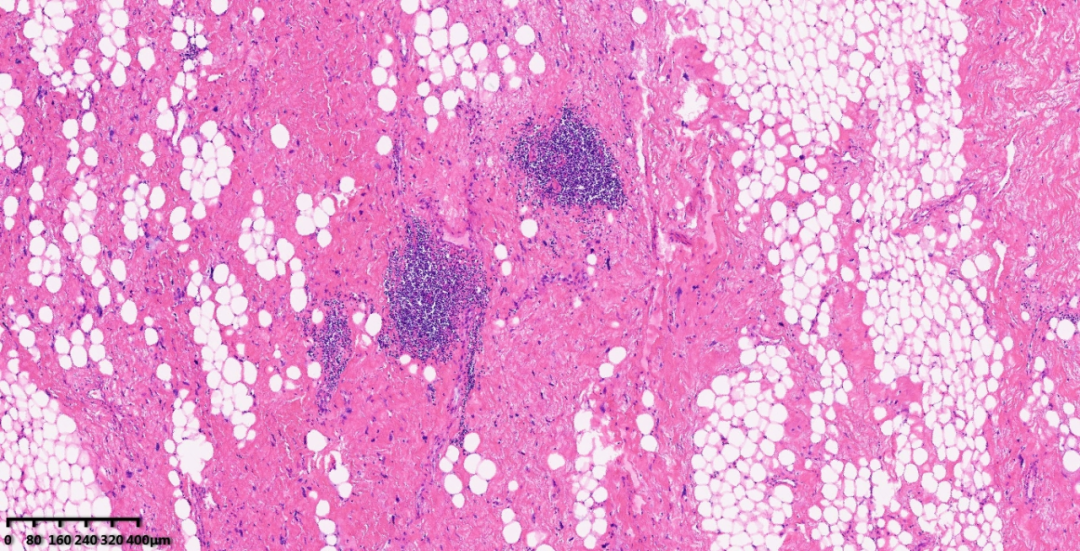
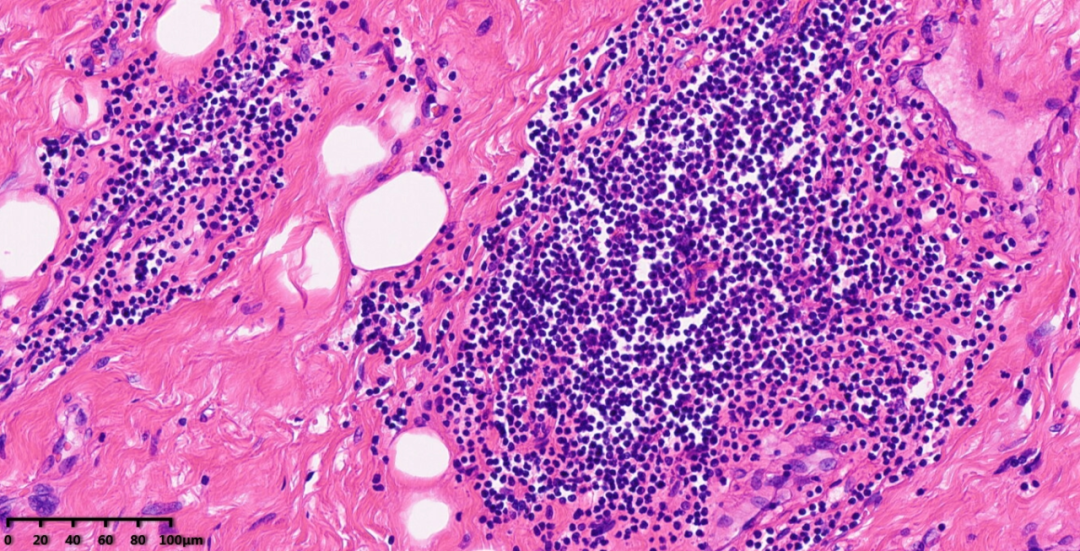
图1-2,低倍镜下,高分化脂肪肉瘤内含有数量不等的炎细胞浸润。中倍镜下,可见浸润的炎细胞以淋巴细胞为主,含少量浆细胞。
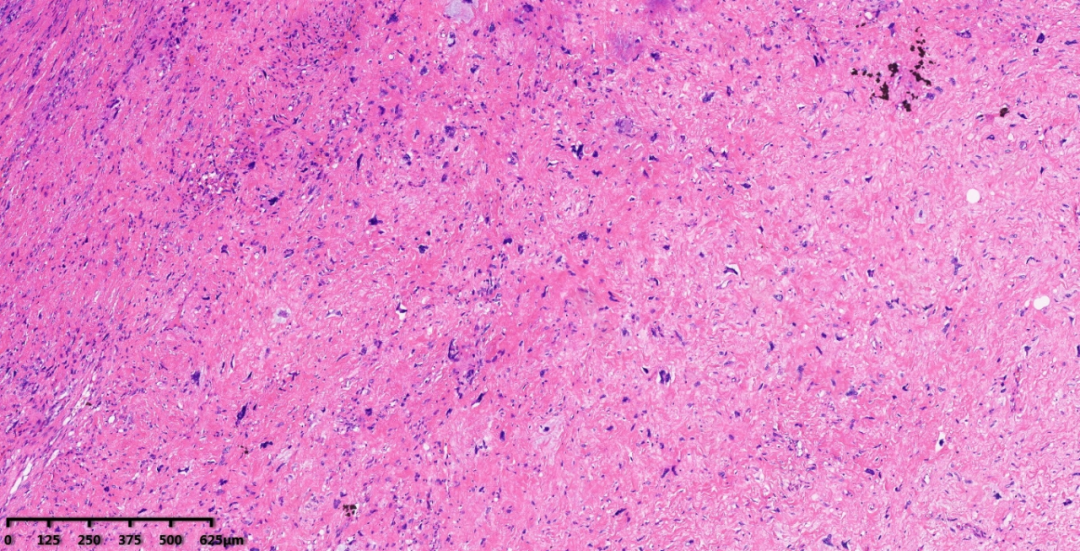
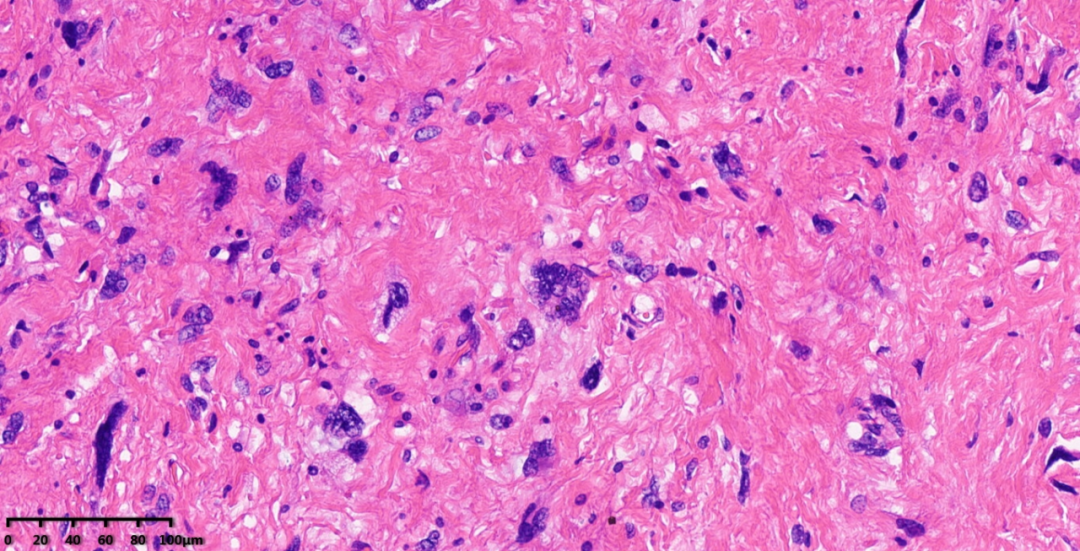
图3-4,低倍镜下,肿瘤组织内含有大片致密的胶原纤维化区域;中倍镜下可见纤维化区域内含有较多深染的奇异型细胞。
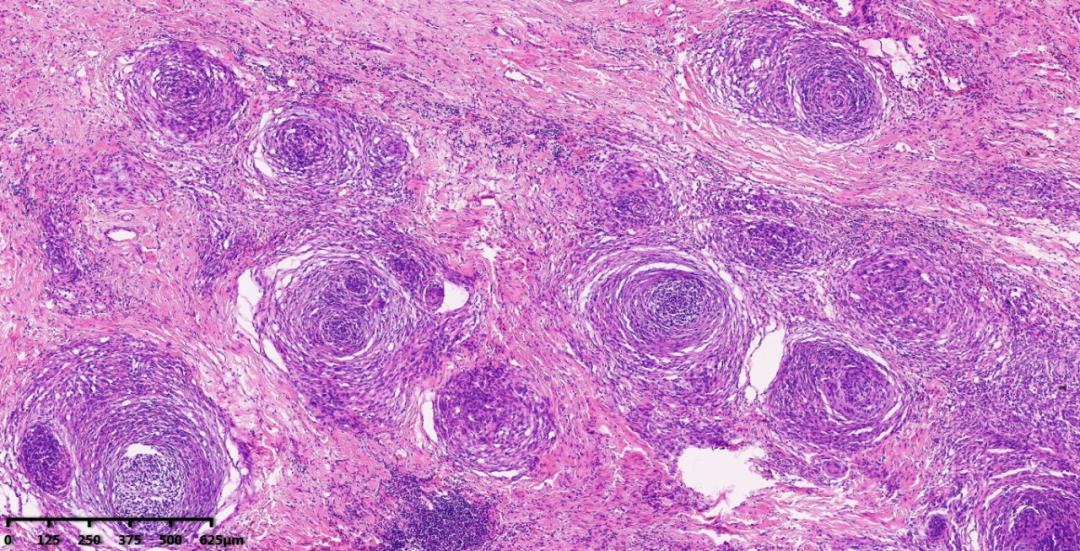
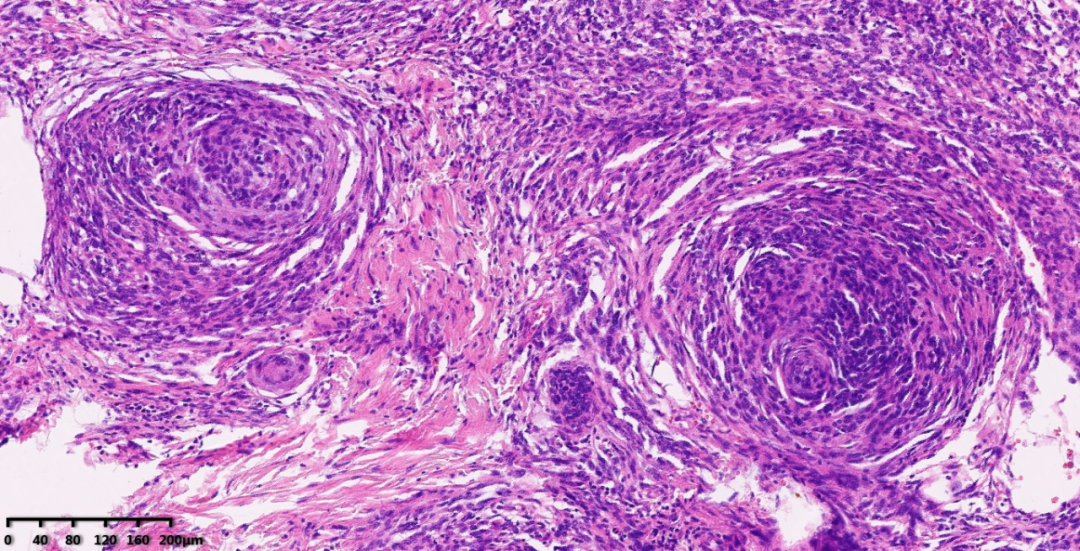
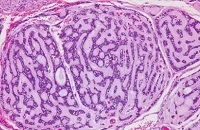
图5-6:低倍镜下,局部区域出现脑膜皮细胞样形态,瘤细胞呈漩涡状排列,类似于神经增生或脑膜瘤样形态。
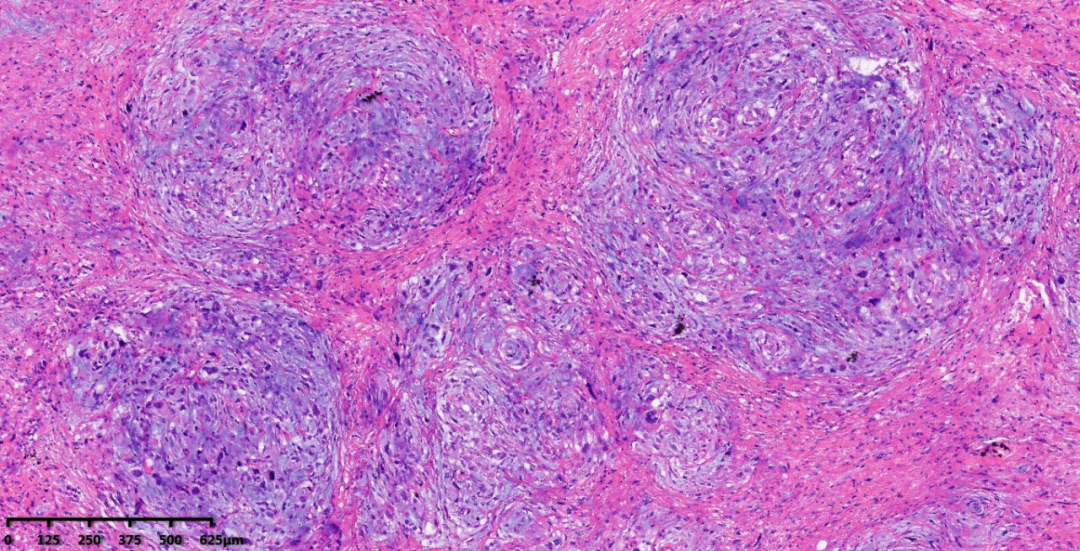

图7-8:低倍镜下,可见高分化脂肪肉瘤成分和黏液纤维肉瘤成分混合存在;中倍镜下,瘤细胞中等细胞密度,异型性明显,可见病理性核分裂象,间质显著黏液样变性,可见少量假脂肪母细胞。
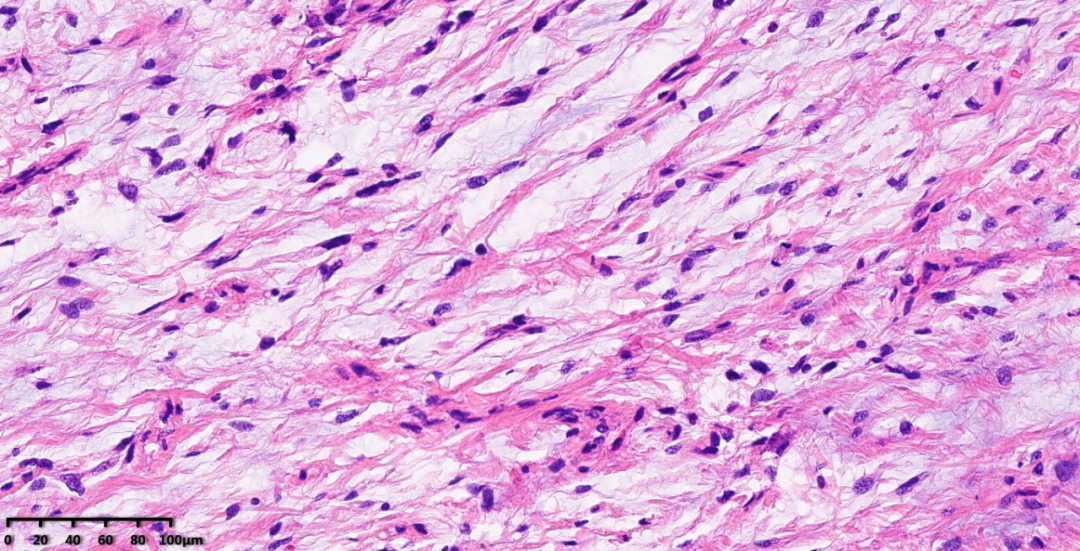
图9:中倍镜下,局部区域也有低细胞密度区,瘤细胞呈梭形、束状排列,核轻度异型性。
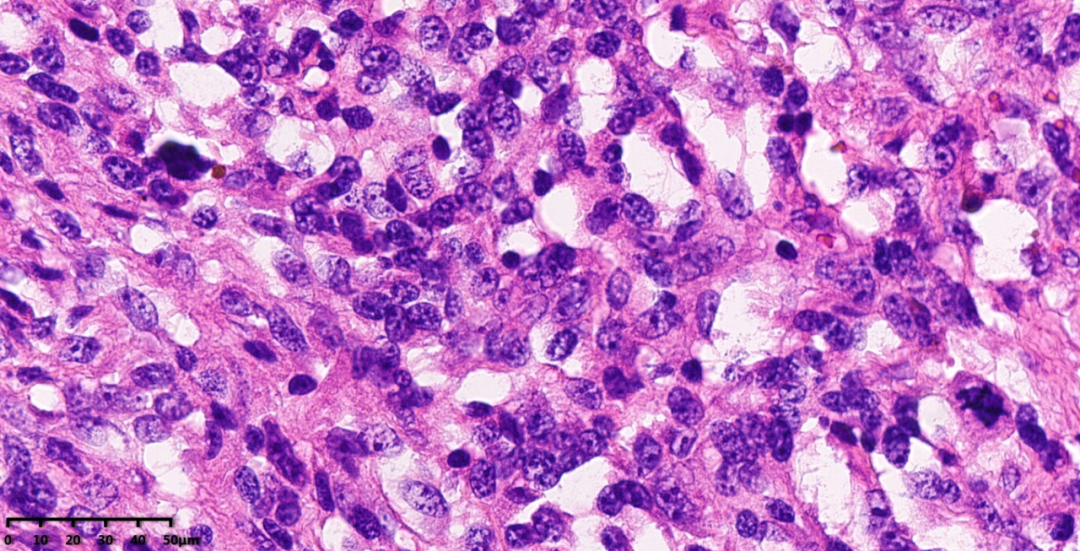
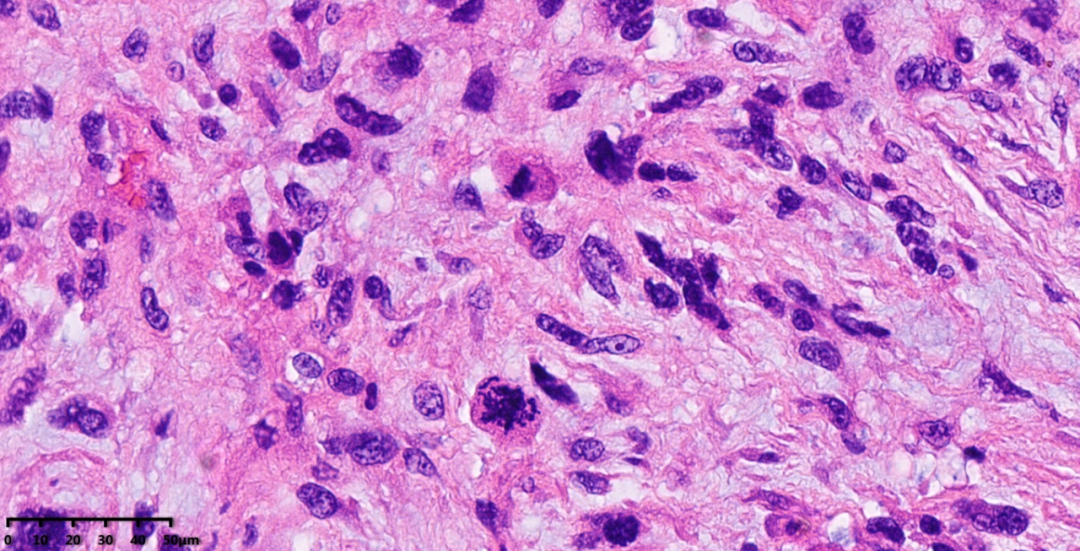
图10-11:高倍镜下,部分区域瘤细胞密度增加,异型性明显,核分裂象活跃
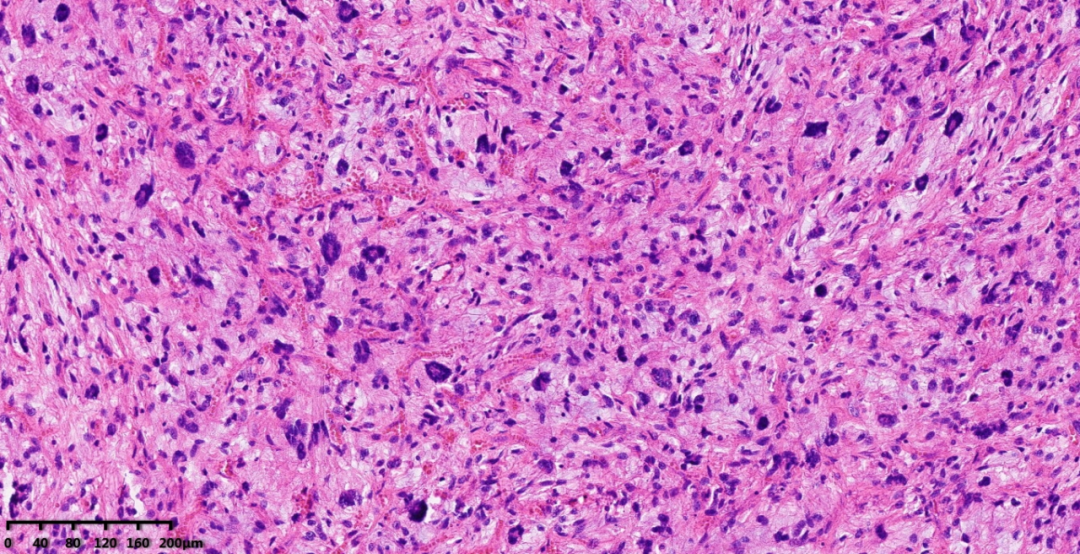
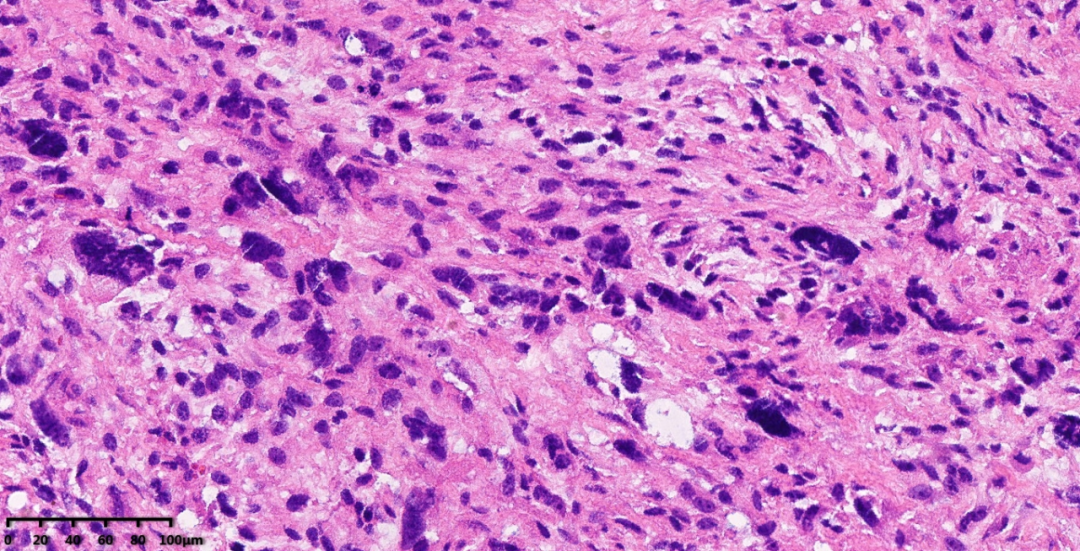
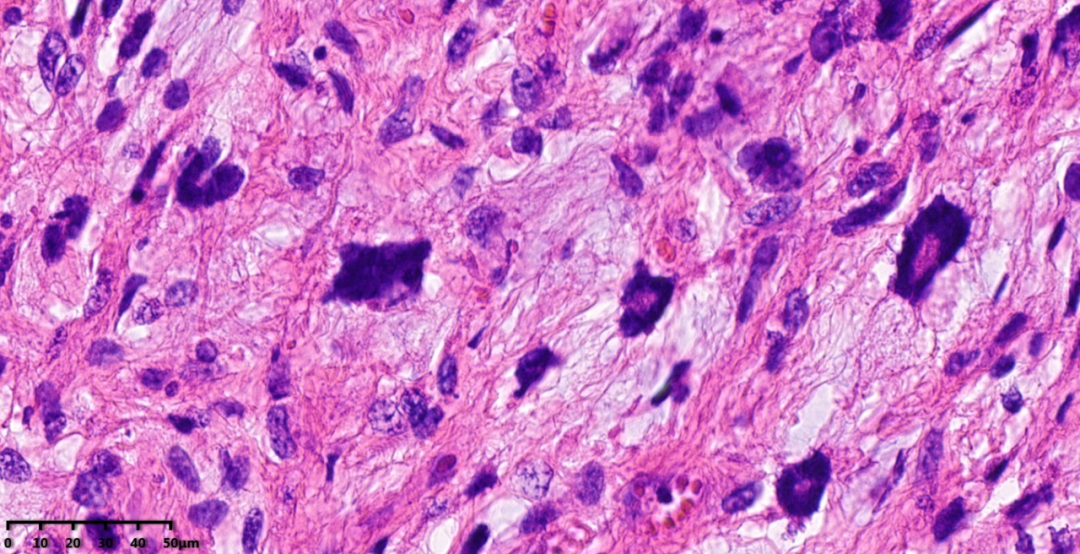
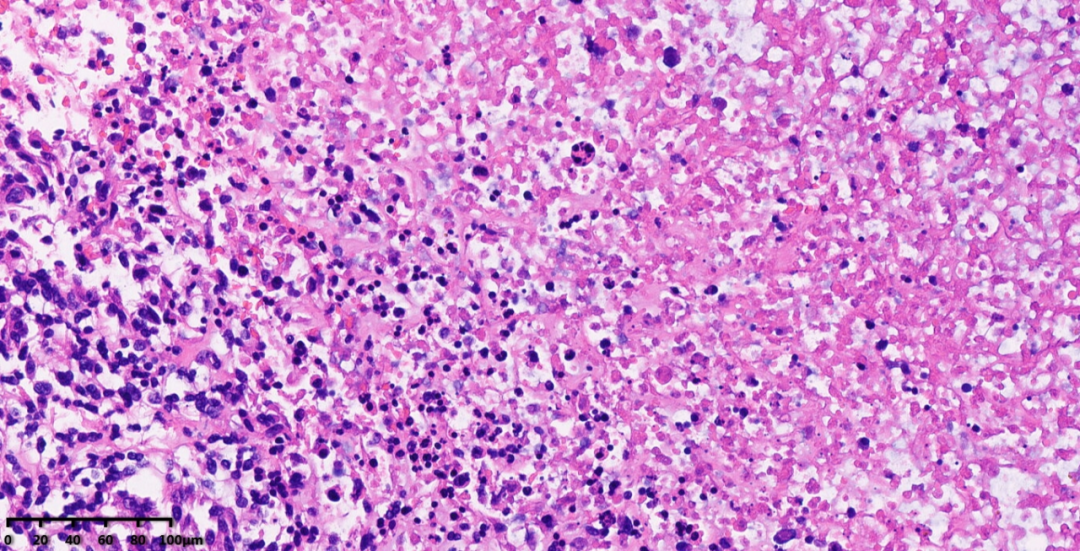
图12-15:瘤细胞呈不规则条束状或杂乱排列,瘤细胞异型性明显,可见核分裂象及大量奇异型瘤巨细胞,伴显著坏死,形态类似未分化多形性肉瘤。
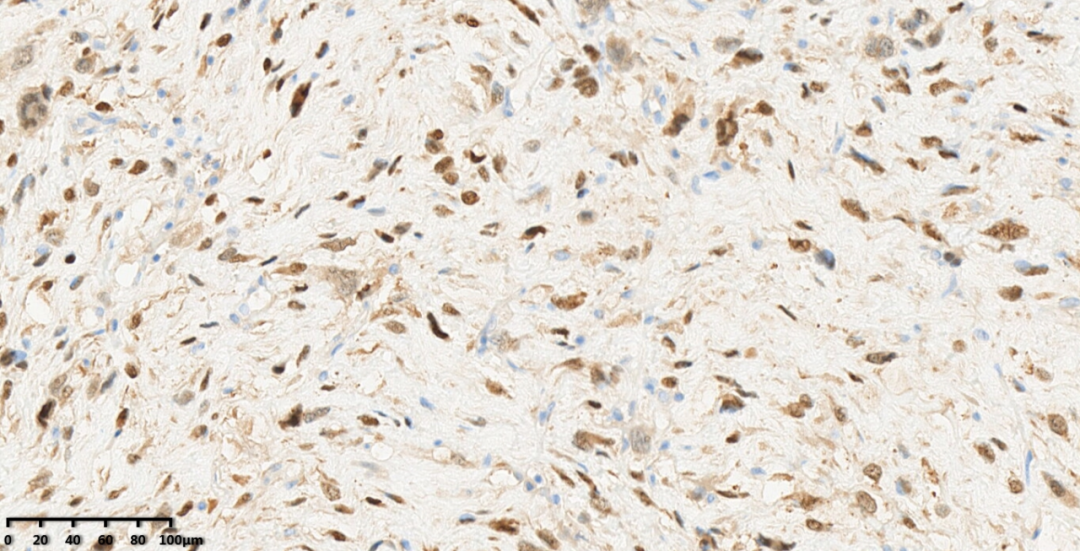
图16:肿瘤细胞表达CDK4标记。
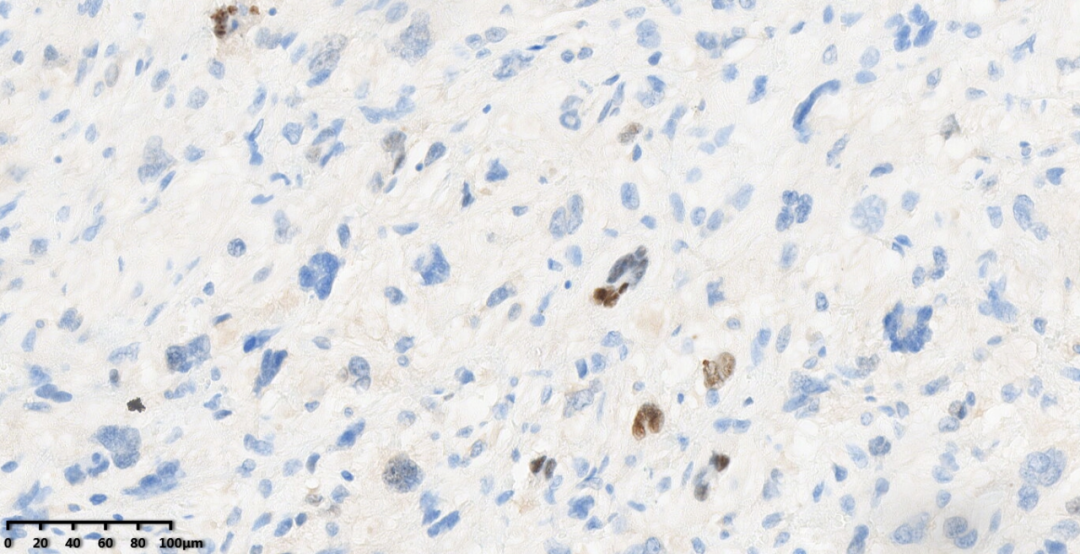
图17:个别肿瘤细胞表达MDM2标记。
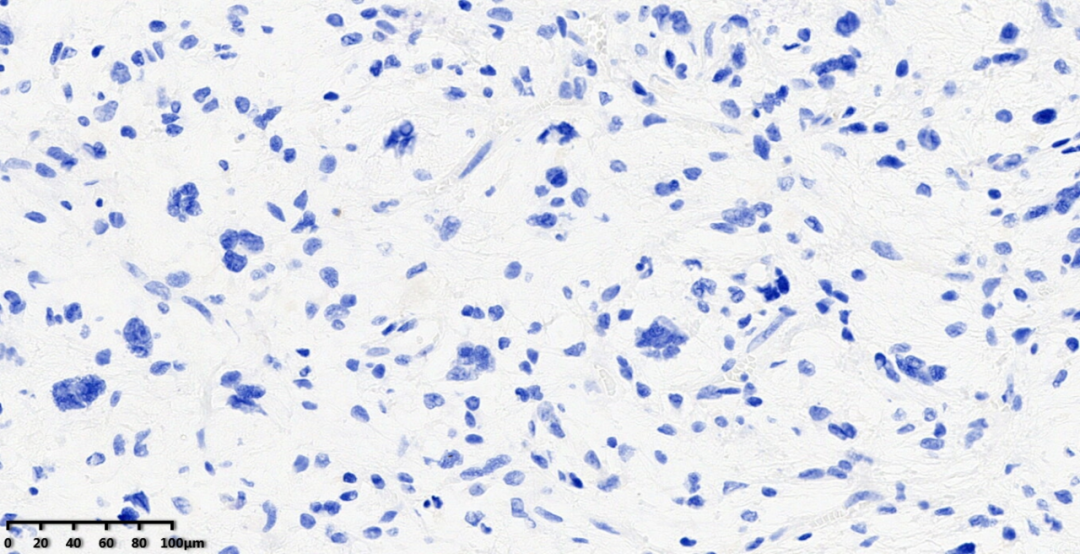
图18:肿瘤细胞不表达S100标记。
免疫组化结果如下:
阳性标记:CDK4、MDM2散在+、Ki-67(热点区约70%)
阴性标记:desmin、SMA、Myogenin、S100、CgA、Syn等
分子检测:
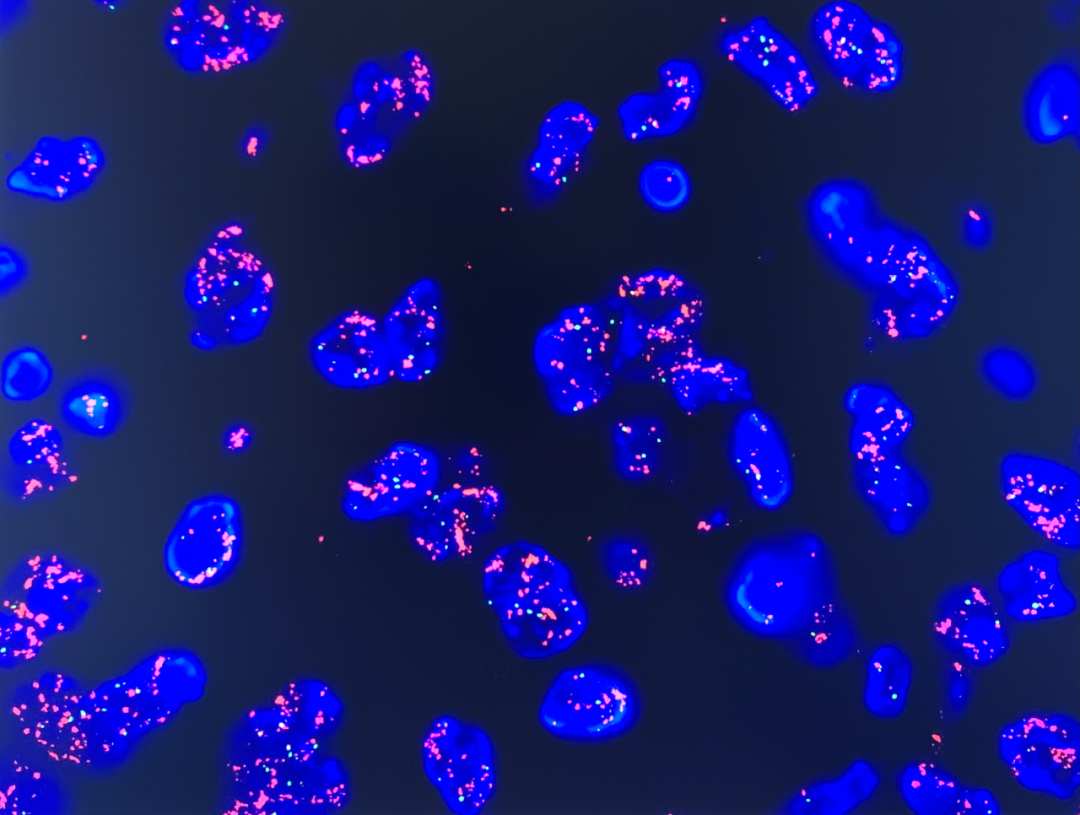
1. 检测到MDM2基因扩增,阳性细胞比例为80%,检测到50%的细胞基因所在的12号染色体为多体。
2. 未检测到DDIT3基因断裂。
最终诊断:
【软组织包块切除标本】(腹膜后)形态结合免疫组化及分子检测结果支持去分化脂肪肉瘤,肿瘤侵及肠壁及肾实质;余处肠管、肠管两侧切缘未查见肿瘤组织。
讨 论
定义:去分化脂肪肉瘤(Dedifferentiated liposarcoma,DDLPS)是一种非典型脂肪瘤样肿瘤/高分化脂肪肉瘤(ALT/WDLPS),表现为原发性或复发性肉瘤(通常为非脂肪源性)的组织学分级变化。在大多数病例中,存在MDM2和CDK4的扩增。分化良好的成分可能无法识别。
ICD-O编码:8858/3
发病部位:DDLPS最常发生于腹膜后,其他位置包括精索、纵隔、头颈和躯干。发生在皮下软组织极为罕见。
临床特征:DDLPS通常表现为一个巨大的无痛性肿块,可偶然发现(特别是在腹膜后)。在四肢部位,患者有长期肿块史,近期肿块体积增大通常表明去分化。影像学常显示脂肪瘤性和非脂肪瘤性实性成分共存。
流行病学:DDLPS是脂肪肉瘤的一种常见形式,在腹膜后的多形性肉瘤中占多数。高达10%的高分化脂肪肉瘤发生去分化,深层(特别是腹膜后)病变的风险较高,而四肢的风险明显较低。DDLPS与ALT/WDLPS好发人群相同,无明显性别差异。大约90%的病例是初发,10%是复发的。
病理特征
大体特征:通常由大的多结节状黄色肿块组成。切面颜色、质地与肿瘤成分相关,去分化区域通常呈褐色至灰白色伴质韧或鱼肉样切面;高分化区域呈黄色或脂肪样。出血坏死常见。
镜下特征:DDLPS的组织学特征是从ALT/WDLPS向非脂源性肉瘤转变。大多数情况下为高级别肉瘤。去分化的程度是可变的,过渡通常是突然的。偶尔也可以缓慢过渡,并且低级别和高级别肉瘤区域混合存在。在某些情况下,分化良好的脂肪瘤样成分难以识别。去分化区域组织形态学图谱宽泛,但最常见的是类似未分化多形性肉瘤或中高级别黏液纤维肉瘤。尽管去分化成分最初是由高级别形态学定义的,但低级别去分化的病例越来约多的被发现。低级别去分化肉瘤成分最常见的特征是存在均匀的梭形成纤维细胞,伴有轻度核异型性,通常呈束状排列,表现为中等细胞密度,介于分化良好的硬化性脂肪肉瘤和高级别肉瘤之间。低级别DDLPS不应与非典型梭形细胞脂肪瘤相混淆,后者含有非典型脂肪细胞或脂肪母细胞,而去分化区域无论是低级别还是高级别,通常都不含脂肪。约5-10%的病例可伴有异源性分化,最常见的异源分化是肌源性或骨肉瘤/软骨肉瘤,罕见血管肉瘤的报道。DDLPS的去分化区域瘤细胞可呈现出席纹状、脑膜皮细胞样形态,类似于神经增生或隆突性皮肤纤维肉瘤形态,其可能与化生性骨形成相关。局部复发的DDLPS也可呈完全分化良好的形态。偶尔,高级别成分可表现出明显的脂肪母细胞分化,要么表现为单个脂肪母细胞分散于高级别成分中,要么表现为非典型多形性脂肪细胞片状排列,导致该区域与多形性脂肪肉瘤在形态上难以区分,这种现象被称为同源性脂肪母细胞分化或多形性脂肪肉瘤样特征。少见孤立性纤维性肿瘤样形态和炎性肌纤维母细胞性肿瘤样形态。也可出现显著的黏液样间质形态,通常类似于中至高级别黏液纤维肉瘤,罕见黏液样脂肪肉瘤形态。
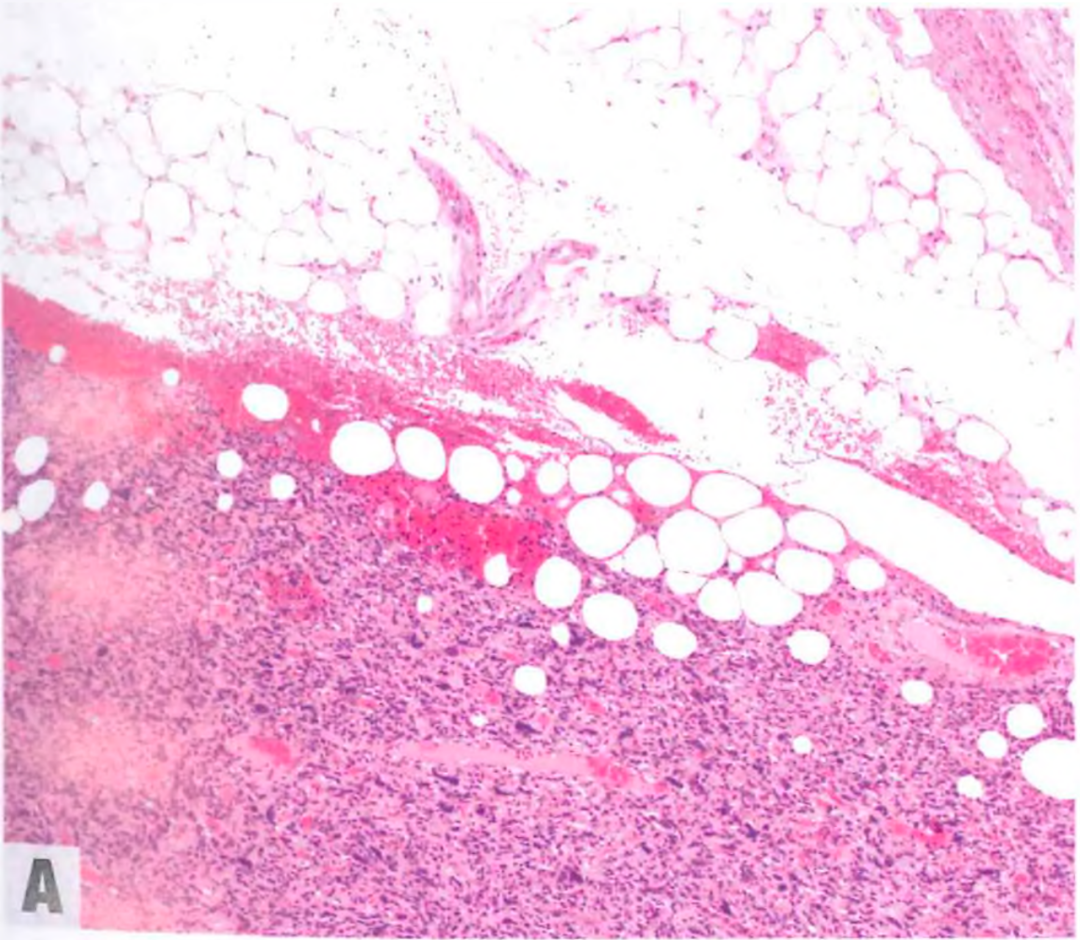
从高分化脂肪肉瘤突变转变为高级别非脂肪源性多形性肉瘤。
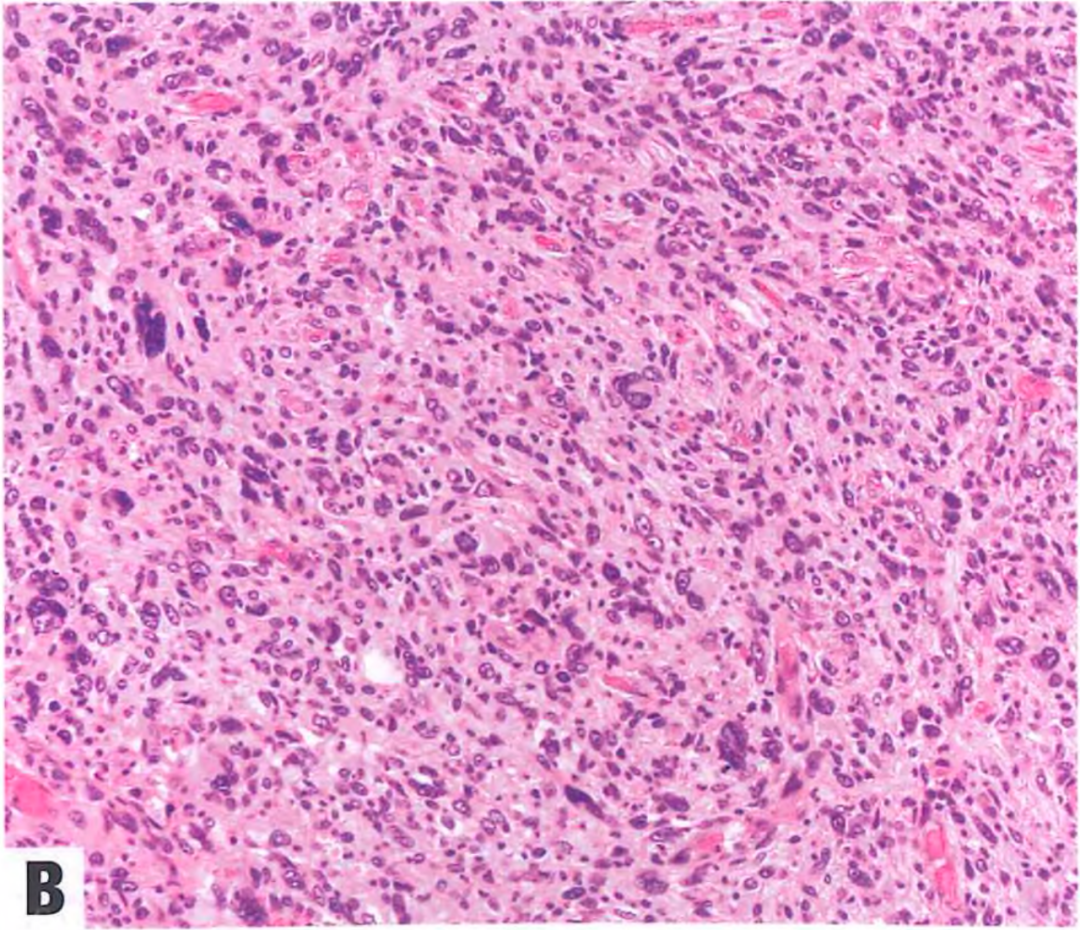
去分化成分的形态通常与未分化多形性肉瘤的形态重叠。
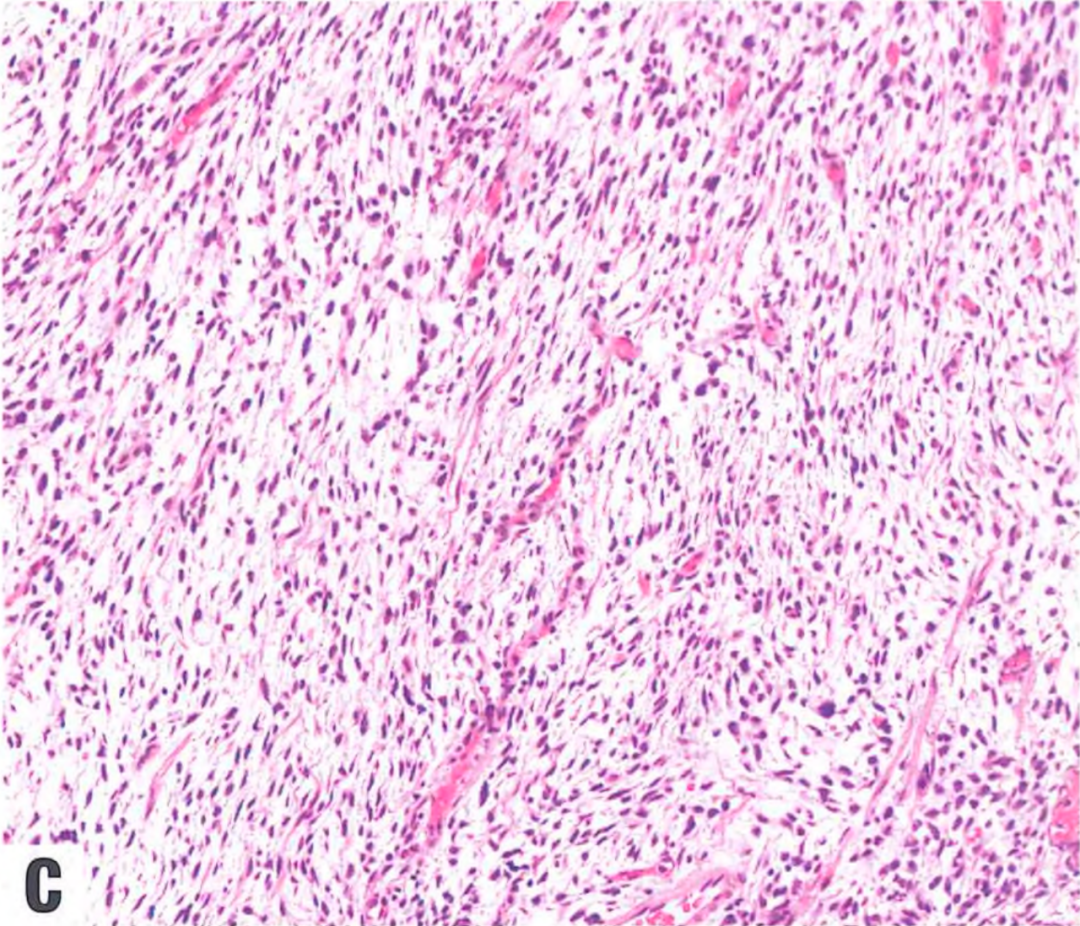
去分化成分的形态可与黏液纤维肉瘤相同。
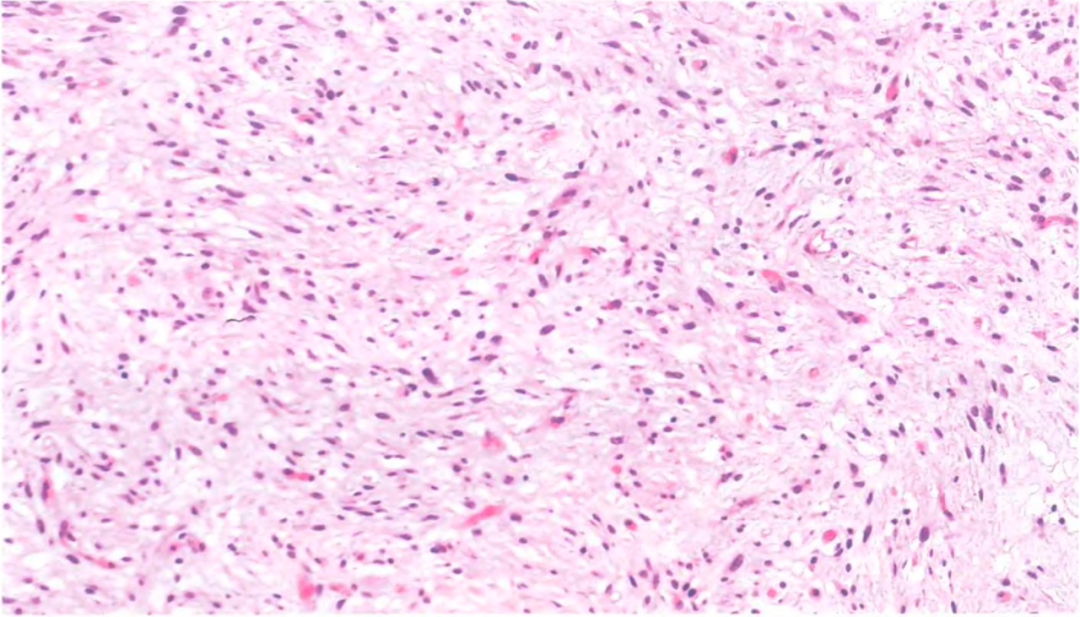
低级别去分化成分最常见的特征是存在均匀的成纤维梭形细胞,伴有轻度核异型性。
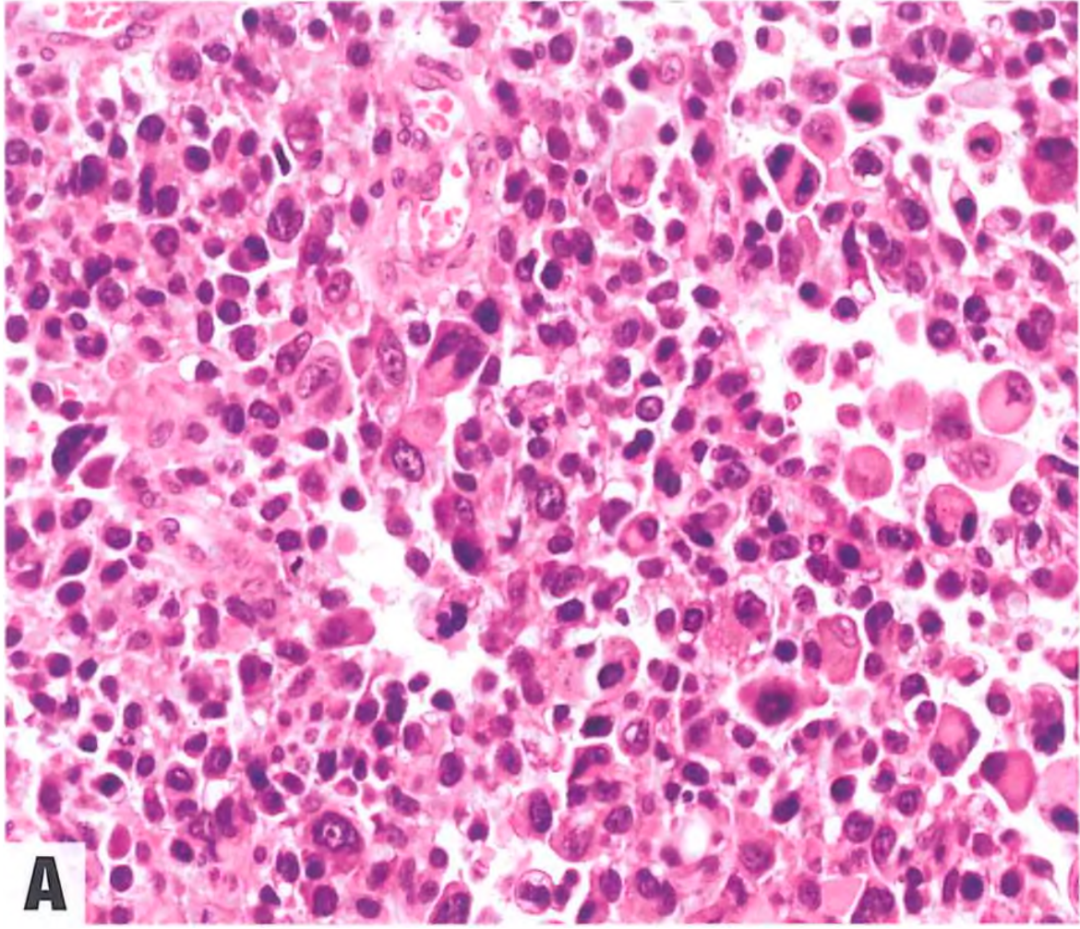
在DDLPS中,横纹肌母细胞分化是最常见的异源性分化类型。
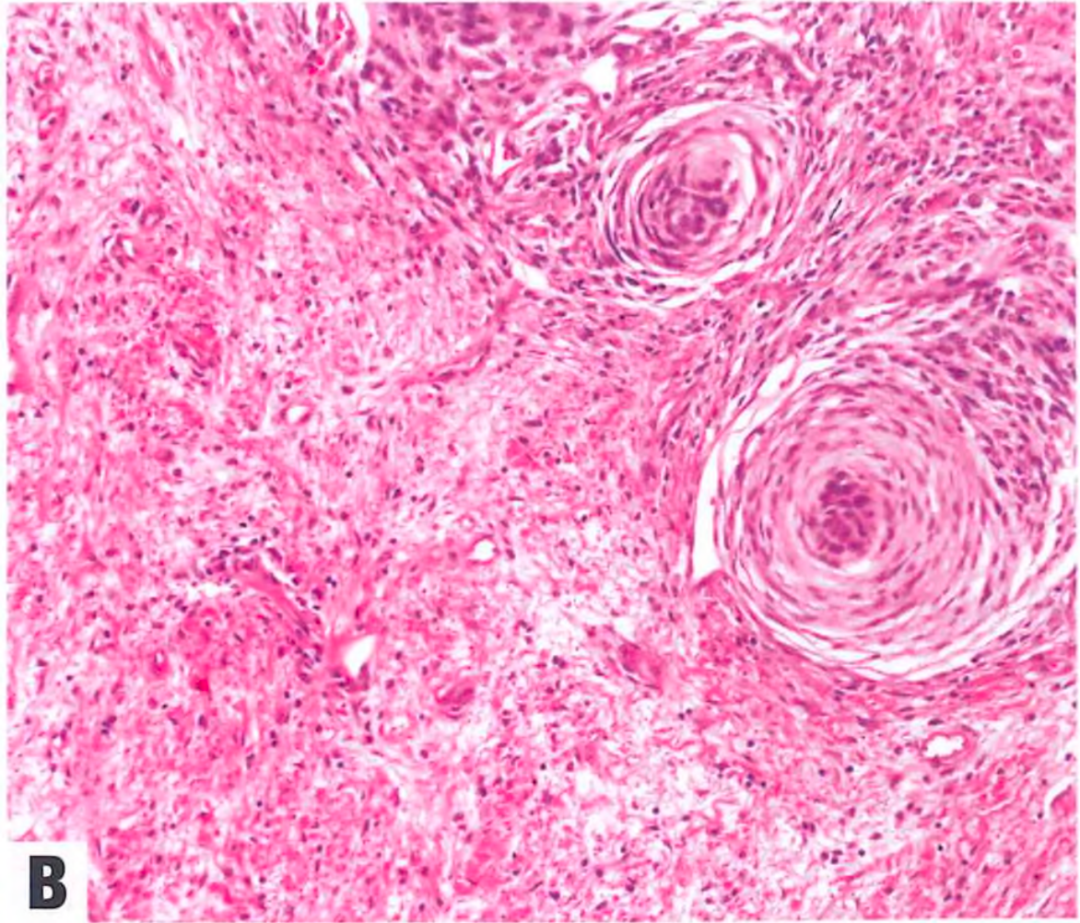
DDLPS可表现为独特的漩涡状结构(罕见),类似于神经或脑膜上皮结构。
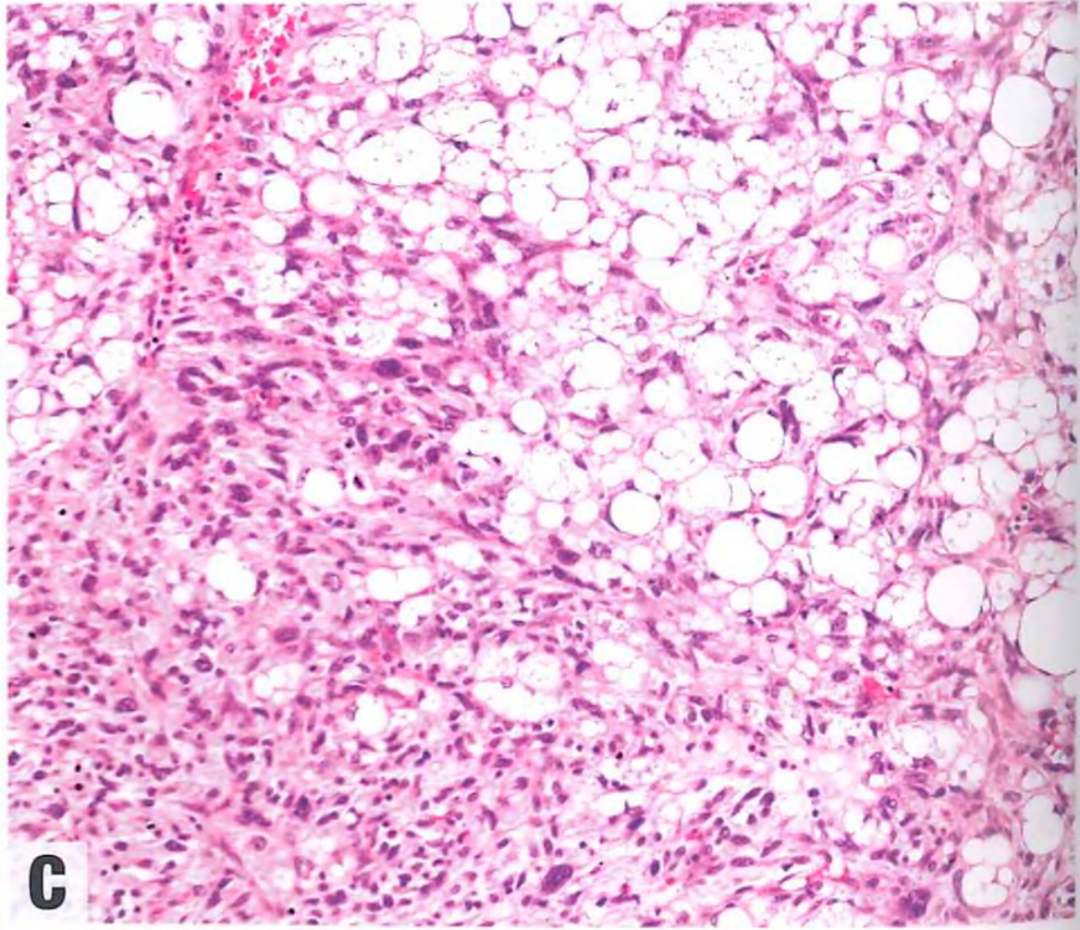
去分化成分表现出显著的脂源性分化(罕见)。
免疫表型:大部分病例弥漫性核MDM2及CDK4阳性。不同程度表达SMA、desmin及CD34标记。INI1核表达保留,H3K27me3核表达通常保留。非脂肪源性区域中的异源性成分可表达相应的标记物。
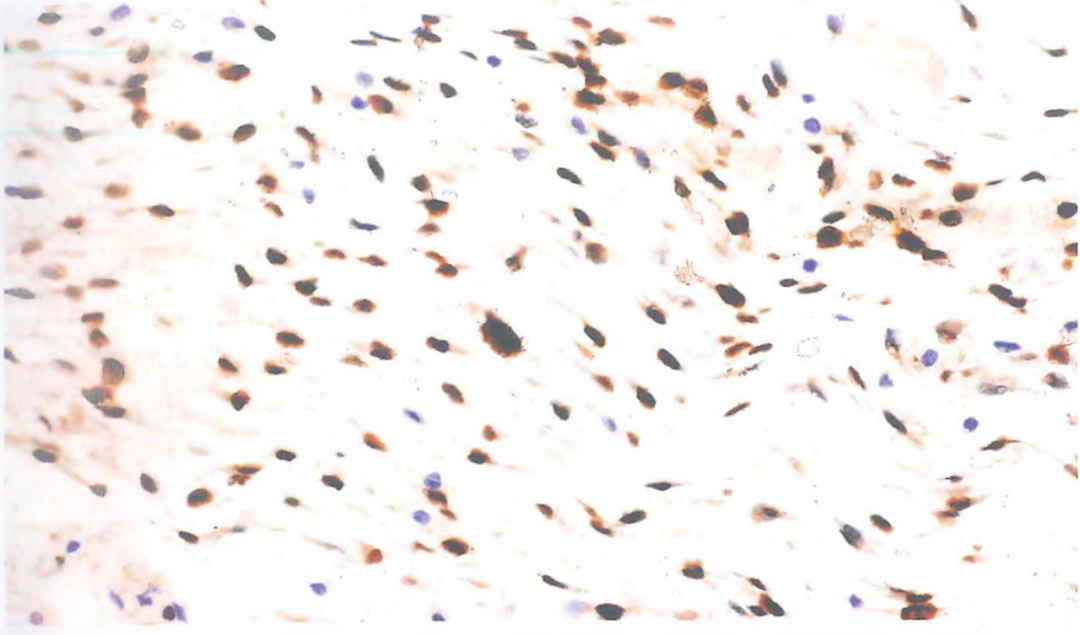
MDM2标记在DDLPS中表现为弥漫一致的核阳性。
分子特征:经MDM2和CDK4基因扩增,30%的病例伴有ATRX缺失。
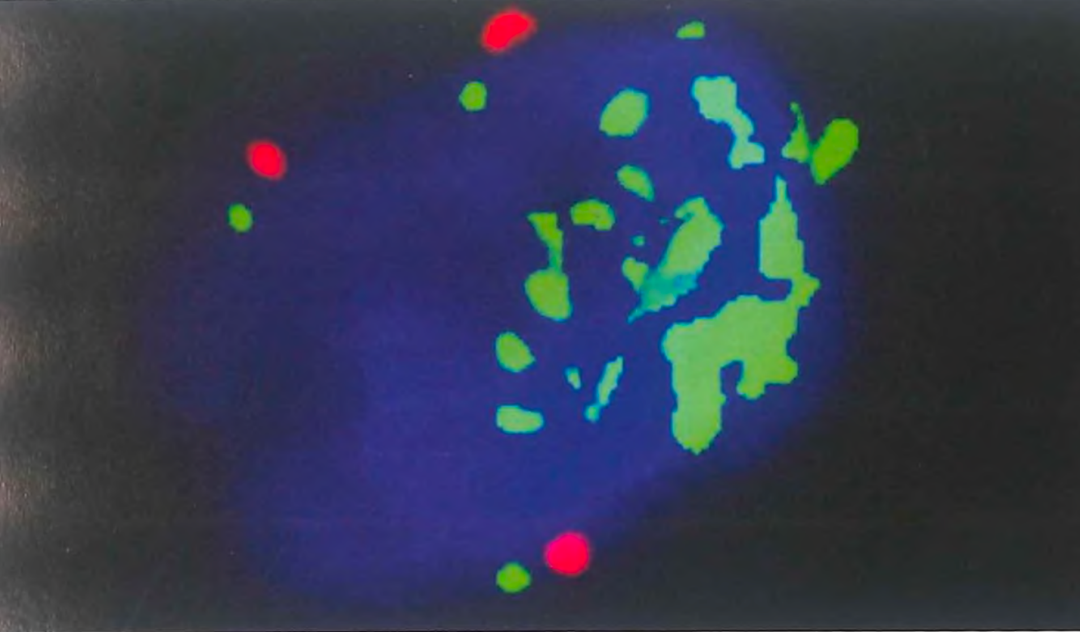
间期FISH显示MDM2高水平扩增。
治疗:完整手术切除,切缘阴性;对于体积大、多灶性腹膜后/腹腔内肿瘤行瘤体灭活术,可能需要切除部分或完整的腹腔内脏器。
预后:至少40%的病例局部复发。然而,如果患者随访10-20年,几乎所有腹膜后病例都会局部复发。15-20%的病例观察到远处转移,5年随访时的总死亡率为28~30%,长期随访后估计死亡率更高。解剖部位是最重要的预后因子,腹膜后或腹腔内肿瘤临床生物学行为最差。去分化区域的范围并不能预测预后,腹膜后肿瘤中出现高级别形态与生存率下降有关,出现肌源性(尤其是横纹肌母细胞性)的去分化成分与生存率降低有关;上皮样形态显著时预示着临床生物学行为侵袭度更高。

鉴别诊断
1. 多形性未分化肉瘤:是一种由多形性梭形细胞和多边形细胞组成的高级别肉瘤,无特异性分化,属于一种排除性诊断。组织学上无明确分化方向(如脂肪母细胞、骨样组织形成、上皮结构),可呈席纹状、条束状或无结构排列的高度异型梭形和(或)多形性细胞。免疫组化主要用于排除其他诊断,无特异性遗传学异常。
2. 黏液纤维肉瘤:与DDLPS好发部位不同,该疾病好发于四肢和腰带,腹膜后和腹腔内极为罕见。镜下通常为多结节状伴不完整的纤维间隔,黏液样间质和特征性细长曲线样薄壁血管,可见假脂肪母细胞。无ALT/WDLPS的组成成分,无MDM2扩增。
3. 多形性脂肪肉瘤:高级别肉瘤,含有数量不等的多形性脂肪母细胞,没有其他特定的分化。最常见于50岁以上患者,男性略多,好发于四肢深部软组织,常见于躯干,也可发生于腹膜后;脂肪母细胞显示有明显的异型性;脂肪母细胞常S100 阳性,上皮样亚型显示局灶EMA阳性,MDM2、CDK4阴性;FISH检测MDM2基因无扩增。
4. 高分化脂肪肉瘤:可具有富于细胞区域,较少或无核分裂象;大体缺乏明显的纤维性或肉瘤样外观。镜下通常可见明显大小不一的脂肪空泡及脂肪母细胞,间质可见不规则、核深染和多形性的非典型梭形细胞。免疫组化:大多数病例中MDM2和/或CDK4核阳性表达;S100脂肪细胞及脂肪母细胞阳性,间质异型细胞P16阳性。FISH检测:MDM2和CDK4基因扩增。
5. 非典型性梭形细胞/多形性脂肪瘤样肿瘤:梭形细胞形态温和、含有“绳索样”胶原、成熟脂肪组织、黏液样间质和肥大细胞以不比例混合构成,无肿瘤性坏死。免疫组化缺乏显著的MDM2、CDK4表达;在大约50-70%的病例中观察到Rb1的核表达缺失;分子检测显示无MDM2或CDK4扩增。
6. 黏液样脂肪肉瘤:由原始的非脂肪源性间叶细胞及数目不等的成脂肪细胞,以及具有特征性分支状毛细血管网结构的显著黏液样间质组成的恶性肿瘤。存在特征性的t(12;16)伴FUS-DDIT3融合而无MDM2扩增。
*本文(包括图片)均为作者投稿,临床图片来自西京医院公众号, 仅供行业交流学习用,不作为医疗诊断依据。
参考文献
1. WHO Classification of Tumours of Soft Tissue and Bone Tumours. 5h Edition.
2. Diagnostic Pathology: Soft Tissue Tumours (3 rd Edition).
3. Kyriazoglou, A, Pagkali, A, Kotsantis, I, et al. Well-differentiated liposarcomas and dedifferentiated liposarcomas: Systemic treatment options for two sibling neoplasms. CANCER TREAT REV. 2024; 125
4. Bourgeau, M, Gandhi, JS, Deeb, KK, et al. Superficial dedifferentiated liposarcoma: A clinicopathologic study. HUM PATHOL. 2024; 145 63-70.
5. Zhou, S, Zhang, C, Zhang, Z, et al. A novel HMGA2::KITLG fusion in a dedifferentiated liposarcoma with amplification of MDM2 and HMGA2. GENE CHROMOSOME CANC. 2023; 63 (1): e23200.
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言













#脂肪肉瘤# #去分化脂肪肉瘤# #DDLPS#
53