【AJH】Ph+ ALL完全分子学反应时异基因移植可改善生存和复发
2024-03-01 聊聊血液 聊聊血液 发表于上海
研究纳入日本成人白血病研究组(JALSG) TKI时代前瞻性研究中注册的、诊断后3个月内获得完全分子学反应 (CMR)的患者,以对比allo-SCT和非SCT队列的治疗结局。
Ph+ ALL异基因移植
异基因造血干细胞移植(allo-SCT)是费城染色体阳性急性淋巴细胞白血病(Ph+ ALL)的治愈性手段。虽然随着移植方法的进步,非复发死亡率(NRM)有所改善,但即使在完全缓解(CR)期进行移植,NRM仍超过15%。因此,是否应在首次完全缓解(CR1)期进行allo-SCT一直存在争议,且根据allo-SCT前的治疗和allo-SCT的患者选择(即allo-SCT的指征),结果也可能会有所不同;但由于供者的随机性,开展前瞻性随机试验以确定是否应该进行allo-SCT非常困难。
《American Journal of Hematology》近日发表一项日本回顾性研究,纳入日本成人白血病研究组(JALSG) TKI时代前瞻性研究中注册的、诊断后3个月内获得完全分子学反应 (CMR)的患者,以对比allo-SCT和非SCT队列的治疗结局。尽管它是一项回顾性研究,但因为初诊后的治疗方案一致,预计可以准确评估allo-SCT的影响。

研究方法
该分析作为JALSG Ph+ ALL TKI-SCT研究的一部分进行,后者是对TKI时代的3项JALSG前瞻性研究的整合分析,包括JALSG Ph+ALL202研究、Ph+ALL208研究和Ph+ALL213研究,分别研究伊马替尼、伊马替尼联合化疗、达沙替尼(分为两步)。三个研究均纳入15-64岁的新诊断Ph+ ALL患者。
当Ph+ALL202研究中有HLOA相合同胞供者、Ph+ALL208研究中有HLA相合亲属或无关供者、Ph+ALL213研究中有包括脐带血在内的合适供者时,建议CR1期行Allo-SCT。如果未行allo-SCT,则以伊马替尼作为TKI维持治疗,Ph+ALL 202或208方案患者从获得CR之日起继续使用2年;未提供移植后TKI,由各移植中心自行决定。在接受Ph+ALL213方案治疗的患者中,达沙替尼每5周给药4周,共12个周期;对于allo-SCT时MRD为阴性的患者,未给予移植后达沙替尼,而对于allo-SCT时MRD为阳性的患者,给予移植后达沙替尼。
患者纳入标准:通过定量聚合酶链反应(qPCR),诊断后3个月内达到CR并获得CMR,且诊断后3个月的后续评估仍为CMR的患者。排除早期死亡(定义为诊断后<3个月死亡)或随访<3个月的患者。
研究结果
患者
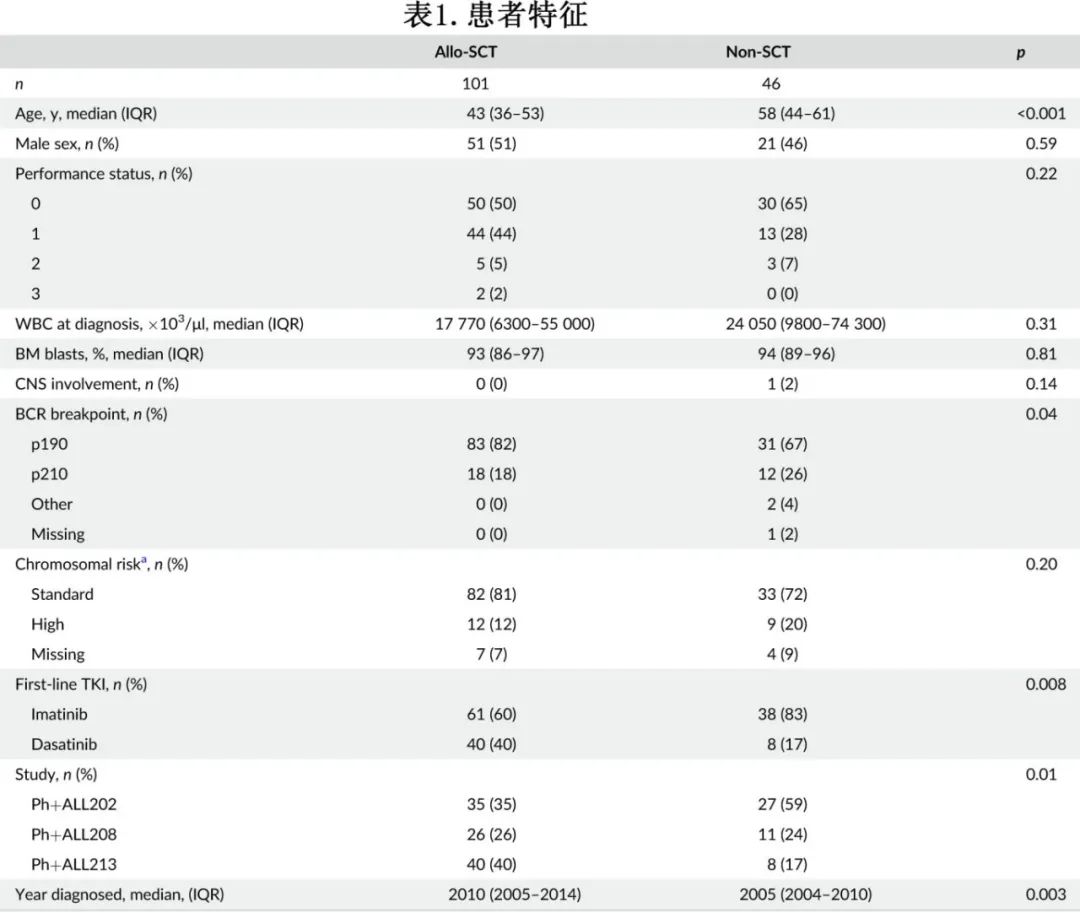
研究纳入147例患者(allo-SCT101例;非SCT46例),患者特征见表1。allo-SCT和非SCT队列的中位随访时间分别为5.9年和4.8年。62例采用JALSG Ph+ALL 202方案治疗,37例采用Ph+ALL 208方案治疗,48例采用Ph+ALL 213方案治疗。移植和非移植队列在性别、诊断时的体能状态、诊断时的WBC、诊断时的骨髓原始细胞百分比和染色体风险方面平衡,但allo-SCT队列较年轻(中位年龄43岁 vs 58岁;p<0.001),此外接受达沙替尼作为一线TKI的患者中allo-SCT较多(40% vs 17%;P=0.008)。
Allo-SCT
骨髓是最常见的干细胞来源(骨髓为55%;外周血为19%;脐带血为15%),超过半数来自无关供者(亲缘供者为39%;无关供者为61%)。大多数患者的HLA完全相合(55%)或部分相合(33%)。77%的患者接受清髓性预处理(MAC), 73%的患者接受全身照射作为预处理方案的一部分。确诊至allo-SCT的中位时间为168天,CR至allo-SCT的中位时间为128天。11例患者(11%)在确诊后126天和移植前13 天检测到BCR::ABL1。
10例患者(10%)在allo-SCT后中位261 天开始接受移植后TKI治疗,移植后维持治疗包括30%的患者使用伊马替尼和70%的患者使用达沙替尼;分别有40%、50%和10%的患者维持治疗<1年、1~3年和>3年。在非SCT队列中发生复发的26例患者中,12例(46%)在CR1之后接受allo-SCT。
未校正的分析
allo-SCT队列的5年总生存率(OS) (73% vs 41%,p=0.0004)和无复发生存率(RFS)(68% vs 30%,p<0.0001)均显著优于非SCT队列。在单因素分析中,染色体风险和TKI均与OS和RFS相关。虽然两个队列的5年非复发死亡率(NRM)无显著差异(17% vs 10%,p=0.17),但alloSCT队列的5年复发率(RR)显著较低(17% vs 60%,p<0.0001)(图1A-D)。在非SCT队列中,6例患者发生分子学复发,即在血液学复发前MRD转为阳性,但最终均出现血液学复发。在非SCT队列中,没有患者在诊断后180天内因复发而死亡。

在allo-SCT队列中,3个月时II-IV级和III-IV级急性GVHD的累积发生率分别为37%和5%,所有和广泛型慢性GVHD的5年累积发生率分别为36%和19%。在allo-SCT和非SCT队列中,5年GRFS(无GVHD无复发生存率)分别为51%和30% (p=0.01)(图1E)。
多因素分析
鉴于基线特征的显著差异,进行了针对年龄、TKI、WBC和染色体风险进行校正的多因素分析。allo-SCT与OS (校正风险比(aHR)=0.54;p=0.04)和无复发生存率(aHR=0.21;p<0.001) 均显著相关,包括WBC、TKI和染色体风险同样如此。allo-SCT组的5年校正OS和RFS分别为73%和70%,而非SCT组分别为50%和20%。allo-SCT与较低的RR显著相关(aHR=0.10;p<0.001),包括年龄和染色体风险也是如此。另一方面,allo-SCT与较高的NRM显著相关(aHR=3.49;p=0.03), 包括TKI也是如此。allo-SCT队列的5年校正RR和NRM分别为14%和17%,而非SCT队列分别为73%和5%。allo-SCT队列从诊断至复发的中位时间比非SCT队列长(17.0个月 vs 8.8个月;P=0.003)。即使非SCT队列仅限于在计划的维持治疗期之前未发生事件的患者,allo-SCT队列的5年校正RR也显著较低(12% vs 46%;p=0.04)。Allo-SCT也与较好的GRFS显著相关(aHR= 0.43;p=0.002),包括WBC和染色体风险同样如此;allo-SCT队列和非SCT队列的5年校正GRFS分别为50%和20% (图2)。
虽然年龄作为连续变量纳入多因素模型,但使用两个年龄组(≤50岁和>50岁)作为变量进行多因素分析后发现,虽然在≤50岁组allo-SCT对RFS (aHR=0.12;p<0.001)和GRFS (aHR=0.29;p=0.001)表现明显,但在>50岁组并非RFS (aHR= 0.44;p=0.08)或GRFS (aHR=0.53;P=0.15) 的显著因素。
倾向性评分(PS)分析
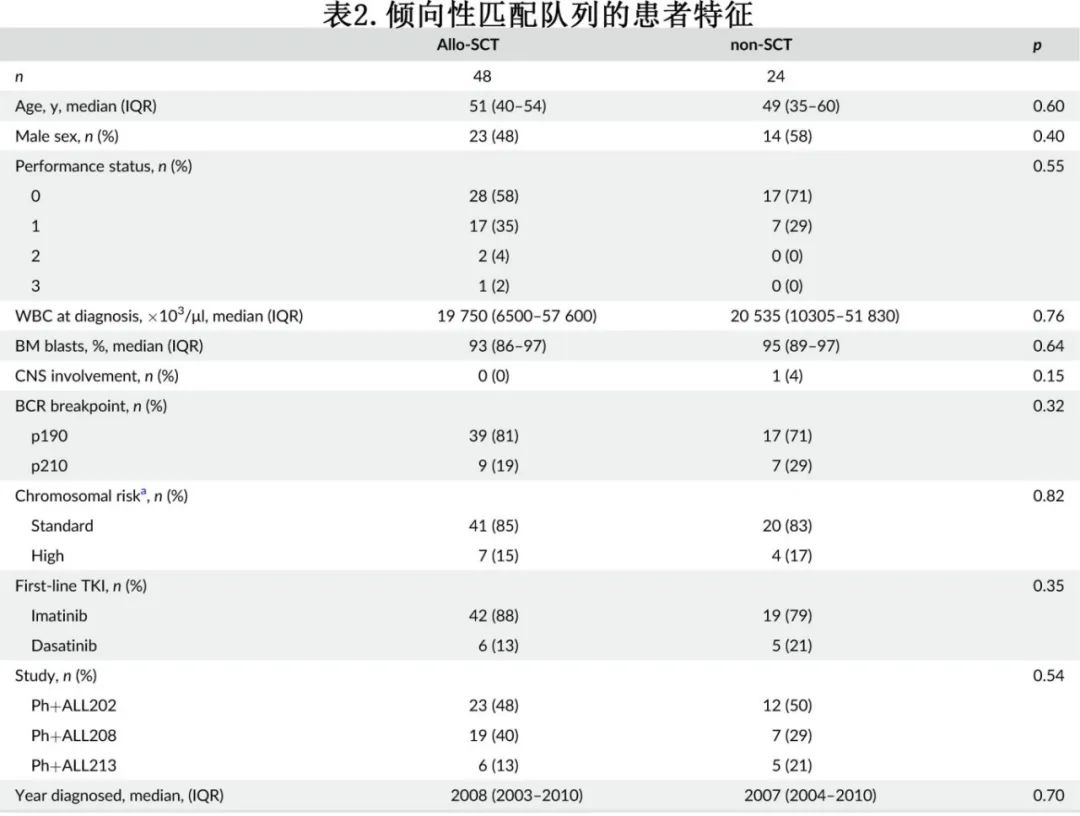
对两个队列的结局进行以2∶1匹配的倾向性评分匹配的验证性分析。选择48例allo-SCT队列患者和24例非SCT队列患者,基线特征很平衡(表2)。
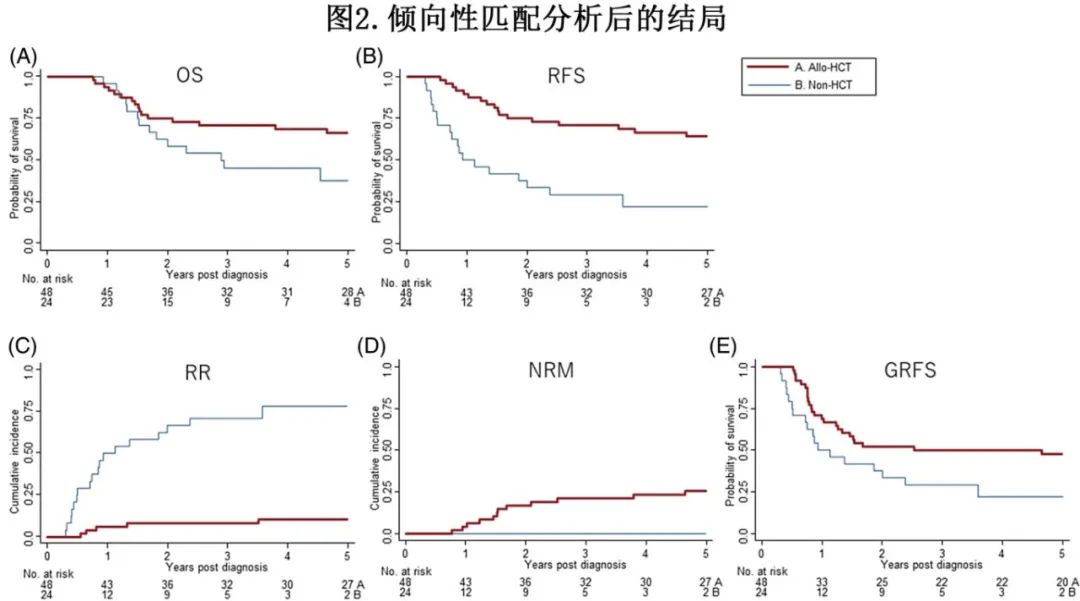
PS匹配分析证实了多因素分析的结果,allo-SCT队列的5年OS优于非SCT队列,但具有边缘显著性(66% vs. 38%;p=0.052),而RFS显著更优(64% vs 22%;P=0.0001)。allo-SCT队列的5年RR显著较低(11% vs 78%;p<0.0001),但5年NRM显著较高(25% vs 0%;P=0.01)。在allo-SCT和非SCT队列之间,从诊断至复发的中位时间无显著差异(9.8个月vs. 9.6个月;P=0.59)。同样,当非SCT队列仅限于在计划的维持治疗期之前未发生事件的患者时,allo-SCT队列的5年RR显著较低(11% vs 48%;p=0.02),且5年GRFS显著较高(48% vs 22%;p=0.03)(图2)。
总结
该分析是对TKI时代在JALSG进行的3项前瞻性临床研究的综合分析,表明对于确诊3个月内获得CMR的Ph+ALL患者,CR1期allo-SCT可获得较好的生存和较低的RR。虽然非SCT队列的NRM较低,但其影响有限,而allo-SCT队列的结局仍然良好,即使在GRFS方面也是如此(而这令人惊讶,或许是日本人群中GVHD发生率较低)。非SCT队列在维持治疗期后观察到复发,提示需要长期治疗策略,尤其是在没有同种免疫的情况下。PS分析可用于调和两队列之间的背景差异,但也必须承认,使用PS分析的患者主要是接受伊马替尼治疗的患者。本研究的结果是基于将伊马替尼作为大多数患者的主要TKI的研究结果,因此可能无法直接外推到二代或三代TKI,它们还需要更多的研究来验证allo-SCT的有效性。随机对照试验可能有助于阐明allo-SCT的作用,但由于需要长期随访才能准确解读结果,因此还需要考虑治疗方法不断发展的可能性,例如引入新药。
参考文献
Nishiwaki S, Sugiura I, Fujisawa S, et al. Utility of allogeneic stem cell transplantation for adult Ph +ALL with complete molecular remission. Am J Hematol. 2024;1‐10. doi:10.1002/ajh.27237
本网站所有内容来源注明为“梅斯医学”或“MedSci原创”的文字、图片和音视频资料,版权均属于梅斯医学所有。非经授权,任何媒体、网站或个人不得转载,授权转载时须注明来源为“梅斯医学”。其它来源的文章系转载文章,或“梅斯号”自媒体发布的文章,仅系出于传递更多信息之目的,本站仅负责审核内容合规,其内容不代表本站立场,本站不负责内容的准确性和版权。如果存在侵权、或不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
在此留言















#急性淋巴细胞白血病# #异基因造血干细胞移植#
104